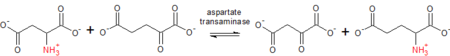Аспартаттрансаминаза - Aspartate transaminase
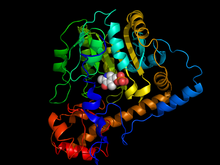 Аспартатаминотрансфераза из Escherichia coli связывается с кофактором пиридоксаль-5-фосфатом .
| |||||||||
| Идентификаторы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| ЕС нет. | 2.6.1.1 | ||||||||
| № CAS | 9000-97-9 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
Аспартаттрансаминаза ( AST ) или аспартатаминотрансфераза , также известная как AspAT / ASAT / AAT или (сывороточная) глутаминовая щавелевоуксусная трансаминаза ( GOT , SGOT ), представляет собой пиридоксальфосфат (PLP) -зависимый фермент трансаминазы ( EC 2.6.1.1 ), который был первым описанный Артуром Карменом и его коллегами в 1954 году. AST катализирует обратимый перенос α-аминогруппы между аспартатом и глутаматом и, как таковой, является важным ферментом в метаболизме аминокислот. АСТ содержится в печени , сердце , скелетных мышцах , почках , головном мозге и эритроцитах. Уровень AST в сыворотке, уровень ALT ( аланинтрансаминазы ) и их соотношение (отношение AST / ALT ) обычно измеряются клинически как биомаркеры здоровья печени. Анализы являются частью панелей крови .
Полураспада общего AST в обращении приблизительно 17 часов и, в среднем, 87 часов для митохондриальной АСТ. Aminotransferase очищается синусоидальных клеток в печени.
Функция
Аспартаттрансаминаза катализирует взаимное превращение аспартата и α-кетоглутарата в оксалоацетат и глутамат .
L-аспартат (Asp) + α-кетоглутарат ↔ оксалоацетат + L-глутамат (Glu)
Как прототип трансаминазы, AST полагается на PLP (витамин B6) в качестве кофактора для переноса аминогруппы с аспартата или глутамата на соответствующую кетокислоту . При этом кофактор перемещается между PLP и формой пиридоксаминфосфата (PMP). Перенос аминогруппы, катализируемый этим ферментом, имеет решающее значение как для деградации аминокислот, так и для биосинтеза. При разложении аминокислот после превращения α-кетоглутарата в глутамат глутамат впоследствии подвергается окислительному дезаминированию с образованием ионов аммония , которые выводятся в виде мочевины . В обратной реакции аспартат может быть синтезирован из оксалоацетата, который является ключевым промежуточным продуктом в цикле лимонной кислоты .
Изоферменты
Два изофермента присутствуют в большом количестве эукариот. В людях:
- GOT1 / cAST, цитозольный изофермент происходит в основном из красных кровяных телец и сердца .
- GOT2 / mAST, митохондриальный изофермент присутствует преимущественно в печени.
Считается, что эти изоферменты произошли от общего предкового AST посредством дупликации генов, и они имеют гомологию последовательностей примерно 45%.
AST также был обнаружен у ряда микроорганизмов, включая E. coli , H. mediterranei и T. thermophilus . В E. coli фермент кодируется геном aspC , и было также показано, что он проявляет активность трансаминазы ароматических аминокислот ( EC 2.6.1.57 ).
Состав
Были проведены исследования рентгеновской кристаллографии для определения структуры аспартаттрансаминазы из различных источников, включая митохондрии курицы, цитозоль сердца свиньи и кишечную палочку . В целом, трехмерная структура полипептидов для всех видов очень похожа. AST представляет собой димер , состоящий из двух идентичных субъединиц, каждая из которых имеет приблизительно 400 аминокислотных остатков и имеет молекулярную массу приблизительно 45 кДа. Каждая субъединица состоит из большого и малого домена, а также третьего домена, состоящего из N-концевых остатков 3-14; эти несколько остатков образуют цепь, которая связывает и стабилизирует две субъединицы димера. Большой домен, который включает остатки 48-325, связывает кофактор PLP через альдиминовую связь с ε-аминогруппой Lys258. Другие остатки в этом домене - Asp 222 и Tyr 225 - также взаимодействуют с PLP посредством водородных связей . Малый домен состоит из остатков 15-47 и 326-410 и представляет собой гибкую область, которая переводит фермент из «открытой» в «закрытую» конформацию при связывании субстрата.
Два независимых активных сайта расположены рядом с интерфейсом между двумя доменами. Внутри каждого активного сайта пара остатков аргинина отвечает за специфичность фермента в отношении субстратов дикарбоновых кислот : Arg386 взаимодействует с проксимальной (α-) карбоксилатной группой субстрата, в то время как Arg292 образует комплексы с дистальным (боковая цепь) карбоксилатом.
Что касается вторичной структуры, AST содержит как α-, так и β-элементы. Каждый домен имеет центральный лист β-тяжей с α-спиралями, упакованными с обеих сторон.
Механизм
Аспартаттрансаминаза, как и все трансаминазы, действует посредством распознавания двойного субстрата; то есть он способен распознавать и избирательно связывать две аминокислоты (Asp и Glu) с разными боковыми цепями. В любом случае трансаминазная реакция состоит из двух одинаковых полуреакций, которые составляют то, что называется механизмом пинг-понга . В первой полуреакции аминокислота 1 (например, L-Asp) реагирует с комплексом фермент-PLP с образованием кетокислоты 1 (оксалоацетат) и модифицированного фермента-PMP. Во второй полуреакции кетокислота 2 (α-кетоглутарат) реагирует с ферментом-PMP с образованием аминокислоты 2 (L-Glu), регенерируя в процессе исходный фермент-PLP. Образование рацемического продукта (D-Glu) происходит очень редко.
Конкретные стадии полуреакции фермент-PLP + аспартат ⇌ фермент-PMP + оксалоацетат следующие (см. Рисунок); другая полуреакция (не показана) протекает в обратном порядке с α-кетоглутаратом в качестве субстрата.
- Образование внутреннего альдимина : Во-первых, ε-аминогруппа Lys258 образует связь основания Шиффа с углеродом альдегида с образованием внутреннего альдимина.
- Трансальдиминирование: внутренний альдимин затем становится внешним альдимином, когда ε-аминогруппа Lys258 замещается аминогруппой аспартата. Эта реакция трансальдиминирования происходит через нуклеофильную атаку депротонированной аминогруппой Asp и протекает через тетраэдрический промежуточный продукт. На этом этапе карбоксилатные группы Asp стабилизируются гуанидиниевыми группами остатков фермента Arg386 и Arg 292.
- Образование хиноноидов : водород, присоединенный к α -углероду Asp, затем извлекается (считается, что Lys258 является акцептором протонов) с образованием промежуточного хиноноида.
- Образование кетимина : хиноноид репротонируется, но теперь на углероде альдегида, с образованием промежуточного кетимина.
- Гидролиз кетимина : наконец, кетимин гидролизуется с образованием PMP и оксалоацетата.
Считается, что этот механизм имеет несколько этапов, частично определяющих скорость . Однако было показано, что стадия связывания субстрата (трансальдиминирование) продвигает каталитическую реакцию вперед.
Клиническое значение
AST похож на аланинтрансаминазу (ALT) в том, что оба фермента связаны с паренхиматозными клетками печени . Разница в том, что АЛТ обнаруживается преимущественно в печени, при этом незначительные количества обнаруживаются в почках, сердце и скелетных мышцах, тогда как АСТ обнаруживается в печени, сердце ( сердечной мышце ), скелетных мышцах, почках, головном мозге и красном цвете. кровяные клетки. В результате АЛТ является более специфическим индикатором воспаления печени, чем АСТ, поскольку АСТ может быть повышен также при заболеваниях, поражающих другие органы, таких как инфаркт миокарда , острый панкреатит , острая гемолитическая анемия , тяжелые ожоги, острое заболевание почек, заболевания опорно-двигательного аппарата, и травма.
AST был определен как биохимический маркер для диагностики острого инфаркта миокарда в 1954 году. Однако использование AST для такого диагноза в настоящее время излишне и заменено сердечными тропонинами .
Лабораторные тесты всегда следует интерпретировать с использованием эталонного диапазона из лаборатории, проводившей тест. Примеры эталонных диапазонов показаны ниже:
| Тип пациента | Референсные диапазоны |
| Мужчина | 8–40 МЕ / л |
| женский | 6–34 МЕ / л |
Смотрите также
- Аланинтрансаминаза (ALT / ALAT / SGPT)
- Трансаминазы
использованная литература
дальнейшее чтение
- Jansonius, JN ; Винсент, MG (1987). «Структурная основа катализа аспартатаминотрансферазой». В Jurnak FA; Макферсон А (ред.). Биологические макромолекулы и сборки . 3 . Нью-Йорк: Вили. С. 187–285. ISBN 978-0-471-85142-4.
- Курамицу С., Окуно С., Огава Т., Огава Х., Кагамияма Х. (1985). «Аспартатаминотрансфераза Escherichia coli: нуклеотидная последовательность гена aspC». J. Biochem . 97 (4): 1259–62. DOI : 10.1093 / oxfordjournals.jbchem.a135173 . PMID 3897210 .
- Кондо К., Вакабаяси С., Яги Т., Кагамияма Х. (1984). «Полная аминокислотная последовательность аспартатаминотрансферазы из Escherichia coli: сравнение последовательностей с изоферментами свиньи». Biochem. Биофиз. Res. Commun . 122 (1): 62–67. DOI : 10.1016 / 0006-291X (84) 90439-X . PMID 6378205 .
- Иноуэ К., Курамицу С., Окамото А., Хироцу К., Хигучи Т., Кагамияма Х. (1991). «Сайт-направленный мутагенез аспартатаминотрансферазы Escherichia coli: роль Tyr70 в каталитических процессах». Биохимия . 30 (31): 7796–7801. DOI : 10.1021 / bi00245a019 . PMID 1868057 .
внешние ссылки
- Аспартат + трансаминаза в Национальных медицинских предметных рубриках США (MeSH)
- AST - Лабораторные тесты онлайн
- AST: Медицинская энциклопедия MedlinePlus