Синдром Бругада - Brugada syndrome
| Синдром Бругада | |
|---|---|
| Другие имена | Синдром внезапной необъяснимой ночной смерти, бангунгут, синдром поккури смерти |
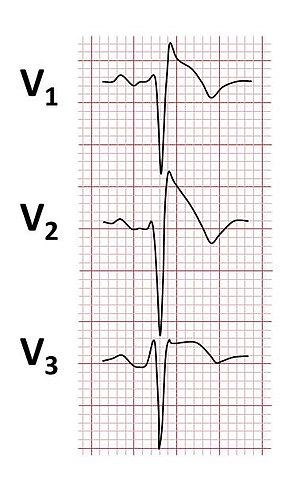 | |
| Типичные изменения ЭКГ 1-го типа при синдроме Бругада | |
| Специальность | Кардиология |
| Симптомы | Обморок , внезапная сердечная смерть |
| Обычное начало | Совершеннолетие |
| Причины | Генетика, некоторые лекарства |
| Факторы риска | Семейный анамнез, азиатское происхождение, мужчина |
| Диагностический метод | Электрокардиограмма (ЭКГ), генетическое тестирование |
| Дифференциальная диагностика | Синдром Романо-Варда , аритмогенная кардиомиопатия , мышечная дистрофия Дюшенна |
| Уход | Выжидательное , имплантируемые дефибрилляторы (ICD) |
| Частота | 1 на 2000 |
| Летальные исходы | 8% случаев внезапной сердечной смерти |
Синдром Бругада ( BrS ) - это генетическое заболевание, при котором электрическая активность сердца является аномальной. Это увеличивает риск нарушения сердечного ритма и внезапной сердечной смерти . У пострадавших могут быть эпизоды потери сознания . Нарушения сердечного ритма, наблюдаемые у людей с синдромом Бругада, часто возникают в состоянии покоя. Они могут быть спровоцированы лихорадкой .
Примерно у четверти людей с синдромом Бругада есть член семьи, который также страдает этим заболеванием. Некоторые случаи могут быть связаны с новой генетической мутацией или некоторыми лекарствами. Наиболее часто задействованным геном является SCN5A, кодирующий натриевый канал сердца . Диагноз обычно ставится на основании электрокардиограммы (ЭКГ), однако аномалии могут не присутствовать постоянно. Для выявления изменений ЭКГ могут использоваться такие лекарства, как аджмалин . Подобные модели ЭКГ могут наблюдаться при определенных нарушениях электролитного баланса или при снижении кровоснабжения сердца .
От синдрома Бругада нет лекарства. Людей с повышенным риском внезапной сердечной смерти можно лечить с помощью имплантируемого кардиовертера-дефибриллятора (ИКД). У тех, у кого нет симптомов, риск смерти намного ниже, и менее ясно, как лечить эту группу. Изопротеренол можно использовать в краткосрочной перспективе для тех, у кого часто возникают опасные для жизни нарушения сердечного ритма, в то время как хинидин можно использовать в более долгосрочной перспективе. Может быть рекомендовано тестирование членов семьи людей.
Заболевание поражает от 1 до 30 человек на 10 000 человек. Это чаще встречается у мужчин, чем у женщин, и у лиц азиатского происхождения. Симптомы появляются обычно в зрелом возрасте. Он назван в честь испанских кардиологов Педро и Хосепа Бругада, которые описали это заболевание в 1992 году. Их брат Рамон Бругада был первым, кто описал одну потенциальную генетическую причину в 1998 году.
Признаки и симптомы
Хотя многие из людей с синдромом Бругада не имеют никаких симптомов, синдром Бругада может вызвать обморок или внезапную сердечную смерть из-за серьезных нарушений сердечного ритма, таких как фибрилляция желудочков или полиморфная желудочковая тахикардия . Потеря сознания может быть вызвана кратковременными нарушениями сердечного ритма, которые самопроизвольно возвращаются к нормальному ритму. Если опасный сердечный ритм не прекращается сам по себе и не лечится, у человека может произойти остановка сердца со смертельным исходом. Тем не менее, у людей с синдромом Бругада, несмотря на нормальный сердечный ритм, могут возникать затемнения из-за внезапного падения артериального давления, известного как вазовагальный обморок .
Нарушения сердечного ритма, наблюдаемые при синдроме Бругада, часто возникают в состоянии покоя, после тяжелой еды или даже во время сна. Эти ситуации связаны с периодами активации блуждающего нерва , которые называются периодами высокого тонуса блуждающего нерва . Нарушения сердечного ритма также могут возникать во время лихорадки или после чрезмерного употребления алкоголя. Некоторые лекарства могут также ухудшать тенденцию к нарушению сердечного ритма у пациентов с синдромом Бругада, и этим пациентам следует избегать их приема.
Причины
Отдельные клетки сердца сообщаются друг с другом электрическими сигналами, и эти электрические сигналы нарушаются у людей с синдромом Бругада. Как генетическое заболевание синдром в конечном итоге вызван изменениями в ДНК человека , известными как генетические мутации . Первые мутации , описанные в связи с синдромом Бругады были в гене , ответственном за белок или канал иона , который регулирует поток ионов натрия через клеточную мембрану в клетках сердечной мышцы - сердца натриевых каналов . Многие из генетических мутаций, которые впоследствии были описаны в связи с синдромом Бругада, так или иначе влияют на натриевый ток или другие ионные токи.
Был описан длинный список факторов, которые могут вызвать картину ЭКГ Бругада, включая определенные лекарства, электролитные нарушения, такие как снижение уровня калия в крови и снижение кровоснабжения ключевых областей сердца, в частности выводящий тракт правого желудочка . К лекарствам, которые были причастны, относятся антиаритмические препараты, такие как флекаинид , верапамил и пропранолол , антидепрессанты, такие как амитриптилин , и препараты, повышающие тонус блуждающего нерва, такие как ацетилхолин . Картину ЭКГ можно также увидеть после чрезмерного употребления алкоголя или кокаина .
Генетика
Синдром Бругада наследуется по аутосомно-доминантному типу, а это означает, что для возникновения синдрома необходима только одна копия дефектного гена. Однако человек, у которого диагностировано это заболевание, может быть первым в своей семье, у кого синдром Бругада возник, если он возник как новая мутация. Ген, мутации в котором чаще всего встречаются при синдроме Бругада, известный как SCN5A , отвечает за натриевый канал сердца. Мутации в SCN5A, связанные с синдромом Бругада, обычно вызывают уменьшение потока ионов натрия. Однако только 20% случаев синдрома Бругада связаны с мутациями в SCN5A, так как у большинства пациентов с синдромом Бругада генетическое тестирование не может определить генетическую мутацию, ответственную за это. На сегодняшний день обнаружено более 290 мутаций в гене SCN5A, каждая из которых изменяет функцию натриевых каналов по-разному. Этот вариант частично объясняет различия в тяжести состояния между разными людьми, начиная от очень опасного состояния, вызывающего смерть в молодом возрасте, до доброкачественного состояния, которое может вообще не вызывать никаких проблем. Однако генетика синдрома Бругада сложна, и вполне вероятно, что это состояние является результатом взаимодействия многих генов. Из-за этих сложных взаимодействий некоторые члены семьи, несущие конкретную мутацию, могут демонстрировать признаки синдрома Бругада, в то время как другие, несущие ту же мутацию, могут не иметь, что называется переменной пенетрантностью . Мутации в гене SCN5A, по-видимому, имеют прогностическое значение.
Было идентифицировано несколько других генов, связанных с синдромом Бругада. Некоторые из них отвечают за другие белки, которые образуют часть натриевого канала, известные как β-субъединицы натриевого канала ( SCN1B , SCN2B , SCN3B ), в то время как другие образуют различные типы натриевых каналов ( SCN10A ). Некоторые гены кодируют ионные каналы , которые перенос кальция или калия ионы ( CACNA1C , CACNB2 , KCND3 , KCNE3 , KCNJ8 ), в то время как другие генерируют белки , которые взаимодействуют с ионными каналами. ( GPD1L , PKP2 , MOG1, FGF12 ). Другой ген, связанный с этим состоянием, - RRAD . Гены, связанные с синдромом Бругада, и их описание включают:
| Тип | OMIM | Ген | Примечания |
|---|---|---|---|
| BrS1 | 601144 | SCN5A | Na V 1.5 - α-субъединица сердечного натриевого канала, несущая натриевой ток I Na . |
| BrS2 | 611778 | GPD1L | Глицерин-3-фосфатдегидрогеназа, подобная пептиду - снижение активности GPD1-L приводит к фосфорилированию Na V 1,5 и снижению I Na . |
| BrS3 | 114205 | CACNA1C | Ca V 1.2 - α субъединица потенциал-зависимого кальциевого канала, несущего кальциевый ток L-типа I Ca (L) . |
| BrS4 | 600003 | CACNB2 | Ca V β2B - субъединица β-2 потенциалзависимого кальциевого канала, несущая кальциевый ток L-типа I Ca (L) . |
| BrS5 | 600235 | SCN1B | Na V β1 - субъединица β-1 натриевого канала, несущего натриевый ток I Na . |
| BrS6 | 604433 | KCNE3 | MiRP2 - β-субъединица потенциалзависимых калиевых каналов. Модулирует переходной исходящий калиевый ток I к . |
| BrS7 | 608214 | SCN3B | Na V β3 - β-3 субъединица сердечного натриевого канала, несущая натриевой ток I Na . |
| BrS8 | 600935 | KCNJ8 | Kir6.1, несет входящий в выпрямитель калиевый ток I Kir . |
| BrS9 | 114204 | CACNA2D1 | субъединица α2δ потенциалзависимого кальциевого канала, несущая кальциевый ток L-типа I Ca (L) . |
| BrS10 | 605411 | KCND3 | K V 4.3, α-субъединица переходного выходящего калиевого канала I к . |
| BrS11 | 607954 | РАНГРФ | Кодирует MOG1 - влияет на трафик Na V 1.5. |
| BrS12 | 602701 | SLMAP | Связанный с сарколеммой мембраной белок, компонент Т-канальцев и саркоплазматического ретикулума, влияет на транспортировку Na V 1.5. |
| BrS13 | 601439 | ABCC9 | SUR2A, аденозинтрифосфат (АТФ) -связывающий кассетный транспортер канала I K (АТФ) . |
| BrS14 | 601327 | SCN2B | Na V β2 - субъединица бета-2 сердечного натриевого канала, несущего натриевый ток I Na . |
| BrS15 | 602861 | ПКП2 | Плакофиллин-2 - взаимодействует с I Na . |
| BrS16 | 601513 | FGF12 | Мутация гомологичного фактора-1 фактора роста фибробластов снижает I Na . |
| BrS17 | 604427 | SCN10A | Na V 1.8 - α-субъединица нейронального натриевого канала. |
| BrS18 | 604674 | ЭЙ2 | Фактор транскрипции идентифицирован в исследовании ассоциации всего генома . |
| BrS19 | 603961 | SEMA3A | Семафорин. |
| BrS20 | 601142 | KCNAB2 | K V β2, субъединица β2 потенциал-зависимого калиевого канала - мутация увеличивает I до . |
Некоторые мутации, связанные с синдромом Бругада, также могут вызывать другие сердечные заболевания. Те, у кого одновременно наблюдается более одного сердечного заболевания, вызванного одной мутацией, описываются как имеющие « синдром перекрытия ». Примером синдрома перекрытия является синдром Бругада и синдром удлиненного интервала QT (LQT3), вызванный мутацией в SCN5A, которая снижает пиковый ток натрия, но одновременно оставляет постоянную утечку тока. Синдром Бругада был описан как наложение с аритмогенной кардиомиопатией правого желудочка (ARVC), вызванной мутацией в гене PKP2, вызывающей картину ЭКГ Бругада, но структурные изменения в сердце, характерные для ARVC.
Механизмы
Аномальные сердечные ритмы, наблюдаемые у людей с синдромом Бругада, обычно представляют собой опасные аритмии, такие как фибрилляция желудочков или полиморфная желудочковая тахикардия, но у пациентов с BrS также более вероятно учащение сердечных сокращений из-за менее опасных аритмий, таких как тахикардия с повторным входом AV-узла и аномально замедленные сердечные ритмы, такие как дисфункция синусового узла . Есть несколько механизмов, с помощью которых генетические мутации, вызывающие это состояние, могут вызывать эти аритмии.
Некоторые утверждают, что основная причина возникновения этих аритмий связана с аномально медленной электропроводностью в областях сердца, особенно в правом желудочке . Генетические варианты, связанные с BrS, подтверждают концепцию SCN5A, гена, наиболее часто связанного с этим заболеванием, наряду с SCN10A, SCN1B, SCN2B и SCN3B, все они напрямую влияют на натриевый ток I Na . Натриевый ток вносит основной вклад в характерный поток электрического заряда через мембрану клеток сердечной мышцы, который происходит с каждым ударом сердца, известный как потенциал действия . I Na вызывает начальный быстрый подъем потенциала действия (фаза 0), а уменьшение раннего пика тока, как это происходит в генетических вариантах, связанных с BrS, приводит к замедлению электропроводности через сердечную мышцу. Эта медленная проводимость позволяет образовываться «коротким замыканиям», блокируя волны электрической активности в одних областях, позволяя волнам проходить в других в явлении, известном как разрушение волн. При правильных обстоятельствах это прерывание волны может позволить волнам электричества совершить разворот в мышце, перемещаясь в обратном направлении, прежде чем начать быстро кружить вокруг точки, называемой повторным входом, и вызывая аномальный сердечный ритм. . Те, кто поддерживает эту точку зрения (известную как гипотеза деполяризации), утверждают, что замедление проводимости может объяснить, почему аритмии у людей с синдромом Бругада, как правило, возникают в среднем возрасте, когда другие факторы, такие как рубцы или фиброз, сопровождающие старость, усугубляют тенденцию к проводимости. замедление вызвано генетической мутацией.
Другие предполагают, что основной причиной аритмий является разница в электрических свойствах сердца внутри ( эндокард ) и снаружи ( эпикард ) (известная как гипотеза реполяризации). Форма потенциала действия в эпикарде и эндокарде различается. Потенциал действия в клетках эпикарда показывает заметную выемку после начального всплеска из-за переходного внутреннего тока. Эта выемка гораздо менее очевидна в клетках эндокарда, а разница между эндокардом и эпикардием наиболее отчетливо видна в правом желудочке. У пациентов с синдромом Бругада эти различия увеличиваются, создавая короткий период в каждом сердечном цикле, когда ток течет от эндокарда к эпикарду, создавая характерную картину ЭКГ. Различия в электрических свойствах эпи и эндокарда описываются как «трансмуральная дисперсия реполяризации», которая, если она достаточно велика, может привести к блокировке электрических импульсов в одних регионах, но не в других. Опять же, этот разрыв волны может пропускать волны электричества. которые обычно движутся только в одном направлении, чтобы вместо этого начать кружить вокруг точки как возвращающийся контур, вызывая аритмию.
Еще одним фактором, способствующим возникновению аритмий при синдроме Бругада, являются изменения структуры сердца. В то время как сердце людей с синдромом Бругада может выглядеть нормально, рубцы или фиброз часто наблюдаются в определенных областях сердца, особенно в выводном тракте правого желудочка. Поскольку синдром Бругада может быть вызван мутацией во многих различных генах, возможно, что разные механизмы могут быть ответственны за аритмию, наблюдаемую у разных пациентов.
Диагностика
Электрокардиография

Синдром Бругада диагностируется путем выявления характерных паттернов на электрокардиограмме . Паттерн, наблюдаемый на ЭКГ, включает подъем сегмента ST в отведениях V 1 -V 3 с появлением блокады правой ножки пучка Гиса (БПНПГ). Могут быть свидетельства замедления электропроводности в сердце, о чем свидетельствует увеличенный интервал PR . Эти закономерности могут присутствовать постоянно, но могут проявляться только в ответ на определенные лекарства (см. Ниже), когда у человека поднимается температура , во время физических упражнений или в результате других триггеров. Картина ЭКГ может стать более очевидной при выполнении ЭКГ, в которой некоторые из электродов расположены в положениях, отличных от обычных, в частности, путем размещения отведений V 1 и V 2 выше грудной стенки в 1-м или 2-м межреберных промежутках.
Исторически были описаны три формы паттерна ЭКГ Бругада, хотя паттерн типа 3 больше не используется в современной практике.
- Тип 1 имеет Coved типа ST с высотой по крайней мере , 2 мм (0,2 мВ) J-точка высоты и постепенно нисходящий сегментом ST с последующим отрицательным Т-волной .
- Тип 2 имеет седлообразную форму с подъемом точки J не менее 2 мм и подъемом терминального сегмента ST не менее 0,5 мм с положительным или двухфазным зубцом T. Паттерн типа 2 иногда можно увидеть у здоровых людей.
- Тип 3 имеет модель «седло назад» (как тип 2) с возвышением точки J не менее 2 мм, но менее 1 мм возвышением конечного сегмента ST. Паттерн типа 3 относительно распространен у здоровых людей и больше не считается признаком синдрома Бругада.
Согласно текущим рекомендациям, только ЭКГ типа 1, возникающая спонтанно или в ответ на лечение, может использоваться для подтверждения диагноза синдрома Бругада, поскольку модели типов 2 и 3 нередко наблюдаются у людей, не страдающих этим заболеванием.
Провокационное тестирование
Некоторые лекарства, особенно антиаритмические препараты, которые блокируют ток натрия в сердце I Na, могут выявить паттерн Бругада 1 типа у восприимчивых людей. Эти препараты можно использовать для постановки диагноза тем, у кого есть подозрение на синдром Бругада (например, выжившие после необъяснимой остановки сердца, члены семьи человека с синдромом Бругада), но у которых не было обнаружено диагностической картины ЭКГ. В этих случаях препараты, блокирующие ток натрия, можно вводить в контролируемой среде. Наиболее часто используемые препараты для этой цели - это аджмалин , флекаинид и прокаинамид , причем некоторые предположения указывают на то, что аджмалин может быть наиболее эффективным. При приеме этих лекарств следует соблюдать осторожность, поскольку существует небольшой риск нарушения сердечного ритма.
Генетическое тестирование
Генетическое тестирование может быть полезно для выявления пациентов с синдромом Бругада, чаще всего у членов семьи человека с синдромом Бругада, но иногда проводится у человека, который умер внезапно и неожиданно. Однако интерпретация результатов генетического тестирования является сложной задачей. У членов семьи, которые все являются носителями определенного генетического варианта, связанного с синдромом Бругада, некоторые члены семьи могут демонстрировать признаки синдрома Бругада на своих ЭКГ, а другие - нет. Это означает, что наличие генетической мутации, связанной с синдромом Бругада, не обязательно означает, что человек действительно страдает этим заболеванием. Еще больше усложняет ситуацию то, что многие часто встречающиеся вариации гена SCN5A не вызывают каких-либо проблем, и поэтому у людей с синдромом Бругада иногда идентифицируются генетические варианты, которые на самом деле не вызывают заболевание.
Другие расследования
Инвазивные электрофизиологические исследования , при которых провода пропускаются через вену для стимуляции и записи электрических сигналов от сердца, иногда можно использовать для оценки риска того, что у человека с синдромом Бругада возникнут опасные нарушения сердечного ритма. Стратификация риска также иногда выполняется с использованием ЭКГ с усредненным сигналом . Амбулаторный мониторинг ЭКГ , включая имплантацию петлевого регистратора , иногда используется для оценки того, вызваны ли головокружение или обмороки у человека с синдромом Бругада ненормальным сердечным ритмом или другими причинами, такими как вазовагальный обморок.
Уход
Основная цель лечения людей с синдромом Бругада - снизить риск внезапной смерти из-за серьезных нарушений сердечного ритма, таких как фибрилляция желудочков или полиморфная желудочковая тахикардия. В то время как некоторые с этим заболеванием подвержены высокому риску серьезных нарушений сердечного ритма, другие подвержены гораздо меньшему риску, а это означает, что некоторым может потребоваться более интенсивное лечение, чем другим. В дополнение к лечению человека с синдромом Бругада часто важно обследовать ближайших родственников, чтобы увидеть, не переносят ли они это заболевание.
образ жизни
Первая линия лечения, подходящая для всех людей с синдромом Бругада, независимо от их риска аритмий, - это советы по образу жизни. Людям следует рекомендовать распознавать и избегать вещей, которые могут увеличить риск серьезных аритмий. К ним относятся отказ от чрезмерного употребления алкоголя, отказ от некоторых лекарств и быстрое лечение лихорадки парацетамолом . Хотя аномальные сердечные ритмы, наблюдаемые при синдроме Бругада, как правило, чаще возникают в состоянии покоя или даже во время сна, некоторые люди с синдромом Бругада испытывают аритмию во время физических упражнений. Поэтому некоторые врачи могут посоветовать людям с синдромом Бругада, что, хотя легкие упражнения полезны, следует избегать очень напряженных упражнений.
Имплантируемый дефибриллятор
Людям с повышенным риском внезапной сердечной смерти можно рекомендовать имплантируемый кардиовертер-дефибриллятор (ИКД). Эти небольшие устройства, имплантированные под кожу, постоянно контролируют сердечный ритм. Если устройство обнаруживает потенциально опасную для жизни аритмию, оно может поразить сердце небольшим электрическим током, вернув сердце в нормальный ритм. ИКД также может функционировать как кардиостимулятор , предотвращая аномально низкую частоту сердечных сокращений, которая также может возникать у людей с синдромом Бругада.
Имплантация ИКД - процедура с относительно низким уровнем риска и часто выполняется в дневном режиме под местной анестезией . Однако могут возникнуть такие осложнения, как инфекция, кровотечение или ненужные разряды, которые иногда могут быть серьезными. Из-за небольшого риска, связанного с имплантацией ИКД, а также из-за стоимости устройств ИКД не рекомендуются для всех людей с синдромом Бругада, а вместо этого предназначены для людей, которые считаются подверженными более высокому риску внезапной сердечной смерти.
Медикамент
Хинидин - это антиаритмический препарат, который может снизить вероятность серьезных нарушений сердечного ритма, возникающих у некоторых людей с синдромом Бругада. Он наиболее часто используется у людей с синдромом Бругада, у которых есть ИКД и которые испытали несколько эпизодов угрожающих жизни аритмий, но также может использоваться у людей с высоким риском аритмий, но которым ИКД не подходит.
Изопреналин , препарат, имеющий сходство с адреналином , может быть использован в экстренных случаях для людей с синдромом Бругада, у которых часто возникают повторяющиеся опасные для жизни аритмии, известные как «электрическая буря». Этот препарат следует вводить в вену непрерывно, поэтому он не подходит для длительного применения.
Катетерная абляция
Еще одним вариантом лечения людей с синдромом Бругада является радиочастотная катетерная абляция . В этой процедуре провода проходят через вену на ноге в сердце или через небольшое отверстие под грудиной . Эти провода используются для поиска области сердца, ответственной за возникновение аритмий. Кончик одного из этих проводов используется, чтобы нанести серию крошечных ожогов, намеренно повреждая область аномальной сердечной мышцы, которая является причиной проблемы. Текущие рекомендации предполагают, что это лечение следует зарезервировать для людей с синдромом Бругада, которые неоднократно подвергались электрошоку от ИКД.
Эпидемиология
От 1 до 30 из 10 000 человек страдают синдромом Бругада. Хотя больные рождаются с этим заболеванием, симптомы обычно появляются только в зрелом возрасте. В то время как редкие случаи, наблюдаемые в детстве, с равной вероятностью могут быть как у мужчин, так и у женщин, во взрослом возрасте симптомы чаще возникают у мужчин, чем у женщин, возможно, из-за более высокого уровня тестостерона у мужчин.
Синдром Бругада чаще встречается у людей азиатского происхождения и является наиболее частой причиной внезапной смерти молодых мужчин без известных сердечных заболеваний в Таиланде и Лаосе . В этих странах синдром Бругада может быть причиной многих случаев синдрома внезапной неожиданной ночной смерти (SUNDS). Местные названия меняются - на Филиппинах это состояние было известно как Бангунгут, что означает «крик с последующей внезапной смертью во сне», в Таиланде оно было известно как Лай Тай , а в Японии - Поккури . Паттерны ЭКГ Бругада 1 типа чаще встречаются в азиатских популяциях (0–0,36%), чем в Европе (0–0,25%) и США (0,03%). Аналогичным образом, ЭКГ типов 2 и 3 более распространены в Азии (0,12–2,23%), чем в Европе (0,0–0,6%) или США (0,02%).
История
Синдром Бругада назван в честь испанских кардиологов Хосепа и Педро Бругада, описавших это состояние в 1992 году, хотя в 1989 году сообщалось о связи между характерным ЭКГ-паттерном и внезапной сердечной смертью. Синдром Бругада был описан как причина внезапной необъяснимой сердечной смерти. синдром, наблюдаемый у тайских мужчин в 1997 году. Первые генетические мутации, затрагивающие ген SCN5A, связанный с этим синдромом, были идентифицированы их братом Рамоном Бругада в 1998 году, и многие другие мутации затронули по крайней мере 19 генов, впоследствии идентифицированных другими. Исследования 2000-х годов привели к появлению конкурирующих теорий о механизмах возникновения аномальных сердечных ритмов. Исследования синдрома Бругада продолжаются, выявляются новые генетические варианты, изучаются механизмы аритмий и ведутся поиски лучших методов лечения.
Общество и культура
- В эпизоде телесериала 1992 года « Неразгаданные тайны» рассказывается о гуаманской семье Сантос, которая потеряла нескольких членов из-за проблем с сердцем. У выживших членов семьи в конечном итоге был диагностирован синдром Бругада.
- В британской мыльной опере EastEnders была показана сюжетная линия, в которой один из персонажей перенес остановку сердца из-за синдрома Бругада.
- В 8-й серии 8-го сезона ситкома «Скрабс» («Влюбленный мой адвокат») Перри Кокс задает последний вопрос стажеру Эду, на который тот не может ответить. Впоследствии он был уволен. Один правильный ответ на его вопрос - синдром Бругада, хотя синдром удлиненного интервала QT также был бы приемлемым ответом.
Смотрите также
использованная литература
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |
-
 СМИ, связанные с синдромом Бругада на Викискладе?
СМИ, связанные с синдромом Бругада на Викискладе? - BrugadaDrugs.org , содержит список лекарств, которых следует избегать людям с синдромом Бругада.
- GeneReviews: синдром Бругада




