Кабазитаксел - Cabazitaxel
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Евтана |
| Другие имена | XRP-6258 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a611009 |
| Данные лицензии | |
Категория беременности |
|
| Пути администрирования |
Внутривенно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard |
100.205.741 |
| Химические и физические данные | |
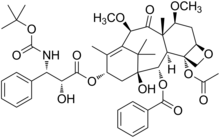
| Формула | C 45 H 57 N O 14 |
| Молярная масса | 835,944 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
|
| |
Кабазитаксел , продаваемый под торговой маркой Jevtana , представляет собой полусинтетическое производное природного таксоида . Он был разработан Санофи-Авентис и был одобрен FDA США для лечения гормонорезистентного рака простаты 17 июня 2010 года. Это ингибитор микротрубочек и четвертый таксан, одобренный для лечения рака .
Кабазитаксел в комбинации с преднизоном является вариантом лечения гормонорезистентного рака простаты после лечения на основе доцетаксела .
Механизм действия
Таксаны усиливают стабилизацию микротрубочек и ингибируют митоз и деление клеток. Более того, таксаны предотвращают передачу сигналов рецептора андрогена (AR) путем связывания клеточных микротрубочек и ассоциированного с микротрубочками моторного белка динеина, тем самым предотвращая ядерную транслокацию AR.
Клинические испытания
У пациентов с метастатическим устойчивым к кастрации раком простаты (mCRPC) общая выживаемость (OS) заметно увеличивается при применении кабазитаксела по сравнению с митоксантроном после предшествующего лечения доцетакселом. FIRSTANA (идентификатор ClinicalTrials.gov: NCT01308567) оценила, превосходит ли кабазитаксел 20 мг / м 2 (C20) или 25 мг / м 2 (C25) доцетаксел 75 мг / м 2 (D75) с точки зрения общей выживаемости у пациентов, получавших химиотерапию: наивный mCRPC. Однако C20 и C25 не продемонстрировали превосходства в отношении ОС по сравнению с D75 у пациентов с не получавшим химиотерапию мКРРПЖ. Кабазитаксел и доцетаксел продемонстрировали разные профили токсичности, а C20 показал самую низкую в целом токсичность. В исследовании III фазы с участием 755 мужчин для лечения резистентного к кастрации рака простаты средняя выживаемость составила 15,1 месяца для пациентов, получавших кабазитаксел, по сравнению с 12,7 месяца для пациентов, получавших митоксантрон . Кабазитаксел был связан с большей частотой нейтропении 3-4 степени (81,7%), чем митоксантрон (58%). Общие побочные эффекты кабазитаксела включают нейтропению (включая фебрильную нейтропению) и побочные эффекты со стороны ЖКТ, проявляющиеся в основном в виде диареи, тогда как невропатия выявлялась редко.
Фармакокинетика
Введение кабазитаксела вызывает снижение концентраций в плазме, демонстрируя трехфазную кинетику: средний период полувыведения (t 1/2 ) 2,6 мин в первой фазе, средний t 1/2 1,3 ч во второй фазе и средний t 1 / 2 из 77,3 ч в третьей фазе.
Метаболизм
Кабазитаксел в основном метаболизируется в печени с помощью [цитохрома P 450 (CYP) 3A4 / 5> CYP2C8], в результате чего образуется семь метаболитов в плазме и выводится 20 метаболитов. В течение 14 дней после приема кабазитаксел выводится на 80%: 76% - с калом и 3,7% - через почки.
Дозирование кабазитаксела
Существует много вопросов об оптимальном использовании кабазитаксела после одобрения его использования для лечения мКРРПЖ, резистентного к доцетакселу. Один вопрос - об оптимальном использовании. Что касается значительной миелосупрессии при введении кабазитаксела в дозе 25 мг / м 2 , рандомизированное исследование III фазы оценит безопасность и эффективность кабазитаксела в дозе 20 мг / м 2 . Еще один вопрос касается эффективности и переносимости кабазитаксела при его применении с другими препаратами. Испытания фазы I / II проверяют совместное применение кабазитаксела с другими препаратами (например, абиратероном ) и исследуемыми агентами (например, кустирсеном ).
Смотрите также
Рекомендации
внешняя ссылка
- «Кабазитаксел» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Кабазитаксел Аккорд 20 мг / мл концентрат для инфузии раствора: риск ошибочного приема лекарств и путаницы с настоем растворителя Jevtana (60 мг / 1,5 мл)» . Европейское агентство по лекарственным средствам (EMA) . 28 октября 2020.
