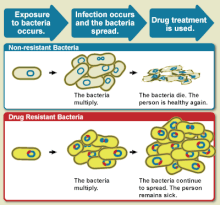
Устойчивость к лекарству - Drug resistance
Устойчивость к лекарствам - это снижение эффективности лекарств, таких как противомикробные или противоопухолевые, при лечении заболевания или состояния. Этот термин используется в контексте резистентности, которую «приобрели» патогены или рак, то есть резистентность развилась. Устойчивость к противомикробным препаратам и противоопухолевое сопротивление задача клинической помощи и исследования привода. Когда организм устойчив к нескольким лекарственным средствам, он считается устойчивым ко многим лекарствам .
Развитие устойчивости к антибиотикам, в частности, происходит из-за лекарств, нацеленных только на определенные бактериальные молекулы (почти всегда на белки). Поскольку препарат настолько специфичен, любая мутация в этих молекулах будет мешать или сводить на нет его деструктивный эффект, что приводит к устойчивости к антибиотикам. Кроме того, растет озабоченность по поводу злоупотребления антибиотиками в животноводстве, на долю которого только в Европейском Союзе приходится в три раза больше, чем у людей, что ведет к развитию сверхустойчивых бактерий.
Бактерии способны не только изменять фермент, на который нацелены антибиотики, но и использовать ферменты для модификации самого антибиотика и, таким образом, его нейтрализации. Примерами патогенов, изменяющих цель, являются Staphylococcus aureus , устойчивые к ванкомицину энтерококки и устойчивые к макролидам стрептококки , а примерами микробов, изменяющих антибиотики, являются Pseudomonas aeruginosa и устойчивые к аминогликозидам Acinetobacter baumannii .
Короче говоря, отсутствие согласованных усилий со стороны правительств и фармацевтической промышленности вместе с врожденной способностью микробов развивать резистентность со скоростью, опережающей разработку новых лекарств, предполагает, что существующие стратегии разработки жизнеспособных, долгосрочных антимикробных препаратов в конечном итоге обречены на провал. Без альтернативных стратегий приобретение лекарственной устойчивости патогенными микроорганизмами становится, возможно, одной из самых серьезных угроз общественному здоровью, с которыми сталкивается человечество в 21 веке. Одними из лучших альтернативных источников, снижающих вероятность устойчивости к антибиотикам, являются пробиотики, пребиотики, пищевые волокна, ферменты, органические кислоты, фитогенные вещества.
Типы
Устойчивость к лекарствам, токсинам или химическим веществам является следствием эволюции и является ответом на давление, оказываемое на любой живой организм. Индивидуальные организмы различаются по своей чувствительности к используемому лекарству, и некоторые из них, обладающие большей приспособленностью, могут выжить при лечении лекарствами. Соответственно, признаки лекарственной устойчивости наследуются последующим потомством, в результате чего популяция становится более устойчивой к лекарствам. Если применяемый препарат не делает невозможным половое размножение, деление клеток или горизонтальный перенос генов во всей целевой популяции, неизбежно последует резистентность к препарату. Это можно увидеть в раковых опухолях, где у некоторых клеток может развиться устойчивость к лекарствам, используемым в химиотерапии . Химиотерапия заставляет фибробласты вблизи опухолей производить большое количество белка WNT16B . Этот белок стимулирует рост раковых клеток, устойчивых к лекарствам. Было также показано, что микроРНК влияют на приобретенную лекарственную устойчивость раковых клеток, и это может быть использовано в терапевтических целях. В 2012 году малярия вновь стала угрозой в Юго-Восточной Азии и странах Африки к югу от Сахары , а устойчивые к лекарствам штаммы Plasmodium falciparum создают огромные проблемы для органов здравоохранения. Проказа показывает возрастающую устойчивость к дапсону .
Между одноклеточными организмами существует быстрый процесс обмена резистентностью , который называется горизонтальным переносом генов, при котором происходит прямой обмен генами, особенно в состоянии биопленки . Похожий бесполый метод используют грибы и называют « парасексуальностью ». Примеры устойчивых к лекарственным средствам штаммов можно найти у микроорганизмов, таких как бактерии и вирусы, паразитов как эндо-, так и экто- , растений, грибов, членистоногих , млекопитающих, птиц, рептилий, рыб и земноводных.
В домашних условиях устойчивые к лекарствам штаммы организмов могут возникать в результате, казалось бы, безопасных действий, таких как использование отбеливателя , чистка зубов и полоскание рта, использование антибиотиков, дезинфицирующих и моющих средств, шампуней и мыла, особенно антибактериального мыла, мыла для рук. мытье, спреи для поверхностей, нанесение дезодорантов , кремов для загара и любых косметических или медицинских продуктов, инсектицидов и соусов. Химические вещества, содержащиеся в этих препаратах, помимо вреда для полезных организмов, могут преднамеренно или непреднамеренно нацеливаться на организмы, у которых может развиться резистентность.
Механизмы
Четыре основных механизма устойчивости микроорганизмов к противомикробным препаратам:
- Инактивация или модификация лекарственного средства: например, ферментативная дезактивация пенициллина G у некоторых устойчивых к пенициллину бактерий посредством продукции β-лактамаз .
- Изменение сайта-мишени: например, изменение PBP - сайта-мишени связывания пенициллинов - у MRSA и других устойчивых к пенициллину бактерий.
- Нарушение метаболического пути: например, некоторым бактериям, устойчивым к сульфонамидам , не требуется парааминобензойная кислота (ПАБК), важный предшественник для синтеза фолиевой кислоты и нуклеиновых кислот в бактериях, ингибируемых сульфонамидами. Вместо этого они, как и клетки млекопитающих, используют предварительно образованную фолиевую кислоту.
- Уменьшение накопления лекарства: за счет уменьшения проницаемости лекарства и / или увеличения активного оттока (откачки) лекарства через поверхность клетки.
Механизмы приобретенной лекарственной устойчивости:
| Механизм | Противомикробный агент | Действие препарата | Механизм сопротивления |
|---|---|---|---|
| Уничтожить наркотик | Аминогликозид
Бета-лактамные антибиотики (пенициллин и цефалоспорин) Хлорамфеникол
|
Связывается с 30S субъединицей рибосомы, подавляя синтез белка.
Связывается с пенициллин-связывающими белками, подавляя синтез пептидогликана. Связывается с 50S субъединицей рибосомы, подавляя образование пептидных связей. |
Плазмида кодирует ферменты, которые химически изменяют лекарство (например, путем ацетилирования или фосфорилирования), тем самым инактивируя его.
Плазмида кодирует бета-лактамазы, которые открывают бета-лактамное кольцо, инактивируя его. Плазмида кодирует фермент, который ацетилирует лекарство, тем самым инактивируя его. |
| Изменяет мишень для лекарства | Аминогликозиды
Бета-лактамные антибиотики (пенициллин и цефалоспорин) Эритромицин Хинолоны Рифампицин Триметоприм |
Связывается с 30S субъединицей рибосомы, подавляя синтез белка.
Связывается с пенициллин-связывающими белками, подавляя синтез пептидогликана. Связывается с 50S субъединицей рибосомы, подавляя синтез белка. Связывается с ДНК-топоизомеразой, ферментом, необходимым для синтеза ДНК. Связывается с РНК-полимеразой; подавление инициации синтеза РНК Подавляет фермент дигидрофолат снижает, блокируя путь фолиевой кислоты |
Бактерии создают измененные рибосомы 30S, которые не связываются с лекарством.
Бактерии производят измененные связывающие пенициллин белки, которые не связываются с лекарством. Бактерии образуют форму 50S рибосомы, которая не связывается с лекарством. Бактерии производят измененную ДНК-топоизомеразу, которая не связывается с лекарством. Бактерии вырабатывают измененную полимеразу, которая не связывается с лекарством. Бактерии вырабатывают измененный фермент, который не связывается с лекарством. |
| Подавляет поступление лекарства или удаляет лекарство | Пенициллин
Эритромицин Тетрациклин |
Связывается с пенициллин-связывающими белками, подавляя синтез пептидогликана.
Связывается с 50S субъединицей рибосомы, подавляя синтез белка. Связывается с субъединицей 30S рибосомы, подавляя синтез белка, блокируя тРНК. |
Бактерии изменяют форму пориновых белков внешней мембраны, предотвращая попадание лекарства в клетку.
Новая мембранная транспортная система предотвращает попадание лекарства в клетку. Новая мембранная транспортная система выкачивает лекарство из клетки. |
Метаболическая стоимость
Биологические затраты - это мера увеличения энергетического метаболизма, необходимого для достижения функции.
Устойчивость к лекарствам имеет высокую метаболическую цену у патогенов, для которых актуальна эта концепция (бактерии, эндопаразиты и опухолевые клетки). Для вирусов эквивалентной «стоимостью» является геномная сложность. Высокая метаболическая стоимость означает, что в отсутствие антибиотиков устойчивый патоген будет иметь более низкую эволюционную пригодность по сравнению с чувствительными патогенами. Это одна из причин, по которой адаптации к лекарственной устойчивости редко наблюдаются в условиях отсутствия антибиотиков. Однако в присутствии антибиотиков преимущество в выживаемости компенсирует высокие метаболические затраты и позволяет устойчивым штаммам размножаться.
Уход
У человека ген ABCB1 кодирует MDR1 (p-гликопротеин), который является ключевым переносчиком лекарств на клеточном уровне. Если MDR1 сверхэкспрессируется, устойчивость к лекарствам возрастает. Следовательно, можно контролировать уровни ABCB1. У пациентов с высоким уровнем экспрессии ABCB1 вторичные методы лечения, такие как метформин, с некоторым успехом применялись в сочетании с первичным медикаментозным лечением.
Для лечения устойчивости к антибиотикам , которая представляет собой широко распространенную проблему в настоящее время, используются препараты, предназначенные для блокирования механизмов устойчивости бактерий к антибиотикам. Например, устойчивость бактерий к бета-лактамным антибиотикам (таким как пенициллин и цефалоспорины ) можно обойти, используя антибиотики, такие как нафциллин , которые не подвержены разрушению определенными бета-лактамазами (группа ферментов, ответственных за расщепление бета-лактамов). . С резистентностью к бета-лактамным бактериям также можно бороться, назначая бета-лактамные антибиотики с лекарствами, которые блокируют бета-лактамазы, такие как клавулановая кислота, так что антибиотики могут работать, не разрушаясь в первую очередь бактериями. Недавно исследователи осознали потребность в новых лекарствах, которые подавляют насосы оттока бактерий , которые вызывают устойчивость к нескольким антибиотикам, таким как бета-лактамы , хинолоны , хлорамфеникол и триметоприм, путем отправки молекул этих антибиотиков из бактериальной клетки. Иногда комбинация антибиотиков разных классов может использоваться синергетически; то есть они работают вместе, чтобы эффективно бороться с бактериями, которые могут быть устойчивы только к одному из антибиотиков.
Уничтожение устойчивых бактерий также может быть достигнуто с помощью фаговой терапии , в которой используется специфический бактериофаг (вирус, убивающий бактерии).
Смотрите также
- Устойчивость к антибиотикам
- Фекальная бактериотерапия
- Массовое введение лекарств
- Множественная лекарственная устойчивость
- Фармакоэпидемиология
- Физические факторы, влияющие на микробную жизнь
- Малый белок множественной лекарственной устойчивости
- Элефтерия терра
использованная литература
внешние ссылки
- BURDEN of Resistance and Disease in European Nations - проект ЕС по оценке финансового бремени устойчивости к антибиотикам в европейских больницах
- Мерк - Терпимость и сопротивление
- База данных косметики
- Инструмент для мутаций лекарственной устойчивости HCMV
- Борьба с лекарственной устойчивостью - информативная статья о множественной лекарственной устойчивости
- Битва за ошибки: борьба с устойчивостью к антибиотикам
- MDRIpred : веб-сервер для прогнозирования ингибиторов устойчивости к лекарственным препаратам M. Tuberculosis, опубликованный в Chemistry Central Journal.
- CancerDR : База данных по устойчивости к лекарствам от рака. Научные отчеты 3, 1445 г.