Эпихлоргидрин - Epichlorohydrin

|
|||
|
|||
| Имена | |||
|---|---|---|---|
|
Предпочтительное название IUPAC
2- (хлорметил) оксиран |
|||
| Другие имена
(Хлорметил) оксиран
Эпихлоргидрин 1-Хлор-2,3-эпоксипропан γ-Оксид хлорпропилена Глицидилхлорид |
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| 79785 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard |
100.003.128 |
||
| Номер ЕС | |||
| 164180 | |||
| КЕГГ | |||
|
PubChem CID
|
|||
| Номер RTECS | |||
| UNII | |||
| Номер ООН | 2023 г. | ||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| C 3 H 5 ClO | |||
| Молярная масса | 92,52 г / моль | ||
| Появление | бесцветная жидкость | ||
| Запах | чеснок или хлороформ -подобных | ||
| Плотность | 1,1812 г / см 3 | ||
| Температура плавления | -25,6 ° С (-14,1 ° F, 247,6 К) | ||
| Точка кипения | 117,9 ° С (244,2 ° F, 391,0 К) | ||
| 7% (20 ° С) | |||
| Давление газа | 13 мм рт. Ст. (20 ° C) | ||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| Пиктограммы GHS |
    
|
||
| Сигнальное слово GHS | Опасность | ||
| H226 , H301 , H311 , H314 , H317 , H331 , H350 | |||
| Р201 , Р202 , Р210 , Р233 , Р240 , Р241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P272 , P280 , P281 , P301 + 310 , P301 + 330 + 331 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P308 + 313 , P310 , P311 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 32 ° С (90 ° F, 305 К) | ||
| Пределы взрываемости | 3,8–21% | ||
| Смертельная доза или концентрация (LD, LC): | |||
|
ЛК 50 ( средняя концентрация )
|
3617 частей на миллион (крыса, 1 час) 2165 частей на миллион (крыса, 1 час) 250 частей на миллион (крыса, 8 часов) 244 частей на миллион (крыса, 8 часов) 360 частей на миллион (крыса, 6 часов) |
||
|
LC Lo ( самый низкий опубликованный )
|
250 частей на миллион (крыса, 4 часа) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
|
PEL (Допустимо)
|
TWA 5 частей на миллион (19 мг / м 3 ) [кожа] | ||
|
REL (рекомендуется)
|
Канцероген | ||
|
IDLH (Непосредственная опасность)
|
Ca [75 частей на миллион] | ||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
Эпихлоргидрин (сокращенно ECH ) представляет собой хлорорганическое соединение и эпоксид . Несмотря на название, это не галогидрин . Это бесцветная жидкость с резким запахом чеснока, умеренно растворимая в воде, но смешивающаяся с большинством полярных органических растворителей . Это хиральная молекула, обычно существующая в виде рацемической смеси правосторонних и левосторонних энантиомеров . Эпихлоргидрин представляет собой высокореактивное электрофильное соединение, которое используется в производстве глицерина , пластмасс, эпоксидных клеев и смол , эпоксидных разбавителей и эластомеров .
Производство
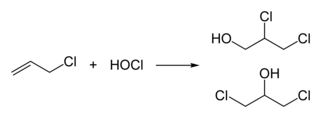
Эпихлоргидрин традиционно получают из аллилхлорида в два этапа, начиная с добавления хлорноватистой кислоты , которая дает смесь двух изомерных спиртов:
На втором этапе эту смесь обрабатывают основанием, чтобы получить эпоксид :
Таким образом ежегодно производится более 800 000 тонн (1997 г.) эпихлоргидрина.
Глицериновые маршруты
Эпихлоргидрин был впервые описан в 1848 году Марселлином Бертло . Соединение было выделено в ходе исследований реакций между глицерином и газообразным хлороводородом .
Напоминая эксперимент Бертло, растения, производящие глицерин-эпихлоргидрин (GTE), были коммерциализированы. Эта технология использует дешевый глицерин, получаемый при переработке биотоплива . В процессе, разработанном Dow Chemical , глицерин претерпевает две реакции замещения при обработке хлористым водородом в присутствии катализатора карбоновой кислоты . Это тот же промежуточный продукт, который образуется в процессе аллилхлорида / хлорноватистой кислоты, который затем аналогичным образом обрабатывается основанием с образованием эпихлоргидрина.
Другие маршруты
Способы использования меньшего количества хлорированных промежуточных продуктов продолжают вызывать интерес. Один из таких процессов включает эпоксидирование аллилхлорида.
Приложения
Синтез глицерина и эпоксидных смол
Эпихлоргидрин в основном превращается в диглицидиловый эфир бисфенола А , строительный блок при производстве эпоксидных смол . Он также является предшественником мономеров для других смол и полимеров. Другое использование - преобразование в синтетический глицерин . Однако быстрое увеличение производства биодизельного топлива , в котором глицерин является отходом, привело к избытку глицерина на рынке, что сделало этот процесс неэкономичным. Синтетический глицерин сейчас используется только в чувствительной фармацевтической и биотехнологической сферах, где стандарты качества очень высоки.
Второстепенные и нишевые приложения
Эпихлоргидрин является универсальным предшественником в синтезе многих органических соединений. Например, он превращается в глицидилнитрат , энергетическое связующее, используемое во взрывчатых и метательных композициях. Эпихлоргидрин реагирует с нитратом щелочного металла, таким как нитрат натрия , с образованием глицидилнитрата и хлорида щелочного металла. Он используется в качестве растворителя для целлюлозы , смол и красок, а также в качестве фумиганта от насекомых.
Полимеры, изготовленные из эпихлоргидрина, например полиамид-эпихлоргидриновые смолы, используются в армировании бумаги и в пищевой промышленности для производства чайных пакетиков, фильтров для кофе и оболочек для колбас / салями, а также для очистки воды .
Важное биохимическое применение эпихлоргидрина является его использованием в качестве сшивающего агента для производства Сефадекса гель-хроматографических смолы из декстраны .
Безопасность
Эпихлоргидрин классифицируется несколькими международными исследовательскими организациями и группами в области здравоохранения как вероятный или вероятный канцероген для человека. Длительное пероральное употребление высоких уровней эпихлоргидрина может привести к проблемам с желудком и повышенному риску рака. Воздействие эпихлоргидрина при вдыхании на рабочем месте может вызвать раздражение легких и повысить риск рака легких.
использованная литература
- Перейти ↑ Merck Index , 12-е издание, 3648 .
- ^ a b c d e f Карманное руководство NIOSH по химической опасности. «# 0254» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ a b «Эпихлоргидрин» . Немедленно опасная для жизни или здоровья концентрация (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ "Потребительский информационный бюллетень EPA" . Epa.gov . Проверено 2 декабря 2011 .
- ^ Браун, Г. (1936). «Эпихлоргидрин и эпибромогидрин». Органический синтез . 16 : 30. DOI : 10,15227 / orgsyn.016.0030 .
- ^ Guenter Sienel; Роберт Рит; Кеннет Т. Роуботтом. «Эпоксиды». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a09_531 .
- ^ Людгер Крэлинг; Юрген Крей; Джеральд Якобсон; Иоганн Гролиг; Леопольд Микше. «Аллильные соединения». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a01_425 .
- Перейти ↑ Berthelot, Marcellin (1854). "Sur les combinaisons de la glycérine avec les acides et sur la synthèse des Principes immédiats des graisses animaux" . Анна. Чим. Phys . Серия 3. 41 : 216–319. Архивировано из оригинала на 2015-04-02 . Проверено 2 марта 2015 .
- ^ Дорис де Гусман (2011-01-20). «Выращивание растений, превращающих глицерин в ЭХГ» . ICIS Green Chemicals.
- ^ Белл, Брюс М .; Бриггс, Джон Р .; Кэмпбелл, Роберт М .; Chambers, Susanne M .; Gaarenstroom, Phil D .; Хипплер, Джеффри Дж .; Крюк, Брюс Д .; Кирнс, Кеннет; и другие. (2008). «Глицерин как возобновляемое сырье для производства эпихлоргидрина. Процесс GTE» (PDF) . ЧИСТЫЙ - почва, воздух, вода . 36 (8): 657. DOI : 10.1002 / clen.200800067 . Архивировано из оригинала (полный текст перепечатки) на 2012-07-18 . Проверено 5 марта 2012 .
- ^ Июня Ли, Gongda Чжао Шуан Гао Ин Lv, Цзянь Ли и Zuwei Xi (2006). «Эпоксидирование аллилхлорида до эпихлоргидрина с помощью обратимого катализатора на носителе с H2O2 в условиях отсутствия растворителя». Орг. Процесс Res. Dev . 10 (5): 876–880. DOI : 10.1021 / op060108k .CS1 maint: использует параметр авторов ( ссылка )
- ^ Pham, Ha Q .; Маркс, Морис Дж. (2012). «Эпоксидные смолы». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a09_547.pub2 . ISBN 978-3527306732.
- ↑ Тейлор, Фил (16 октября 2008 г.). «Синтетический глицерин вернулся (но никогда не исчез)!» . Технолог In-Pharma . Проверено 29 ноября 2018 .
- Перейти ↑ Gould, RF Advanced Propellant Chemistry , ACS Chemistry Series 54, 1966
- ^ «Пригородные лаборатории тестирования воды: информационный бюллетень по эпихлоргидрину» . H2otest.com. Архивировано из оригинала на 2012-04-05 . Проверено 2 декабря 2011 .
- ^ "Правительство Канады Химические вещества: Оксиран, (хлорметил) - (эпихлоргидрин) Регистрационный номер CAS 106-89-8" . 13 февраля 2008 . Проверено 7 мая 2013 .
- ^ «GE Healthcare Life Sciences - инструкции для Sephadex Media» . .gelifesciences.com. Архивировано из оригинала на 2012-02-18 . Проверено 2 декабря 2011 .
- ^ «Интегрированная система информации о рисках EPA: эпихлоргидрин (CASRN 106-89-8)» . Проверено 7 мая 2013 .
- ^ «Правительство Канады: Оценка скрининга эпихлоргидрина» . Проверено 7 мая 2013 .
- ^ "Карманный справочник NIOSH по химической опасности - эпихлоргидрин" . Проверено 20 сентября 2013 .
- ^ «Основная информация об эпихлоргидрине в питьевой воде» . Проверено 7 мая 2013 .
- ^ «Правительство Канады: Оценка скрининга эпихлоргидрина» . Проверено 7 мая 2013 .