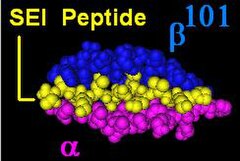
HLA-DR - HLA-DR
| MHC класс II , DR | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| (гетеродимер) | |||||||||||||||||||
|
Иллюстрация DR со связанным лигандом (желтый)
| |||||||||||||||||||
| Тип белка | рецептор клеточной поверхности | ||||||||||||||||||
| Функция | Распознавание иммунитета и презентация антигена |
||||||||||||||||||
| |||||||||||||||||||
HLA-DR представляет собой рецептор MHC класса II на клеточной поверхности, кодируемый антигенным комплексом лейкоцитов человека в области 6p21.31 хромосомы 6. Комплекс HLA-DR ( H Уманский L eukocyte A ntigen - DR изотипа) и пептида, как правило , от 9 до 30 аминокислот в длину, представляет собой лиганд для рецептора Т-клеток (TCR). HLA ( человеческие лейкоцитарные антигены ) первоначально были определены как антигены клеточной поверхности, которые опосредуют реакцию « трансплантат против хозяина» . Идентификация этих антигенов привела к большему успеху и долголетию трансплантации органов.
Антигенами, наиболее ответственными за потерю трансплантата, являются HLA-DR (первые шесть месяцев), HLA-B (первые два года) и HLA-A (длительная выживаемость). Хорошее соответствие этих антигенов между хозяином и донором является наиболее важным для достижения выживаемости трансплантата.
HLA-DR также участвует в нескольких аутоиммунных состояниях, восприимчивости к болезням и устойчивости к болезням. Он также тесно связан с HLA-DQ, и эта связь часто затрудняет устранение более причинного фактора заболевания.
Молекулы HLA-DR активируются в ответ на передачу сигналов. В случае инфекции пептид (такой как пептид стафилококкового энтеротоксина I) связывается с молекулой DR и представляется некоторым из очень многих Т-клеточных рецепторов, обнаруженных на Т-хелперных клетках. Затем эти клетки связываются с антигенами на поверхности В-клеток, стимулируя пролиферацию В-клеток.
Функция
Основная функция HLA-DR - представлять пептидные антигены, потенциально чужеродные по происхождению, иммунной системе с целью выявления или подавления ответов Т- (хелперных) -клеток, которые в конечном итоге приводят к выработке антител против того же пептидного антигена. . Антигенпрезентирующие клетки (макрофаги, B-клетки и дендритные клетки ) представляют собой клетки, в которых обычно обнаруживаются DR. Повышенное содержание «антигена» DR на поверхности клетки часто является ответом на стимуляцию, и, следовательно, DR также является маркером иммунной стимуляции.
Состав
HLA-DR является αβ гетеродимером , рецептор клеточной поверхности , каждая субъединица которых содержит два внеклеточных домен, домен трансмембранного и цитоплазматический хвост. Обе цепи α и β закреплены в мембране. N-концевой домен зрелого белка образует альфа-спираль, которая составляет открытую часть связывающей бороздки, C-концевой участок цитоплазмы взаимодействует с другой цепью, образуя бета-лист под связывающей бороздкой, проходящей через клеточную мембрану. Большинство положений контакта пептида находятся в первых 80 остатках каждой цепи.
Генетика
В генетике по HLA-DR является сложным. HLA-DR кодируется несколькими локусами и несколькими «генами», выполняющими различные функции в каждом локусе. ДР α-цепь кодируется HLA-DRA локуса . В отличие от других локусов DR, функциональные вариации в продуктах зрелого гена DRA отсутствуют. (Примечание: см. Таблицу Количество вариантов локусов HLA-DR аллелей - снижает потенциальные функциональные комбинации с ~ 1400 до ~ 400 ([таблица не точна, потому что новые аллели добавляются постоянно; не все новые аллели являются функциональными вариантами зрелых субъединиц ]).
| DR | DR - DQ | DR | DQ | Частота | |||
|---|---|---|---|---|---|---|---|
| Серотип | гаплотип | B1 | A1 | B1 | % | ||
| DR1 | DR1 - DQ5 | 01:01 | 01:01 | 05:01 | 9. | 1 | |
| 01:02 | 01:01 | 05:01 | 1. | 4 | |||
| 01:03 | 01:01 | 05:01 | 0. | 5 | |||
| DR3 | DR3 - DQ2 | 03:01 | 05:01 | 02:01 | 13. | 1 | |
| DR4 | DR4 - DQ7 | 04:01 | 0300 | 03:01 | 5. | 4 | |
| 04:07 | 0300 | 03:01 | 0. | 9 | |||
| DR4 - DQ8 | 04:01 | 0300 | 03:02 | 5. | 0 | ||
| 04:02 | 0300 | 03:02 | 1. | 0 | |||
| 04:03 | 0300 | 03:02 | 0. | 4 | |||
| 04:04 | 0300 | 03:02 | 3. | 9 | |||
| 04:05 | 0300 | 03:02 | 0. | 3 | |||
| DR7 | DR7 - DQ2 | 07:01 | 02:01 | 02:02 | 11. | 1 | |
| DR7 - DQ9 | 07:01 | 02:01 | 03:03 | 3. | 7 | ||
| DR8 | DR8 - DQ4 | 8:01 | 04:01 | 04:02 | 2. | 2 | |
| DR8 - DQ7 | 8:03 | 06:01 | 03:01 | 0. | 1 | ||
| DR9 | DR9 - DQ9 | 09:01 | 0300 | 03:03 | 0. | 8 | |
| DR10 | DR10 - DQ5 | 10:01 | 01:04 | 05:01 | 0. | 7 | |
| DR11 | DR11 - DQ7 | 11:01 | 05:05 | 03:01 | 5. | 6 | |
| 11:03 | 05:05 | 03:01 | 0. | 3 | |||
| 11:04 | 05:05 | 03:01 | 2. | 7 | |||
| DR12 | DR12 - DQ7 | 12:01 | 05:05 | 03:01 | 1. | 1 | |
| DR13 | DR13 - DQ6 | 13:01 | 01:03 | 06:03 | 5. | 6 | |
| 13:02 | 01:02 | 06:04 | 3. | 4 | |||
| 13:02 | 01:02 | 06:09 | 0. | 7 | |||
| DR13 - DQ7 | 13:03 | 05:05 | 03:01 | 0. | 7 | ||
| DR14 | DR14 - DQ5 | 14:01 | 01:04 | 05:03 | 2. | 0 | |
| DR15 | DR15 - DQ6 | 15:01 | 01:02 | 06:02 | 14. | 2 | |
| 15:02 | 01:03 | 06:01 | 0. | 7 | |||
| DR16 | DR16 - DQ5 | 16:01 | 01:02 | 05:02 | 1. | 0 | |
ДР β-цепь , не кодируется 4 локусов, однако не более чем на 3 функциональные локусы присутствуют в одной особи, и не более двух на одной хромосоме. Иногда у человека может быть только 2 копии одного и того же локуса DRB1 *. По HLA-DRB1 локуса повсеместно и кодирует очень большое количество функционально переменной генных продуктов ( HLA-DR1 к HLA-DR17 ). Локус HLA-DRB3 кодирует специфичность HLA-DR52 , умеренно вариабелен и по-разному связан с определенными типами HLA-DRB1 . Локус HLA-DRB4 кодирует специфичность HLA-DR53 , имеет некоторые вариации и связан с определенными типами HLA-DRB1 . Локус HLA-DRB5 кодирует специфичность HLA-DR51 , которая обычно неизменна и связана с типами HLA-DR2 .
- связь (см. таблицу)
-
DQA1 и DQB1
- Нарушение равновесия по сцеплению существует для многих типов DR-DQ .
- Номенклатурные вопросы. Некоторые более ранние исследования могут относиться к DR15 или 16 как к DR2, а DQ5 и DQ6 как к DQ1, поэтому гаплотип DR2-DQ1 обычно относится к DR15-DQ6, но может относиться к DR16-DQ5. DR5 используется для обозначения DR11 и DR12, и в этом случае можно использовать DQ3. В этих случаях DQ3 почти всегда можно интерпретировать как DQ7, но DR5 чаще всего DR11 и реже DR12. Аналогичные проблемы существуют для DR6 по сравнению с DR13 и DR14. DR6-DQ1 может относиться к DR13-DQ6 или, реже, к DR14-DQ5, но DR6-DQ3 или DR6-DQ7 обычно относится к DR13-DQ7. Даже в более старой литературе есть более запутанные обозначения. Глядя на изменение ассоциации заболевания с улучшенным тестированием, мы можем увидеть, как номенклатура HLA менялась с течением времени.
-
DQA1 и DQB1
| HLA-DR | ||||
|---|---|---|---|---|
| HLA | - А1 | - B1 | От -B3 до -B5 1 | Потенциал |
| Locus | # | # | # | Комбинации |
| Аллели | 3 | 463 | 74 | 1635 |
| Уникальный полипептид | 2 | 394 | 57 год | 902 |
| Контактный вариант | 1 | ~ 300 | ~ 30 | ~ 330 |
| 1 DRB3, DRB4, DRB5 имеют вариабельное присутствие у людей | ||||
Эволюция и частоты аллелей
У HLA DRB1 высокий уровень аллельного разнообразия, по количеству аллельных вариантов он уступает только локусу HLA-B. Эти два локуса представляют собой самую высокую скорость изменения последовательности в геноме человека. Это означает, что HLA-DRB1 быстро развивается, гораздо быстрее, чем почти все другие локусы, кодирующие белок. Большая часть вариаций в HLA DRB1 происходит в позициях контакта пептида в связывающей бороздке, в результате чего многие аллели изменяют способ связывания DR пептидных лигандов и изменяют репертуар, который может связываться каждым рецептором. Это означает, что большинство изменений имеют функциональный характер и, следовательно, находятся на стадии отбора. В области HLA гены подвергаются гетерозиготному или уравновешивающему отбору, хотя определенные аллели, по-видимому, находятся под положительным или отрицательным отбором, в прошлом или в настоящем.
HLA обычно развиваются в процессе генной конверсии , которая является формой короткой или «прерванной» генетической рекомбинации . Функциональные мотивы в генах обмениваются с образованием новых аллелей и часто новых, функционально различных изоформ DR . HLA-DR представляет собой крайний пример этого. Обзор X-сцепленных локусов показывает, что большинство локусов человека претерпели фиксацию в течение последних 600 000 лет, а диплоидные локусы претерпели значительную часть фиксации за этот период времени.
Уровень глубокого ветвления в X-сцепленных локусах указывает на то, что локусы были близки к фиксации или зафиксированы в конце узкого места человеческой популяции 100 000–150 000 лет назад. Локус HLA-DR представляет собой серьезное исключение из этого наблюдения. Основываясь на распределении основных групп в человеческой популяции, можно утверждать, что более десятка основных вариантов пережили узкое место в популяции. Это наблюдение подтверждается концепцией коэффициента гетерозиготного отбора, действующего на HLA-DR и в локусе HLA-DRB1 в большей степени по сравнению с HLA-DQB1 и HLA-DPB1 . Большинство аллелей HLA, присутствующих в настоящее время в человеческой популяции, можно объяснить преобразованием генов между этими древними предковыми типами, некоторые из которых сохраняются в современной популяции.
Серогруппы
| Серотипы продуктов гена HLA-DRB1 | ||
| Расщепленные антигены | ||
| HLA-DR1 | ||
| HLA-DR2 | HLA-DR15 | HLA-DR16 |
| HLA-DR3 | HLA-DR17 | HLA-DR18 |
| HLA-DR4 | ||
| HLA-DR5 | HLA-DR11 | HLA-DR12 |
| HLA-DR6 | HLA-DR13 | HLA-DR14 |
| HLA-DR7 | ||
| HLA-DR8 | ||
| HLA-DR9 | ||
| HLA-DR10 | ||
В таблице ниже приведены ссылки на подстраницы с информацией о распространении, генетической связи и ассоциации заболеваний для серогрупп HLA-DR.
Связь Interlocus DRB
DRB1 связан с другими локусами DRB четырьмя способами.
| не DRB1 | связанные антигены DRB1 | |||
|---|---|---|---|---|
| антигены | антигены | |||
| Никто | DR1 | DR8 | DR10 | |
| DR51 | DR2 | DR15 | DR16 | |
| DR52 | DR3 | DR17 | DR18 | |
| DR5 | DR11 | DR12 | ||
| DR6 | DR13 | DR14 | ||
| DR53 | DR4 | DR7 | DR8 | DR9 |
| Класс | Болезнь | Ассоциированный DR | 2 | 3 | 4 |
|---|---|---|---|---|---|
| очаговая алопеция | DR5 | ||||
| анемия | пагубный | DR15 | |||
| антифосфолипидный синдром , первичный | DR5 | DR12 | |||
| аневризма | коронарной артерии | DR16 | |||
| артериит | Такаясу | DR16 | |||
| артрит , ревматоидный | малолетний | DR4 | DR5 | DR14 | DR15 |
| pauciarticular, juv. | DR8 | ||||
| Болезнь Стилла | DR12 | ||||
| ирит с юв. артрит | DR12 | ||||
| серопозитивный | DR1 | DR4 | DR10 | ||
| с системным склерозом | DR1 | ||||
| болезнь Лайма, вызванная | DR4 | ||||
| непереносимость тиопронина | DR5 | DR11 | DR12 | ||
| кардиомиопатия | гипертрофический | DR4 | DR17 | ||
| T. cruzi индуцировал | DR4 | DR7 | DR15 | ||
| колит | Крона | DR1 | |||
| язвенный | DR1 | ||||
| диабет | ювенильный ( тип 1 ) | DR3 | DR4 | DR17 | DR18 |
| жирная печень ( тип 2 ) | DR8 | ||||
| энцефаломиелит | вакцина против бешенства | DR17 | |||
| энцефалопатия | острый некротизирующий | DR52 | |||
| эпилепсия | детство | DR5 | |||
| инфантильный / спазм | DR17 | ||||
| сердечное заболевание | ревматический | DR16 | |||
| гепатит | аутоиммунный | DR2 | DR4 | DR17 | |
| первичный билиарный цирроз | DR2 | DR8 | |||
| хронический тип C | DR11 | ||||
| красный плоский лишай | DR1 | DR10 | |||
| волчанка , | системный | DR3 | DR4 | DR52 | |
| гидралазин-индуцированный | DR4 | ||||
| с синдромом Шегрена | DR15 | ||||
| лимфаденопатия | обобщенный | DR5 | |||
| лимфома , | грибовидный микоз | DR5 | |||
| мелиоидоз | DR16 | ||||
| миастения | гравис | DR3 | DR6 | DR13 | DR14 |
| пеницилламин-индуцированный | DR1 | ||||
| миозит | воспалительное тело включения | DR17 | DR18 | DR52 | |
| нарколепсия | DR2 | DR12 | |||
| нефрит , | тубулоинтерстициальный | DR1 | |||
| нефропатия | IgA-опосредованный | DR4 | |||
| синдром полигландулярной недостаточности | DR5 | ||||
| пузырчатка | лиственный | DR1 | |||
| vulgaris | DR4 | ||||
| псориаз | vulgaris | DR1 | DR7 | ||
| папилломатоз, | респираторный | DR1 | |||
| саркоидоз | не хронический | DR17 | DR52 | ||
| склероз , | несколько | DR2 | DR15 | DR53 | |
| "начало схватки" множественное | DR3 | ||||
| системный | DR4 | DR11 | DR16 | DR52 | |
| вульвальный лишай | DR12 | ||||
| шизофрения | DR1 | ||||
| восприимчивость | проказа | DR2 | |||
| туберкулез | DR2 | ||||
| аллергия на амброзию Ra6 | DR5 | ||||
| астма, чувствительность к клещам | DR11 | ||||
| Вторичная инфекция, СПИД | DR3 | ||||
| аспергиллез | DR15 | ||||
| Саркома Капоши | DR5 | ||||
| карциномы щитовидной железы | DR8 | DR11 | |||
| рак яичников / шейки матки | DR10 | DR11 | DR15 | ||
| анафилаксия, вызванная виноградом | DR11 | ||||
| Chlamydia pneumoniae | DR52 | ||||
| тиреоидит | Хашимото | DR3 | DR5 | ||
| Могилы | DR3 | DR17 | DR52 | ||
| увеит | тубулоинтерстициальный | DR1 | |||
| * ссылки представлены на связанных подстраницах | |||||
использованная литература
дальнейшее чтение
- Бенишу С., Бенмера А. (2003). «Nef ВИЧ и белки K3 / K5 вируса, ассоциированного с саркомой Капоши:« паразиты »пути эндоцитоза» . Med Sci (Париж) . 19 (1): 100–6. DOI : 10.1051 / medsci / 2003191100 . PMID 12836198 .
- Толструп М., Остергард Л., Лаурсен А.Л. и др. (2004). «Ускользание от иммунного надзора за ВИЧ / ВИП: в центре внимания Nef». Curr. HIV Res . 2 (2): 141–51. DOI : 10.2174 / 1570162043484924 . PMID 15078178 .
- Андерсон Дж. Л., Надежда Т. Дж. (2005). «Вспомогательные белки ВИЧ и выживание в клетке-хозяине». Текущие отчеты о ВИЧ / СПИДе . 1 (1): 47–53. DOI : 10.1007 / s11904-004-0007-х . PMID 16091223 . S2CID 34731265 .
- Li L, Li HS, Pauza CD, et al. (2006). «Роль вспомогательных белков ВИЧ-1 в вирусном патогенезе и взаимодействиях хозяин-патоген» . Cell Res . 15 (11–12): 923–34. DOI : 10.1038 / sj.cr.7290370 . PMID 16354571 .
- Плита V, Верхассельт B (2006). «Моделирование эффектов Nef ВИЧ-1 в тимусе». Curr. HIV Res . 4 (1): 57–64. DOI : 10.2174 / 157016206775197583 . PMID 16454711 .
- Мацусима Г.К., Ито-Линдстрем Ю., Тинг Дж. П. (1992). «Активация гена HLA-DRA в первичных Т-лимфоцитах человека: новое использование ТАТА и элементов промоторов X и Y» . Мол. Клетка. Биол . 12 (12): 5610–9. DOI : 10,1128 / MCB.12.12.5610 . PMC 360500 . PMID 1448091 .
- Шайфф В.Т., Хруска К.А., Маккорт Д.В. и др. (1992). «HLA-DR связывается со специфическими стрессовыми белками и сохраняется в эндоплазматическом ретикулуме в инвариантных клетках с отрицательной цепью» . J. Exp. Med . 176 (3): 657–66. DOI : 10,1084 / jem.176.3.657 . PMC 2119345 . PMID 1512535 .
- Пьятье-Тонно Д., Гастинель Л.Н., Амблард Ф. и др. (1991). «Взаимодействие CD4 с антигенами HLA класса II и gp120 ВИЧ». Иммуногенетика . 34 (2): 121–8. DOI : 10.1007 / BF00211424 . PMID 1869305 . S2CID 10116507 .
- Нонг И, Кандил О., Тобин Э. Х. и др. (1991). «Коровой белок p24 ВИЧ ингибирует индуцированное гамма-интерфероном повышение уровней мРНК тяжелой цепи HLA-DR и цитохрома b в человеческой моноцитоподобной клеточной линии THP1». Клетка. Иммунол . 132 (1): 10–6. DOI : 10.1016 / 0008-8749 (91) 90002-S . PMID 1905983 .
- Rosenstein Y, Burakoff SJ, Herrmann SH (1990). «ВИЧ-gp120 может блокировать адгезию, опосредованную МНС CD4-класса II». J. Immunol . 144 (2): 526–31. PMID 1967269 .
- Каллахан К.М., Форт М.М., Обах Е.А. и др. (1990). «Генетическая изменчивость gp120 ВИЧ-1 влияет на взаимодействие с молекулами HLA и рецептором Т-клеток». J. Immunol . 144 (9): 3341–6. PMID 1970352 .
- Bowman MR, MacFerrin KD, Schreiber SL, Burakoff SJ (1991). «Идентификация и структурный анализ остатков в области V1 CD4, участвующих во взаимодействии с гликопротеином оболочки вируса иммунодефицита человека gp120 и молекулами главного комплекса гистосовместимости класса II» . Proc. Natl. Акад. Sci. США . 87 (22): 9052–6. DOI : 10.1073 / pnas.87.22.9052 . PMC 55099 . PMID 1978941 .
- Коппельман Б., Крессвелл П. (1990). «Быстрая нелизосомная деградация собранных гликопротеинов HLA класса II, включающих мутантную альфа-цепь DR». J. Immunol . 145 (8): 2730–6. PMID 2212658 .
- Клейтон Л.К., Сие М., Благочестивый Д.А., Рейнхерц Е.Л. (1989). «Идентификация остатков CD4 человека, влияющих на MHC класса II по сравнению с связыванием gp120 ВИЧ-1» . Природа . 339 (6225): 548–51. Bibcode : 1989Natur.339..548C . DOI : 10.1038 / 339548a0 . PMID 2543930 . S2CID 4246781 .
- Diamond DC, Sleckman BP, Gregory T и др. (1988). «Ингибирование функции CD4 + Т-клеток белком оболочки ВИЧ, gp120». J. Immunol . 141 (11): 3715–7. PMID 2846691 .
- Тьернлунд У., Шейниус А., Йоханссон С. и др. (1989). «Т-клеточный ответ на очищенное производное белка после удаления клеток Лангерганса из суспензий эпидермальных клеток, содержащих кератиноциты, экспрессирующие трансплантационные антигены класса II». Сканд. J. Immunol . 28 (6): 667–73. DOI : 10.1111 / j.1365-3083.1988.tb01500.x . PMID 3266023 . S2CID 25824282 .
- Андрие Дж. М., Эвен П., Венет А. (1986). «СПИД и родственные синдромы как вирусное аутоиммунное заболевание иммунной системы: нарушение анти-MHC II. Терапевтические последствия». Исследования СПИДа . 2 (3): 163–74. DOI : 10,1089 / aid.1.1986.2.163 . PMID 3489470 .
- Дас Х.К., Лоуренс С.К., Вайсман С.М. (1983). «Структура и нуклеотидная последовательность гена тяжелой цепи HLA-DR» . Proc. Natl. Акад. Sci. США . 80 (12): 3543–7. Полномочный код : 1983PNAS ... 80.3543D . DOI : 10.1073 / pnas.80.12.3543 . PMC 394085 . PMID 6304715 .
- Schamboeck A, Korman AJ, Kamb A, Strominger JL (1984). «Организация транскрипционной единицы антигена гистосовместимости класса II человека: тяжелая цепь HLA-DR» . Nucleic Acids Res . 11 (24): 8663–75. DOI : 10.1093 / NAR / 11.24.8663 . PMC 326615 . PMID 6324094 .
- Дас Х.К., Биро П.А., Коэн С.Н. и др. (1983). «Использование синтетических олигонуклеотидных зондов, комплементарных генам альфа и бета HLA-DR человека, в качестве праймеров для удлинения для выделения 5'-специфичных геномных клонов» . Proc. Natl. Акад. Sci. США . 80 (6): 1531–5. Bibcode : 1983PNAS ... 80.1531D . DOI : 10.1073 / pnas.80.6.1531 . PMC 393635 . PMID 6403940 .
внешние ссылки
- HLA-DR + антигены в предметных рубриках медицинской тематики Национальной медицинской библиотеки США (MeSH)