Коллективный иммунитет -Herd immunity

Коллективный иммунитет (также называемый стадным эффектом , коллективным иммунитетом , популяционным иммунитетом или массовым иммунитетом ) — это форма косвенной защиты от инфекционных заболеваний , которая может возникать при некоторых заболеваниях, когда достаточный процент населения становится невосприимчивым к инфекции, будь то в результате предшествующего инфекций или вакцинации , тем самым снижая вероятность заражения у лиц с недостаточным иммунитетом. Иммунные люди вряд ли будут способствовать передаче болезни , нарушая цепочки инфекций, что останавливает или замедляет распространение болезни. Чем больше доля иммунных людей в сообществе, тем меньше вероятность того, что неиммунные люди вступят в контакт с инфицированным человеком.
Люди могут стать невосприимчивыми , выздоровев от более ранней инфекции или с помощью вакцинации. Некоторые люди не могут стать иммунными из-за заболеваний, таких как иммунодефицит или иммуносупрессия , и для этой группы коллективный иммунитет является решающим методом защиты. Как только порог коллективного иммунитета достигнут, болезнь постепенно исчезает из популяции. Эта ликвидация, если она будет достигнута во всем мире, может привести к постоянному сокращению числа инфекций до нуля, что называется ликвидацией . Коллективный иммунитет, созданный с помощью вакцинации, способствовал окончательной ликвидации оспы в 1977 году и способствовал уменьшению других заболеваний. Коллективный иммунитет применяется только к инфекционным заболеваниям , что означает, что они передаются от одного человека к другому. Столбняк , например, заразен, но не заразен, поэтому коллективный иммунитет не применяется.
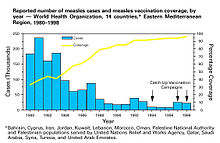
Коллективный иммунитет был признан естественным явлением в 1930-х годах, когда было замечено, что после того, как значительное число детей стали невосприимчивы к кори , число новых инфекций временно уменьшилось. С тех пор массовая вакцинация для индукции коллективного иммунитета стала обычным явлением и доказала свою эффективность в предотвращении распространения многих инфекционных заболеваний. Противодействие вакцинации поставило под угрозу коллективный иммунитет, позволив предотвратимым заболеваниям сохраняться или возвращаться к популяциям с недостаточным уровнем вакцинации.
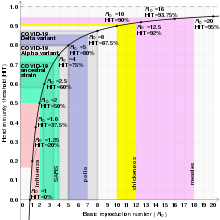
Точный порог коллективного иммунитета (HIT) варьируется в зависимости от основного репродуктивного числа болезни. Примером заболевания с высоким порогом является корь, при которой ГИТ превышает 95%.
Эффекты
Защита тех, у кого нет иммунитета
Некоторые люди либо не могут выработать иммунитет после вакцинации, либо по медицинским показаниям не могут быть вакцинированы. Новорожденные слишком малы, чтобы получать многие вакцины либо по соображениям безопасности, либо потому, что пассивный иммунитет делает вакцину неэффективной. Лица с иммунодефицитом из-за ВИЧ/СПИДа , лимфомы , лейкемии , рака костного мозга , нарушения функции селезенки , химиотерапии или лучевой терапии могут утратить иммунитет, который у них был ранее, и вакцины могут быть бесполезны для них из-за их иммунодефицита.
У части вакцинированных может не развиться длительный иммунитет. Противопоказания к вакцинации могут препятствовать вакцинации определенных лиц. Помимо отсутствия иммунитета, люди в одной из этих групп могут подвергаться большему риску развития осложнений от инфекции из-за своего медицинского статуса, но они все же могут быть защищены, если достаточно большой процент населения имеет иммунитет.
Высокий уровень иммунитета в одной возрастной группе может создать коллективный иммунитет для других возрастных групп. Вакцинация взрослых против коклюша снижает заболеваемость коклюшем среди младенцев, слишком маленьких для вакцинации, которые подвергаются наибольшему риску осложнений от болезни. Это особенно важно для близких членов семьи, на долю которых приходится большая часть случаев передачи инфекции младенцам раннего возраста. Таким же образом дети, получающие вакцины против пневмококка, снижают заболеваемость пневмококковой инфекцией среди младших непривитых братьев и сестер. Вакцинация детей против пневмококка и ротавируса привела к снижению числа госпитализаций, связанных с пневмококком и ротавирусом , среди детей старшего возраста и взрослых, которые обычно не получают эти вакцины. Грипп (грипп) протекает более тяжело у пожилых людей, чем у более молодых возрастных групп, но вакцины против гриппа неэффективны в этой демографической группе из-за ослабления иммунной системы с возрастом. Однако было показано, что отдание приоритета детям школьного возраста для иммунизации против сезонного гриппа, которая более эффективна, чем вакцинация пожилых людей, создает определенную степень защиты для пожилых людей.
В отношении инфекций, передающихся половым путем (ИППП), высокий уровень иммунитета у гетеросексуалов одного пола индуцирует коллективный иммунитет у гетеросексуалов обоих полов. Вакцины против ИППП, предназначенные для гетеросексуалов одного пола, приводят к значительному снижению заболеваемости ИППП среди гетеросексуалов обоих полов, если иммунизация целевого пола высока. Однако коллективный иммунитет от вакцинации самок не распространяется на самцов, имеющих половые контакты с самцами. Поведение, связанное с высоким риском, затрудняет устранение ИППП, поскольку, несмотря на то, что большинство случаев инфицирования происходит среди лиц с умеренным риском, большая часть случаев передачи инфекции происходит из-за лиц, поведение которых сопряжено с высоким риском. По этой причине в некоторых группах населения может потребоваться иммунизация лиц из групп высокого риска независимо от пола.
Эволюционное давление и замена серотипа
Коллективный иммунитет сам по себе действует как эволюционное давление на патогены, влияя на эволюцию вируса , стимулируя производство новых штаммов, называемых ускользающими мутантами, которые способны уклоняться от коллективного иммунитета и заражать ранее иммунных людей. Эволюция новых штаммов известна как замена серотипа или сдвиг серотипа, поскольку распространенность определенного серотипа снижается из-за высокого уровня иммунитета, что позволяет другим серотипам замещать его.
На молекулярном уровне вирусы ускользают от коллективного иммунитета посредством антигенного дрейфа , когда мутации накапливаются в той части вирусного генома , которая кодирует поверхностный антиген вируса , обычно белок вирусного капсида , вызывая изменение вирусного эпитопа . В качестве альтернативы, реассортация отдельных сегментов вирусного генома или антигенный сдвиг , который более распространен, когда в циркуляции находится больше штаммов, также может привести к образованию новых серотипов . Когда происходит что-либо из этого, Т-клетки памяти больше не распознают вирус, поэтому люди не имеют иммунитета к доминирующему циркулирующему штамму. Как для гриппа, так и для норовируса эпидемии временно вызывают коллективный иммунитет, пока не появится новый доминирующий штамм, вызывающий последовательные волны эпидемий. Поскольку эта эволюция бросает вызов коллективному иммунитету, разрабатываются широко нейтрализующие антитела и «универсальные» вакцины, которые могут обеспечить защиту за пределами определенного серотипа.
Первоначальные вакцины против Streptococcus pneumoniae значительно снизили назофарингеальное носительство вакцинных серотипов (VT), включая устойчивые к антибиотикам типы, но были полностью компенсированы увеличением носительства невакцинных серотипов (NVT). Однако это не привело к пропорциональному увеличению заболеваемости, поскольку НЖТ были менее инвазивными, чем ЖТ. С тех пор были внедрены пневмококковые вакцины , которые обеспечивают защиту от новых серотипов и успешно противостоят их появлению. Возможность смещения в будущем остается, поэтому дальнейшие стратегии для решения этой проблемы включают расширение охвата VT и разработку вакцин, в которых используются либо убитые целые клетки , которые имеют больше поверхностных антигенов, либо белки, присутствующие в нескольких серотипах.
Искоренение болезней
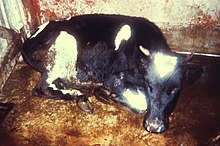
Если коллективный иммунитет установился и поддерживается в популяции в течение достаточного времени, болезнь неизбежно ликвидируется – больше не происходит эндемических передач. Если элиминация достигнута во всем мире и число случаев заболевания навсегда сведено к нулю, то болезнь можно объявить искорененной. Таким образом, искоренение можно считать конечным эффектом или конечным результатом инициатив общественного здравоохранения по борьбе с распространением инфекционных заболеваний. В случаях, когда коллективный иммунитет нарушен, наоборот, вероятны вспышки заболеваний среди невакцинированного населения.
Преимущества искоренения включают прекращение всей заболеваемости и смертности, вызванных болезнью, экономию финансовых средств для отдельных лиц, поставщиков медицинских услуг и правительств, а также возможность использования ресурсов, используемых для борьбы с болезнью, в других местах. На сегодняшний день с помощью коллективного иммунитета и вакцинации ликвидированы две болезни: чума крупного рогатого скота и оспа . Усилия по искоренению полиомиелита , основанные на коллективном иммунитете, в настоящее время предпринимаются, хотя гражданские беспорядки и недоверие к современной медицине затруднили это. Обязательная вакцинация может быть полезна для усилий по искоренению, если недостаточное количество людей решит пройти вакцинацию.
Бесплатная езда
Коллективный иммунитет уязвим перед проблемой безбилетника . Лица, у которых отсутствует иммунитет, в том числе те, кто предпочитает не вакцинироваться, бесплатно пользуются коллективным иммунитетом, созданным теми, у кого есть иммунитет. По мере увеличения числа безбилетников в популяции вспышки предотвратимых болезней становятся более частыми и более серьезными из-за потери коллективного иммунитета. Люди могут предпочесть безбилетник или воздержаться от вакцинации по целому ряду причин, включая убеждение в том, что вакцины неэффективны или что риски, связанные с вакцинами, выше, чем риски, связанные с инфекцией, недоверие к вакцинам или должностным лицам системы здравоохранения, пропаганда или групповое мышление , социальные нормы или давление со стороны сверстников и религиозные убеждения. Некоторые люди с большей вероятностью предпочтут не получать вакцины, если показатели вакцинации достаточно высоки, чтобы убедить человека в том, что ему или ей, возможно, не нужна вакцинация, поскольку достаточный процент других уже имеет иммунитет.
Механизм
Люди, которые невосприимчивы к болезни, действуют как барьер в распространении болезни, замедляя или предотвращая передачу болезни другим. Индивидуальный иммунитет может быть приобретен в результате естественной инфекции или искусственными средствами, такими как вакцинация. Когда критическая часть населения становится невосприимчивой, что называется порогом коллективного иммунитета (HIT) или уровнем коллективного иммунитета (HIL), заболевание может больше не сохраняться в популяции, переставая быть эндемичным .
Теоретическая основа коллективного иммунитета обычно предполагает, что вакцины вызывают стойкий иммунитет, что популяции смешиваются случайным образом, что патоген не эволюционирует, чтобы уклониться от иммунного ответа, и что не существует нечеловеческого переносчика болезни.
Теоретические основы
Критическое значение или пороговое значение для данной популяции — это точка, в которой болезнь достигает эндемического устойчивого состояния , что означает, что уровень инфекции не растет и не снижается экспоненциально . Этот порог можно рассчитать из эффективного числа репродукции R e , полученного путем произведения основного числа воспроизводства R 0 , среднего числа новых инфекций, вызванных каждым случаем в полностью восприимчивой популяции, которая является однородной или хорошо смешанный, что означает, что каждый человек с равной вероятностью вступит в контакт с любым другим восприимчивым человеком в популяции, и S , доля населения, восприимчивого к инфекции, и установив этот продукт равным 1:
S можно переписать как (1 − p ), где p — доля иммунного населения, так что p + S равно единице. Затем уравнение можно переставить, чтобы поместить p отдельно, следующим образом:
Поскольку p сам по себе находится в левой части уравнения, его можно переименовать в pc , представляя критическую долю населения, необходимую для иммунитета, чтобы остановить передачу болезни, что совпадает с «порогом коллективного иммунитета». УДАР. R 0 функционирует как мера контагиозности, поэтому низкие значения R 0 связаны с более низкими HIT, тогда как более высокие значения R 0 приводят к более высоким HIT. Например, HIT для заболевания с R 0 2 теоретически составляет только 50%, тогда как для заболевания с R 0 10 теоретическое HIT составляет 90 %.
Когда эффективное число репродукции Re заразной болезни снижается и поддерживается на уровне ниже 1 новой особи на инфекцию, число случаев, возникающих в популяции, постепенно уменьшается до тех пор, пока болезнь не будет ликвидирована. Если население невосприимчиво к заболеванию, превышающему HIT этого заболевания, число случаев заболевания сокращается более быстрыми темпами, вспышки еще менее вероятны, а возникающие вспышки меньше, чем они были бы в противном случае. Если эффективное репродуктивное число увеличивается до значения выше 1, то болезнь не находится ни в устойчивом состоянии, ни в снижении заболеваемости , а активно распространяется среди населения и заражает большее число людей, чем обычно.
В этих расчетах предполагается, что популяции однородны или хорошо смешаны, а это означает, что каждый человек с равной вероятностью вступает в контакт с любым другим человеком, тогда как в действительности популяции лучше описываются как социальные сети, поскольку люди имеют тенденцию группироваться вместе, оставаясь в относительно тесном контакте с ограниченным числом других лиц. В этих сетях передача происходит только между теми, кто географически или физически находится близко друг к другу. Форма и размер сети, вероятно, изменяют ГИТ заболевания, делая заболеваемость более или менее распространенной.
В неоднородных популяциях R 0 считается мерой числа случаев, генерируемых «типичным» инфекционным лицом, которое зависит от того, как люди внутри сети взаимодействуют друг с другом. Взаимодействия внутри сетей более распространены, чем между сетями, и в этом случае наиболее тесно связанные сети легче передают заболевание, что приводит к более высокому R 0 и более высокому HIT, чем это требуется в менее связанной сети. В сетях, которые либо предпочитают не становиться иммунными, либо недостаточно иммунизированы, болезни могут сохраняться, несмотря на то, что они не существуют в сетях с более высокой иммунизацией.
| Болезнь | Передача инфекции | Р 0 | УДАР |
|---|---|---|---|
| Корь | аэрозоль | 12–18 | 92–94% |
| Ветряная оспа (ветряная оспа) | аэрозоль | 10–12 | 90–92% |
| Свинка | Дыхательные капли | 10–12 | 90–92% |
| Краснуха | Дыхательные капли | 6–7 | 83–86% |
| Полиомиелит | Фекально-оральный путь | 5–7 | 80–86% |
| Коклюш | Дыхательные капли | 5,5 | 82% |
| COVID-19 ( вариант Дельта ) | Респираторные капли и аэрозоль | 5.1 | 80% |
| Оспа | Дыхательные капли | 3,5–6,0 | 71–83% |
| COVID-19 ( альфа-вариант ) | Респираторные капли и аэрозоль | 4–5 | 75–80% |
| ВИЧ/СПИД | Телесные жидкости | 2–5 | 50–80% |
| COVID-19 ( наследственный штамм ) | Респираторные капли и аэрозоль | 2,9 ( 2.4 –3.4 ) | 65% (58 –71% ) |
| атипичная пневмония | Дыхательные капли | 2–4 | 50–75% |
| Дифтерия | слюна | 2,6 (1,7 –4.3 ) | 62% (41 –77% ) |
| Простуда | Дыхательные капли | 2–3 | 50–67% |
| Грипп ( пандемический штамм 1918 г. ) | Дыхательные капли | 2 | 50% |
| Эбола ( вспышка 2014 г. ) | Телесные жидкости | 1,8 (1,4 –1.8 ) | 44% (31 –44% ) |
| Грипп ( пандемический штамм 2009 г. ) | Дыхательные капли | 1,6 (1.3 –2.0 ) | 37% (25 –51% ) |
| Грипп (сезонные штаммы) | Дыхательные капли | 1,3 (1.2 –1.4 ) | 23% (17 –29% ) |
| Андский хантавирус | Респираторные капли и биологические жидкости | 1,2 (0,8 –1.6 ) | 16% (0 –36% ) |
| Вирус Нипах | Телесные жидкости | 0,5 | 0% |
| БВРС | Дыхательные капли | 0,5 (0,3 –0,8 ) | 0% |
Перерегулирование
Совокупная доля лиц, заразившихся в ходе вспышки заболевания, может превышать HIT. Это связано с тем, что HIT представляет собой не точку, в которой болезнь перестает распространяться, а скорее точку, в которой каждый инфицированный человек в среднем заражает менее одного дополнительного человека. При достижении HIT количество дополнительных заражений не сразу падает до нуля. Превышение кумулятивной доли инфицированных лиц над теоретическим HIT известно как выброс .
Бусты
вакцинация
Основным способом повышения уровня иммунитета у населения является вакцинация. Первоначально вакцинация основывалась на наблюдении, что доярки, подвергшиеся воздействию коровьей оспы , были невосприимчивы к оспе, поэтому практика вакцинации людей вирусом коровьей оспы началась как способ предотвращения оспы. Хорошо разработанные вакцины обеспечивают защиту гораздо более безопасным способом, чем естественные инфекции, поскольку вакцины, как правило, не вызывают заболеваний, от которых они защищают, а серьезные побочные эффекты встречаются значительно реже, чем осложнения от естественных инфекций.
Иммунная система не делает различий между естественными инфекциями и вакцинами, формируя активный ответ на оба, поэтому иммунитет, вызванный вакцинацией, подобен тому, который возник бы при заражении и выздоровлении от болезни. Для достижения коллективного иммунитета с помощью вакцинации производители вакцин стремятся производить вакцины с низким уровнем отказов, а политики стремятся поощрять их использование . После успешного внедрения и широкого применения вакцины можно наблюдать резкое снижение заболеваемости болезнями, от которых она защищает, что снижает число госпитализаций и смертей от таких болезней.
Если предположить, что вакцина эффективна на 100%, то уравнение, используемое для расчета порога коллективного иммунитета, можно использовать для расчета уровня вакцинации, необходимого для элиминации болезни, который записывается как V c . Однако вакцины обычно несовершенны, поэтому необходимо учитывать эффективность E вакцины:
Из этого уравнения видно, что если E меньше (1 − 1/ R 0 ), то ликвидировать болезнь невозможно, даже если вакцинировать все население. Точно так же ослабление индуцированного вакциной иммунитета, как это происходит с бесклеточными коклюшными вакцинами , требует более высоких уровней бустерной вакцинации для поддержания коллективного иммунитета. Если болезнь перестала быть эндемичной для населения, то естественные инфекции больше не способствуют сокращению доли восприимчивого населения. Этому снижению способствует только вакцинация. Связь между охватом и эффективностью вакцинации и заболеваемостью можно показать путем вычитания произведения эффективности вакцины и доли вакцинированного населения, p v , из уравнения порога коллективного иммунитета следующим образом:
Из этого уравнения можно заметить, что при прочих равных условиях (" при прочих равных условиях ") любое увеличение либо охвата вакцинацией, либо эффективности вакцины, включая любое превышение ГИТ заболевания, еще больше снижает число случаев заболевания. . Скорость снижения числа случаев зависит от R 0 болезни, при этом болезни с более низкими значениями R 0 испытывают более резкое снижение.
Вакцины обычно имеют как минимум одно противопоказание для определенной группы населения по медицинским показаниям, но если и эффективность, и охват достаточно высоки, коллективный иммунитет может защитить этих людей. На эффективность вакцины часто, но не всегда, негативно влияет пассивный иммунитет, поэтому для некоторых вакцин рекомендуются дополнительные дозы, в то время как другие не вводятся до тех пор, пока человек не потеряет свой пассивный иммунитет.
Пассивный иммунитет
Индивидуальный иммунитет можно приобрести и пассивно, когда антитела к возбудителю передаются от одного человека к другому. Это может происходить естественным путем, когда материнские антитела, прежде всего антитела иммуноглобулина G , передаются через плаценту и с молозивом плодам и новорожденным. Пассивный иммунитет можно получить и искусственно, когда восприимчивому человеку вводят антитела из сыворотки или плазмы иммунного человека.
Защита, создаваемая пассивным иммунитетом, проявляется немедленно, но ослабевает в течение нескольких недель или месяцев, поэтому любой вклад в коллективный иммунитет носит временный характер. При заболеваниях, особенно тяжелых среди плодов и новорожденных, таких как грипп и столбняк, беременным женщинам может быть сделана прививка с целью передачи антител ребенку. Таким же образом группы высокого риска, которые либо с большей вероятностью заразятся, либо у которых с большей вероятностью разовьются осложнения от инфекции, могут получать препараты антител для предотвращения этих инфекций или для уменьшения тяжести симптомов.
Анализ выгоды и затрат
Коллективный иммунитет часто учитывается при проведении анализа затрат и результатов программ вакцинации. Это рассматривается как положительный внешний эффект высокого уровня иммунитета, дающий дополнительное преимущество в снижении заболеваемости, которого не было бы, если бы у населения не сформировался коллективный иммунитет. Таким образом, включение коллективного иммунитета в анализ затрат и выгод приводит как к более благоприятному соотношению затрат и эффективности или затрат и выгод, так и к увеличению числа случаев заболеваний, предотвращенных с помощью вакцинации. Планы исследований, проведенные для оценки пользы коллективного иммунитета, включают регистрацию заболеваемости в домохозяйствах с вакцинированным членом, рандомизацию населения в одном географическом районе для вакцинации или нет, а также наблюдение за заболеваемостью до и после начала программы вакцинации. Из них можно сделать вывод, что заболеваемость может снизиться до уровня, превышающего тот, который можно предсказать только по прямой защите, что указывает на то, что коллективный иммунитет способствовал снижению. Когда учитывается замена серотипа , это снижает ожидаемую пользу от вакцинации.
История
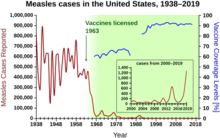
Термин «стадный иммунитет» впервые был использован в 1894 году американским ученым-ветеринаром, а затем начальником Бюро животноводства Министерства сельского хозяйства США Дэниелом Элмером Сэлмоном для описания здоровой жизненной силы и устойчивости к болезням сытых стад свиней. В 1916 году ученые-ветеринары того же Бюро животноводства использовали этот термин для обозначения иммунитета, возникающего после выздоровления крупного рогатого скота, зараженного бруцеллезом, также известного как «заразный аборт». К 1923 году британские бактериологи использовали его для описания экспериментальных эпидемий на мышах, экспериментов, предпринятых в рамках усилий по моделированию эпидемических заболеваний человека. К концу 1920-х годов эта концепция широко использовалась, особенно среди британских ученых, для описания формирования у населения иммунитета к таким заболеваниям, как дифтерия, скарлатина и грипп. Коллективный иммунитет был признан естественным явлением в 1930-х годах, когда А. В. Хедрич опубликовал исследование по эпидемиологии кори в Балтиморе и обратил внимание на то, что после того, как многие дети стали невосприимчивы к кори, число новых инфекций временно уменьшилось, в том числе среди восприимчивых детей. . Несмотря на это знание, усилия по контролю и ликвидации кори не увенчались успехом, пока в 1960-х годах не началась массовая вакцинация против кори . Массовая вакцинация, обсуждение искоренения болезней и анализ затрат и выгод вакцинации впоследствии привели к более широкому использованию термина «коллективный иммунитет » . В 1970-х годах была разработана теорема, используемая для расчета порога коллективного иммунитета. Во время кампании по ликвидации оспы в 1960-х и 1970-х годах практика кольцевой вакцинации , неотъемлемой частью которой является коллективный иммунитет, началась как способ иммунизации каждого человека в «кольце» вокруг инфицированного человека, чтобы предотвратить распространение вспышек.
С момента принятия массовой и кольцевой вакцинации возникли сложности и проблемы с коллективным иммунитетом. При моделировании распространения инфекционных заболеваний изначально был сделан ряд допущений, а именно, что целые популяции восприимчивы и хорошо смешаны, что на самом деле не так, поэтому были разработаны более точные уравнения. В последние десятилетия было признано, что доминирующий штамм микроорганизма в циркуляции может измениться из-за коллективного иммунитета либо из-за того, что коллективный иммунитет действует как эволюционное давление, либо из-за того, что коллективный иммунитет против одного штамма позволил распространиться другому уже существующему штамму. Возникающие или сохраняющиеся опасения и противоречия по поводу вакцинации привели к снижению или устранению коллективного иммунитета в некоторых сообществах, что позволяет предотвратимым заболеваниям сохраняться или возвращаться в эти сообщества.
Смотрите также
Примечания
использованная литература
внешние ссылки
| Схолия имеет профиль коллективного иммунитета (Q736798) . |
- Топли В.В. , Уилсон Г.С. (май 1923 г.). «Распространение бактериальной инфекции. Проблема коллективного иммунитета» . Журнал гигиены . 21 (3): 243–9. doi : 10.1017/s0022172400031478 . ПВК 2167341 . PMID 20474777 .
- Визуальная симуляция коллективного иммунитета , написанная Шейном Киллианом и модифицированная Робертом Уэббом.
- Моделирование коллективного иммунитета