Наследственный диффузный рак желудка - Hereditary diffuse gastric cancer
| Наследственный диффузный рак желудка | |
|---|---|
| Другие названия | HDGC |
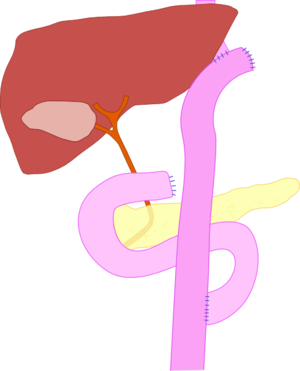 | |
| Диаграмма, демонстрирующая конечный результат тотальной гастрэктомии, наиболее распространенного профилактического лечения HDGC. В этой процедуре пищевод напрямую связан с тонкой кишкой. | |
| Специальность | Онкология , Гастроэнтерология |
| Осложнения | Дольчатый рак молочной железы |
| Обычное начало | 38 лет (средний) |
| Причины | Мутация гена E-кадгерина (CDH1) |
| Факторы риска | Рак желудка |
| Уход | Тотальная гастрэктомия |
| Частота | 1-3% случаев рака желудка |
Наследственный диффузный рак желудка (HDGC) - это наследственный генетический синдром, чаще всего вызываемый инактивирующей мутацией в гене E-кадгерина (CDH1), расположенном на хромосоме 16 . Люди, унаследовавшие неактивную копию гена CDH1, имеют значительно повышенный риск развития рака желудка . По этой причине люди с этими мутациями часто выбирают профилактическую резекцию желудка или полное удаление желудка, чтобы предотвратить этот рак. Мутации в CDH1 также связаны с высоким риском лобулярного рака молочной железы и могут быть связаны с умеренно повышенным риском рака толстой кишки.
Наиболее распространенной формой рака желудка, связанной с мутациями CDH1, является аденокарцинома диффузного типа. По оценкам, у 70% мужчин и 56% женщин, унаследовавших инактивирующую мутацию CDH1, к 80 годам разовьется эта форма рака. По оценкам, риск развития лобулярного рака молочной железы в течение жизни составляет 42%. Средний возраст диагноза рака желудка у людей с мутацией, инактивирующей CDH1, составляет 38 лет, но сообщалось о случаях заболевания в возрасте 14 лет.
Генетика
Наследственный диффузный рак желудка наследуется как аутосомно-доминантная мутация гена E-кадгерина (CDH1), который расположен на хромосоме 16q22.1. Поскольку это состояние свидетельствует только о значительно повышенном риске рака, его можно охарактеризовать как неполное пенетрантное состояние .
Аутосомно-доминантный характер мутаций подразумевает, что наследования только одной мутированной копии гена CDH1 достаточно, чтобы вызвать болезненное состояние. Однако для того, чтобы у этих людей возник рак, обе копии гена CDH1 должны быть неактивными. Следовательно, HDGC развивается в результате потери гетерозиготности , при которой одна немутантная копия гена CDH1 претерпевает мутацию или инактивацию в некоторых клетках в течение жизни индивидуума. Это объясняет, почему у большинства людей с мутациями CDH1 разовьется клинически очевидный рак, а у некоторых - нет.
Ген, мутировавший в HDGC, CDH1, кодирует белок E-Cadherin. Этот белок выполняет множество функций в межклеточных взаимодействиях, а также во внутриклеточной передаче сигналов. Развитие раковых клеток и злокачественных новообразований может быть связано с некоторыми из этих функций. Одна из основных функций включает клеточную адгезию, облегченную связыванием E-кадгерина. Утрата этой функции может привести к дедифференцировке клеток и / или нерегулируемому росту и репликации клеток. Другая важная функция включает связывание и изоляцию фактора транскрипции бета-катенина , поддерживая его неактивность. Утрата этой функции может привести к повышенной активности фактора транскрипции.
Семьям, отвечающим следующим критериям, рекомендуется генетическое консультирование и тестирование на мутации CDH1:
- Семьи с двумя или более задокументированными случаями диффузного рака желудка среди родственников первой или второй степени родства, в которых хотя бы один случай диагностирован до 50 лет.
- Семьи с двумя или более задокументированными случаями лобулярного рака молочной железы среди родственников первой или второй степени родства с диффузным раком желудка или без него у родственников первой или второй степени родства.
- Любой человек с диагнозом диффузный рак желудка в возрасте до 35 лет из группы с низкой заболеваемостью.
Формы, не относящиеся к CDH1
Хотя CDH1 на сегодняшний день является наиболее распространенным геном, связанным с HDGC, около 11% случаев возникают у людей, которые не имеют мутаций в этом гене. Доказано, что никакой другой ген не вызывает HDGC, но возможные ассоциированные гены включают CTNNA1 , BRCA2 , STK11 , SDHB , PRSS1 , ATM , MSR1 и PALB2 .
Уход
Хирургическое удаление желудка (гастрэктомия) обычно рекомендуется людям в возрасте от 20 до 40 лет, чтобы предотвратить развитие диффузной аденокарциномы желудка. Тем не менее, люди, у которых обнаруживаются мутации CDH1 после 40 лет, все же могут рассматриваться для гастрэктомии. При определении оптимального времени для выполнения этой операции следует учитывать физическое и психологическое здоровье каждого человека. Молодые люди могут пожелать отложить эту процедуру, и их часто наблюдают с помощью эндоскопии и случайной биопсии . Кроме того, всем людям с положительным результатом теста проводится первичная эндоскопия, на которой проводится биопсия любого поражения, поскольку рак желудка часто начинается без симптомов.
Женщины с мутациями CDH1 также имеют повышенный риск лобулярной карциномы молочной железы. Этим людям рекомендуется частое обследование на рак груди с помощью маммографии и МРТ .
Риск рака толстой кишки у людей с мутациями CDH1 до сих пор неясен. Из-за небольшого риска, который может быть связан, люди часто проходят скрининговую колоноскопию в возрасте 40 лет, за пять лет до рекомендации среди населения в целом.
Эпидемиология
Средний возраст постановки диагноза - 38 лет. По оценкам, 1-3% случаев рака желудка связаны с наследственными онкологическими синдромами. HDGC - наиболее распространенный наследственный синдром рака желудка.
Изначально HDGC был обнаружен в результате исследований семей маори в Новой Зеландии, в которых отмечалось повышение заболеваемости раком желудка. Выявление мутаций CDH1, вызывающих HDGC, является самым высоким в странах с низкой заболеваемостью раком желудка, таких как США и Канада. И наоборот, выявление мутаций CDH1 является самым низким в странах с высоким уровнем заболеваемости раком желудка, таких как Португалия, Италия и Япония. По этой причине некоторые настаивают на усилении генетического скрининга в странах с высоким уровнем заболеваемости раком желудка, поскольку эти показатели могут скрывать частоту мутаций CDH1.

