Наследственный неполипозный колоректальный рак - Hereditary nonpolyposis colorectal cancer
| Наследственный неполипозный колоректальный рак | |
|---|---|
| Другие имена | Синдром Линча |
 | |
| Микрофотография, показывающая инфильтрирующие опухоль лимфоциты (при колоректальном раке ), обнаружение, связанное с опухолями MSI -H, что можно увидеть при синдроме Линча. Пятно H&E . | |
| Специальность |
Онкология |
Наследственный неполипозный колоректальный рак ( HNPCC ) или синдром Линча - это аутосомно-доминантное генетическое заболевание, которое связано с высоким риском рака толстой кишки, а также других видов рака, включая рак эндометрия (второй по частоте), яичников , желудка , тонкой кишки , гепатобилиарного тракта , верхние мочевыводящие пути , мозг и кожа . Повышенный риск этих видов рака связан с наследственными мутациями, которые нарушают репарацию несоответствия ДНК . Это разновидность онкологического синдрома . Поскольку у пациентов с синдромом Линча могут быть полипы, термин HNPCC вышел из моды.
Признаки и симптомы
Риск рака
Пожизненный риск и средний возраст на момент постановки диагноза рака, связанного с синдромом Линча
| Тип рака | Пожизненный риск (%) | Средний возраст на момент постановки диагноза (лет) |
| Колоректальный | 52-58 | 44-61 |
| Эндометрия | 25-60 | 48-62 |
| Желудочный | 6-13 | 56 |
| Яичников | 4–12 | 42,5 |
Понятно, что помимо типов рака, представленных в таблице выше, синдром Линча также способствует повышенному риску рака тонкой кишки, рака поджелудочной железы , рака мочеточника / почечной лоханки, рака желчных путей, рака мозга и новообразований сальных желез . Повышенный риск развития рака простаты и рака молочной железы был также связан с синдромом Линча, хотя эта связь не совсем понял.
Две трети случаев рака толстой кишки возникают в проксимальном отделе толстой кишки, и общие признаки и симптомы включают кровь в стуле, диарею или запор , а также непреднамеренную потерю веса . Средний возраст диагноза колоректального рака составляет 44 года для членов семей, соответствующих критериям Амстердама. Средний возраст диагностирования рака эндометрия составляет около 46 лет. Среди женщин с HNPCC, у которых есть рак толстой кишки и эндометрия, около половины впервые заболевают раком эндометрия , что делает рак эндометрия наиболее распространенным дозорным раком при синдроме Линча. Самый частый симптом рака эндометрия - аномальное вагинальное кровотечение. При HNPCC средний возраст диагноза рака желудка составляет 56 лет, причем аденокарцинома кишечного типа является наиболее часто встречающейся патологией. HNPCC-ассоциированный рак яичников диагностируется в среднем 42,5 года; примерно 30% диагностируются до 40 лет.
Были обнаружены значительные различия в частоте рака в зависимости от мутации. До 75 лет риски колоректального рака, рака эндометрия, рака яичников , верхних отделов желудочно-кишечного тракта (желудка, двенадцатиперстной кишки, желчных протоков или поджелудочной железы), рака мочевыводящих путей, рака предстательной железы и опухолей головного мозга были следующими: для мутаций MLH1 риск было - 46%, 43%, 10%, 21%, 8%, 17% и 1% соответственно: для мутаций MSH2 риски составляли 57%, 17%, 10%, 25%, 32% и 5% соответственно: для мутаций MSH6 риски составляли 15%, 46%, 13%, 7%, 11%, 18% и 1% соответственно.
| Ген | Риск рака яичников | Риск рака эндометрия |
|---|---|---|
| MLH1 | 4-24% | 25-60% |
| MSH2 / EPCAM | 4-24% | 25-60% |
| MSH6 | 1-11% | 16–26% |
| PMS2 | 6% (комбинированный риск) | 15% |
Генетика
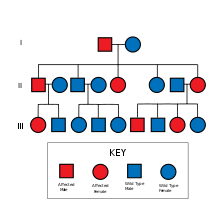
HNPCC наследуется по аутосомно-доминантному типу. Отличительной чертой HNPCC является дефектная репарация несоответствия ДНК , которая вызывает повышенную скорость однонуклеотидных изменений и микросателлитную нестабильность , также известную как MSI-H (H - «высокий»). MSI идентифицируется в образцах рака в лаборатории патологии . В большинстве случаев приводят к изменению длин динуклеотидных повторов этих нуклеотидных цитозин и аденин (последовательность: CACACACACA ...).
Четыре основных гена, участвующих в HNPCC, обычно кодируют белки, которые образуют димеры для функционирования:
- Белок MLH1 димеризуется с белком PMS2 с образованием MutLα, который координирует связывание других белков, участвующих в репарации ошибочного спаривания, таких как ДНК-геликаза , одноцепочечный ДНК-связывающий белок (RPA) и ДНК-полимеразы .
- Белок MSH2 димеризуется с белком MSH6, который определяет несовпадения с помощью модели скользящего зажима , белка для сканирования на наличие ошибок.
Нарушение любого гена димера белка нарушает функцию белка. Эти 4 гена участвуют в исправлении ошибок (исправлении несоответствия), поэтому дисфункция генов может привести к неспособности исправить ошибки репликации ДНК и вызвать HNPCC. Известно, что HNPCC связан с другими мутациями в генах, участвующих в пути репарации ошибочного спаривания ДНК :
| Имя OMIM | Гены, участвующие в HNPCC | Частота мутаций в семьях HNPCC | Locus | Первая публикация |
|---|---|---|---|---|
| HNPCC1 ( 120435 ) | MSH2 / EPCAM | примерно 60% | 2p22 | Фишель 1993 |
| HNPCC2 ( 609310 ) | MLH1 | примерно 30% | 3п21 | Пападопулос 1994 |
| HNPCC5 | MSH6 | 7-10% | 2п16 | Мияки 1997 |
| HNPCC4 | PMS2 | относительно нечасто | 7p22 | Николаидес 1994 |
| HNPCC3 | PMS1 | история болезни | 2q31-q33 | Николаидес 1994 |
| HNPCC6 | TGFBR2 | история болезни | 3p22 | |
| HNPCC7 | MLH3 | оспаривается | 14q24.3 |
Люди с мутациями MSH6 с большей вероятностью будут отрицательными по Амстердамскому критерию II. Представление с MSH6 немного отличается от MLH1 и MSH2, и термин «синдром MSH6» был использован для описания этого состояния. В одном исследовании руководящие принципы Bethesda были более чувствительны, чем критерии Амстердама при его обнаружении.
До 39% семей с мутациями в гене HNPCC не соответствуют критериям Амстердама . Следовательно, семьи, в которых обнаружена вредная мутация в гене HNPCC, следует рассматривать как имеющие HNPCC независимо от степени семейного анамнеза. Это также означает, что критерии Амстердама не позволяют выявить многих людей, подверженных риску синдрома Линча. Улучшение критериев для скрининга - активная область исследований, как подробно описано в разделе «Стратегии скрининга» этой статьи.
Большинство людей с HNPCC наследуют заболевание от родителей. Однако из-за неполной пенетрантности, различного возраста диагноза рака, снижения риска рака или ранней смерти не у всех людей с мутацией гена HNPCC есть родитель, который болел раком. У некоторых людей HNPCC развивается de novo в новом поколении, не унаследовав гена. Этих людей часто выявляют только после развития рака толстой кишки в раннем возрасте. Вероятность передачи генетической мутации каждому ребенку у родителей с HNPCC составляет 50%. Также важно отметить, что вредной мутации в одном из генов MMR недостаточно, чтобы вызвать рак, но скорее должны произойти дальнейшие мутации в других генах-супрессорах опухоли.
Диагностика
Диагноз синдрома Линча применяется к людям с мутацией ДНК зародышевой линии в одном из генов MMR (MLH1, MSH2, MSH6 и PMS2) или гене EPCAM, идентифицированном с помощью генетического тестирования. Кандидатов на генетическое тестирование зародышевой линии можно определить по клиническим критериям, таким как Амстердамские клинические критерии и рекомендации Bethesda, или с помощью анализа опухолей с помощью иммуногистохимии (IHC) или тестирования микросателлитной нестабильности (MSI). В США профессиональные сообщества рекомендуют проверять каждый рак толстой кишки на MSI или IHC в качестве скрининга на синдром Линча, но это не всегда выполняется из-за ограничений стоимости и ресурсов. Генетическое тестирование доступно в продаже и состоит из анализа крови.
Иммуногистохимия
Иммуногистохимия (ИГХ) - это метод, который можно использовать для обнаружения аномальной экспрессии белка восстановления несоответствия (MMR) в опухолях, связанных с синдромом Линча. Хотя это не является диагностикой синдрома Линча, оно может сыграть роль в выявлении людей, которым следует пройти тестирование на зародышевые линии. Два метода внедрения тестирования IHC включают возрастное тестирование и универсальное тестирование для всех людей. В настоящее время нет широкого согласия относительно того, какой метод скрининга следует использовать. Возрастное тестирование для IHC было предложено отчасти из-за анализа затрат и выгод, тогда как универсальное тестирование для всех людей с колоректальным раком гарантирует, что люди с синдромом Линча не будут пропущены. Чтобы снизить затраты, исследователи пытаются предсказать MSI или IHC непосредственно по тому, как опухоль выглядит под микроскопом, без каких-либо молекулярных тестов.
Нестабильность микроспутников
Мутации в системах репарации несоответствия ДНК могут привести к затруднениям с передачей участков внутри ДНК, которые содержат повторяющиеся образцы из двух или трех нуклеотидов ( микросателлиты ), иначе известные как микросателлитная нестабильность ( MSI ). MSI идентифицируется путем выделения ДНК как из образца опухолевой ткани, так и из образца нормальной ткани с последующим ПЦР- анализом микросателлитных областей. Анализ MSI можно использовать для выявления людей, у которых может быть синдром Линча, и направления их для дальнейшего тестирования.
Классификация
По гистопатологическим критериям можно выделить три основные группы рака MSI-H ( микросателлитная нестабильность - MSI):
- правосторонние низкодифференцированные раковые образования
- правосторонний муцинозный рак
- аденокарциномы в любом месте, показывающие любой измеримый уровень интраэпителиальных лимфоцитов (TIL)
Гистопатологические критерии недостаточно чувствительны для обнаружения MSI по гистологии, но исследователи пытаются использовать искусственный интеллект для прогнозирования MSI по гистологии.
Кроме того, HNPCC можно разделить на синдром Линча I (семейный рак толстой кишки) и синдром Линча II (HNPCC, связанный с другими видами рака желудочно-кишечного тракта или репродуктивной системы ).
Профилактика
После сообщения о нулевом результате их рандомизированного контролируемого исследования аспирина (ацетилсалициловой кислоты - ASA) для предотвращения колоректальной неоплазии синдрома Линча, Берн и его коллеги сообщили новые данные, представляющие более длительный период наблюдения, чем сообщалось в первоначальной статье NEJM . Эти новые данные демонстрируют снижение заболеваемости у людей с синдромом Линча, которые принимали высокие дозы аспирина не менее четырех лет, с удовлетворительным профилем риска. Эти результаты широко освещались в СМИ; будущие исследования будут направлены на изменение (снижение) дозы (для снижения риска, связанного с высокой дозировкой АСК).
Скрининг
Для семей, соответствующих Амстердамским критериям, рекомендуется генетическое консультирование и генетическое тестирование, желательно до начала рака толстой кишки.
Рак толстой кишки
Колоноскопия рекомендуется в качестве профилактического метода наблюдения для людей с синдромом Линча или LS-ассоциированными генами. В частности, рекомендуется начинать колоноскопию в возрасте 20–25 лет для носителей мутаций MLH1 и MSH2 и в 35 лет для носителей мутаций MSH6 и PMS2. Затем следует проводить колоноскопическое наблюдение за пациентами с синдромом Линча с интервалом 1-2 года.
Рак эндометрия / яичников
Трансвагинального УЗИ с или без биопсии эндометрия ежегодно рекомендуется для яичников и эндометрия скрининга рака. Для женщин с синдромом Линча ежегодный анализ крови на CA-125 может использоваться для скрининга рака яичников, однако данные об эффективности этого теста в снижении смертности ограничены.
Другие виды рака
Существуют также стратегии раннего обнаружения других видов рака или снижения шансов их развития, которые люди с синдромом Линча могут обсудить со своим врачом, однако их эффективность не ясна. Эти варианты включают:
- Эндоскопия верхних отделов кишечника для выявления рака желудка и тонкой кишки каждые 3-5 лет, начиная с 30-летнего возраста (желательно в исследовательских условиях)
- Ежегодный анализ мочи для выявления рака мочевого пузыря не ранее 30 лет (желательно в исследовательских условиях)
- Ежегодные физические и неврологические обследования для выявления рака центральной нервной системы ( головного или спинного мозга), начиная с 25-летнего возраста.
Критерии Амстердама
Ниже приведены критерии Амстердама для выявления кандидатов высокого риска для молекулярно-генетического тестирования:
Критерии Амстердама I (должны быть выполнены все пункты списка): Критерии Амстердама I были опубликованы в 1990 году; однако считались недостаточно чувствительными.
- Три или более члена семьи с подтвержденным диагнозом колоректального рака, один из которых является родственником первой степени (родитель, ребенок, брат или сестра) двух других
- Два последовательных поколения пострадавших
- Один или несколько видов рака толстой кишки диагностированы в возрасте до 50 лет.
- Семейный аденоматозный полипоз (FAP) исключен.
Критерии Амстердама II были разработаны в 1999 году и улучшили диагностическую чувствительность синдрома Линча за счет включения рака эндометрия , тонкой кишки, мочеточника и почечной лоханки.
Амстердамские критерии II (должны быть выполнены все пункты списка):
- Три или более члена семьи с раком, связанным с HNPCC, один из которых является родственником первой степени родства двух других.
- Два последовательных поколения пострадавших
- Один или несколько видов рака, связанных с HNPCC, диагностированных в возрасте до 50 лет.
- Семейный аденоматозный полипоз (FAP) исключен.
Критерии Bethesda были разработаны в 1997 году и позже обновлены в 2004 году Национальным институтом рака для выявления лиц, которым требуется дальнейшее тестирование на синдром Линча через MSI. В отличие от Амстердамских критериев, пересмотренные рекомендации Bethesda используют патологические данные в дополнение к клинической информации, чтобы помочь поставщикам медицинских услуг выявлять лиц с высоким риском.
Пересмотренные правила Bethesda
Если человек соответствует одному из пяти критериев, опухоль (опухоли) человека должна быть проверена на MSI:
1. Колоректальный рак диагностирован до 50 лет.
2. Наличие синхронного или метахронного колоректального или другого рака, связанного с синдромом Линча (например, рак эндометрия, яичников, желудка, тонкой кишки, поджелудочной железы, желчных путей, мочеточника, почечной лоханки, мозга, сальных желез, кератоакантомы )
3. Колоректальный рак с патологией MSI-high у человека моложе 60 лет.
4. Колоректальный рак, диагностированный у человека с одним или несколькими родственниками первой степени родства с колоректальным раком или опухолью, ассоциированной с синдромом Линча, диагностированной в возрасте до 50 лет.
5. Человек с колоректальным раком и два или более родственника первой или второй степени родства с колоректальным раком или раком, ассоциированным с синдромом Линча, диагностированный в любом возрасте.
Важно отметить, что эти клинические критерии могут быть трудными для использования на практике, а используемые сами по себе клинические критерии пропускают от 12 до 68 процентов случаев синдрома Линча.
Операция
Профилактическая гистерэктомия и сальпингоофорэктомия (удаление матки , маточных труб и яичников для предотвращения развития рака) могут быть выполнены до того, как разовьется рак яичников или эндометрия.
Уход
Хирургия остается передовой терапией HNPCC. Пациентам с синдромом Линча, у которых развивается колоректальный рак, можно лечить либо частичную колэктомию, либо полную колэктомию с илеоректальным анастомозом. Из-за повышенного риска колоректального рака после частичной колэктомии и аналогичного качества жизни после обеих операций полная колэктомия может быть предпочтительным методом лечения HNPCC, особенно у молодых пациентов.
Продолжаются споры о пользе адъювантной терапии на основе 5-фторурацила для колоректальных опухолей, связанных с HNPCC, особенно на стадиях I и II.
- Терапия антителами против PD-1 может быть эффективной.
Блокада контрольной точки с терапией анти-PD-1 в настоящее время является предпочтительной терапией первой линии для поздней стадии микросателлитной нестабильности - высокого колоректального рака.
Эпидемиология
Хотя точная распространенность мутаций, вызывающих синдром Линча, в общей популяции остается неизвестной, недавние исследования оценивают распространенность как 1 на 279 человек, или 0,35%. Известно, что некоторые группы населения имеют более высокую распространенность мутаций-основателей, включая, помимо прочего, франко-канадцев , исландцев , афроамериканцев и евреев-ашкенази . Мутации, вызывающие синдром Линча, обнаруживаются примерно в 3% всех диагностированных колоректальных опухолей и в 1,8% всех диагностированных злокачественных новообразований эндометрия. Средний возраст диагноза рака у пациентов с этим синдромом составляет 44 года по сравнению с 64 годами у людей без синдрома.
Терминология
Генри Т. Линч , профессор медицины Медицинского центра Университета Крейтон , охарактеризовал этот синдром в 1966 году. В своей более ранней работе он описал заболевание как «семейный синдром рака». Термин «синдром Линча» был придуман в 1984 году другими авторами; Линч назвал это состояние HNPCC в 1985 году. С тех пор эти два термина использовались взаимозаменяемо, пока более поздние достижения в понимании генетики заболевания не привели к тому, что термин HNPCC потерял популярность.
Другие источники оставляют за собой термин «синдром Линча», когда имеется известный дефект репарации рассогласования ДНК , и используют термин «семейный колоректальный рак типа X», когда соблюдаются критерии Амстердама , но нет известного дефекта репарации рассогласования ДНК. Предполагаемые семьи «типа X», по-видимому, имеют более низкую общую заболеваемость раком и более низкий риск неколоректального рака, чем семьи с задокументированным дефицитом репарации несоответствия ДНК. Около 35% людей, отвечающих критериям Амстердама, не имеют мутации гена восстановления несоответствия ДНК.
Ситуацию усложняет наличие альтернативного набора критериев, известного как «Рекомендации Bethesda».
Общество
Информацию и поддержку предоставляет ряд некоммерческих организаций, в том числе Lynch Syndrome International , AliveAndKickn , Lynch Syndrome UK и Bowel Cancer UK. В США 22 марта отмечается Национальный день осведомленности о синдроме Линча.
использованная литература
дальнейшее чтение
Книги
- Маккей, Ами (2019). Дочь Семьи Г.: воспоминания о генах рака, любви и судьбе . Торонто: Альфред А. Кнопф, Канада. ISBN 978-0-345-80946-9. OCLC 1089450897 . Версия в мягкой обложке под новым названием «До моего времени».
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |
