Идиопатическая мультицентрическая болезнь Кастлемана - Idiopathic multicentric Castleman disease
| Идиопатическая мультицентрическая болезнь Кастлемана | |
|---|---|
| Другие названия | Гиперплазия гигантских лимфатических узлов, лимфоидная гамартома, гиперплазия ангиофолликулярных лимфатических узлов |
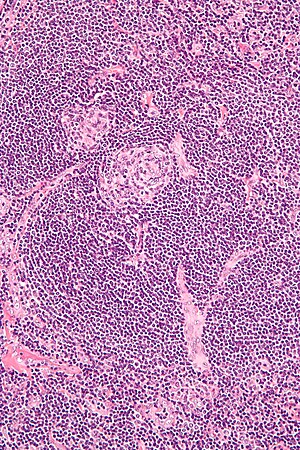 | |
| Микрофотография биопсии лимфатического узла, демонстрирующая свойства гиалиновых сосудов, соответствующие болезни Кастлемана. | |
| Специальность | Гематология, иммунология, ревматология, патология |
| Диагностический метод | На основании истории болезни пациента, физического осмотра, лабораторных исследований, медицинских изображений, гистопатологии |
| Частота | примерно 1500-1800 новых случаев в США |
Идиопатическая мультицентрическая болезнь Кастлемана (iMCD) является подтипом болезни Кастлемана (также известной как гиперплазия гигантских лимфатических узлов , лимфоидная гамартома или гиперплазия ангиофолликулярных лимфатических узлов ), группы лимфопролиферативных заболеваний, характеризующихся увеличением лимфатических узлов , характерными признаками при микроскопическом анализе увеличенного ткань лимфатического узла, а также ряд симптомов и клинических проявлений.
Люди с iMCD имеют увеличенные лимфатические узлы во многих регионах и часто имеют симптомы, похожие на грипп, аномальные результаты анализов крови и дисфункцию жизненно важных органов, таких как печень, почки и костный мозг.
iMCD имеет особенности, часто встречающиеся при аутоиммунных заболеваниях и раках, но механизм основного заболевания неизвестен. Лечение iMCD может включать использование различных лекарств, включая иммунодепрессанты и химиотерапию.
Болезнь Кастлмана была названа в честь доктора Бенджамина Кастлмана , который впервые описал это заболевание в 1956 году. Сеть сотрудничества по борьбе с болезнью Кастлмана - крупнейшая организация, занимающаяся этим заболеванием, которая занимается исследованиями, повышением осведомленности и поддержкой пациентов.
Признаки и симптомы
Пациенты с iMCD могут испытывать увеличение лимфатических узлов в нескольких областях лимфатических узлов; системные симптомы (жар, ночная потливость, непреднамеренное похудание, быстрая утомляемость); увеличение печени и / или селезенки ; накопление внесосудистой жидкости в конечностях ( отек ), брюшной полости ( асцит ) или слизистой оболочке легких ( плевральный выпот ); легочные симптомы, такие как кашель и одышка; и кожные проявления, такие как вишневые гемангиомы .
Причины
Причина iMCD неизвестна, и факторы риска не выявлены. Генетические варианты наблюдались в случаях болезни Кастлемана; однако ни один генетический вариант не был подтвержден как вызывающий заболевание.
В отличие от MCD , ассоциированного с HHV-8 , iMCD не вызывается неконтролируемой инфекцией HHV-8.
Механизм
Механизм заболевания iMCD полностью не описан. Известно, что интерлейкин-6 (IL-6) , молекула, которая стимулирует иммунные клетки, играет роль в некоторых случаях iMCD. Уровни IL-6, измеренные у некоторых пациентов с iMCD, увеличиваются и уменьшаются с соответствующими изменениями активности заболевания, у мышей, получавших IL-6, развиваются черты iMCD, а блокада пути IL-6 с использованием препаратов силтуксимаб и тоцилизумаб эффективно лечит некоторых пациентов с iMCD. Однако у многих пациентов с iMCD не наблюдается повышенных уровней IL-6, а уровни IL-6 не сильно коррелируют с ответом на лечение препаратами против IL-6. В случаях, когда IL-6 действительно играет роль, основная причина повышенных уровней IL-6 и клетки, ответственные за производство IL-6, остаются неизвестными.
Несколько теоретических механизмов для iMCD были предложены на основе существующих исследований и наблюдаемых сходств между iMCD и другими заболеваниями, которые имеют сходные клинические данные и гистологию лимфатических узлов:
- Аутоиммунный - иммунная система может вырабатывать антитела, которые нацелены на здоровые клетки организма, а не на бактерии и вирусы. Самонаправленные антитела обычно наблюдаются при аутоиммунных заболеваниях, таких как системная красная волчанка и ревматоидный артрит .
- Аутовоспалительный - мутация в гене, контролирующем воспалительные системы, может способствовать пагубной активации воспалительных путей у пациентов с iMCD.
- Неопластические - генетические мутации, которые развиваются в зрелых клетках ( соматические мутации), могут вызывать чрезмерный рост аномальных клеток, как при раке, таком как лимфома .
- Возбудитель. Вирус герпеса человека 8 (HHV-8) является известным возбудителем MCD, ассоциированного с HHV-8, который имеет симптомы и симптомы, очень похожие на iMCD. Хотя iMCD по определению не вызывается HHV-8, заболевание может вызывать неизвестный вирус.
О случаях преобразования UCD в iMCD не сообщалось.
Диагностика
iMCD диагностируется в соответствии с согласованными диагностическими критериями, основанными на доказательствах, которые требуют тщательной оценки, включая анамнез пациента , физический осмотр , лабораторные исследования , рентгенологическое изображение и микроскопический анализ (гистологию) биопсии ткани увеличенного лимфатического узла. Диагностика iMCD требует клинических отклонений, исключения других заболеваний и биопсии лимфатических узлов, показывающей признаки, соответствующие болезни Кастлемана. Одной биопсии лимфатического узла недостаточно для постановки диагноза.
Лабораторные испытания
Лабораторные исследования могут продемонстрировать повышенный С-реактивный белок , пониженный уровень гемоглобина ( анемия ), низкий уровень альбумина , повышенный креатинин , повышенный уровень иммуноглобулина и аномальное (повышенное или пониженное) количество тромбоцитов . У пациентов также может быть повышенное содержание молекул, участвующих в воспалении ( цитокинов ), таких как интерлейкин 6 (IL-6) и фактор роста эндотелия сосудов (VEGF) .
Медицинская визуализация
Радиологическая визуализация продемонстрирует увеличенные лимфатические узлы во многих областях, которые, как правило, являются 18F-фтордоксиглюкозой (FDG) на позитронно-эмиссионной томографии (ПЭТ) .
Сопутствующие заболевания
iMCD обычно наблюдается у пациентов с синдромом POEMS, но неясно, возникает ли iMCD как независимый болезненный процесс или как проявление синдрома POEMS у этих пациентов. Пациенты с iMCD имеют повышенный риск солидных опухолей и рака крови. Иногда у пациентов с iMCD развивается лимфоцитарный интерстициальный пневмонит .
Синдром ТАФРО
IMCD пациентов с т hrombocytopenia, nasarca, myelo х ibrosis, г еналь дисфункции, а также о rganomegaly синдрома (синдром TAFRO) считается имеющим ярко выраженным клиническим подтипом IMCD. У пациентов часто наблюдается быстрое прогрессирование симптомов и часто развивается тяжелая органная дисфункция. По сравнению с пациентами iMCD без синдрома TAFRO, пациенты iMCD с синдромом TAFRO с большей вероятностью будут иметь сильную боль в животе, низкий уровень тромбоцитов, прогрессирующую почечную дисфункцию и нормальный или слегка повышенный уровень иммуноглобулинов. Хотя iMCD с синдромом TAFRO был впервые описан у японских пациентов в 2010 году, случаи iMCD с синдромом TAFRO с тех пор были зарегистрированы у неяпонских пациентов во многих других странах.
Классификация
Болезнь Кастлемана описывает группу, по крайней мере, из 3 различных заболеваний - уникентрическую болезнь Кастлемана (UCD), мультицентрическую болезнь Кастлмана, связанную с вирусом герпеса 8 (HHV-8-ассоциированную MCD), и идиопатическую многоцентровую болезнь Кастлемана (iMCD) . Определение правильного подтипа заболевания важно, так как три расстройства значительно различаются по симптомам, клиническим данным, механизму заболевания, подходу к лечению и прогнозу.
- При уникентрической болезни Кастлемана увеличенные лимфатические узлы с характерными микроскопическими находками присутствуют только в одной области лимфатических узлов.
- При мультицентрических подтипах болезни Кастлемана увеличенные лимфатические узлы с характерными признаками присутствуют в нескольких областях лимфатических узлов. Мультицентрические варианты болезни Кастлемана далее классифицируются по известным причинам заболевания.
- MCD, ассоциированный с HHV-8, вызывается неконтролируемым инфицированием вирусом герпеса 8 человека (HHV-8).
- При идиопатической многоцентровой болезни Кастлемана (iMCD) причина заболевания неизвестна ( идиопатическая ). Для диагностики iMCD тестирование на HHV-8 должно быть отрицательным.
Идиопатическая мультицентрическая болезнь Кастлемана
IMCD может быть дополнительно дифференцируются наличием сопутствующих заболеваний, таких как р olyneuropathy, о rganomegaly, е ndocrinopathy, м onoclonal белка, с родственниками изменяет синдром (синдром POEMS), или с помощью различных клинических признаков, таких как т hrombocytopenia, nasarca, myelo е ibrosis, г еналя дисфункции, а также о rganomegaly синдром (синдром TAFRO).
Диагностические критерии
Диагностика iMCD требует: наличия обоих основных критериев, множественных областей увеличенных лимфатических узлов, что подтверждается медицинской визуализацией; наличие как минимум двух второстепенных критериев, хотя бы одним из которых должен быть отклоненный от нормы лабораторный тест; и исключение болезней, которые могут имитировать iMCD.
Основной критерий 1: несколько областей увеличенных лимфатических узлов.
Радиологическое изображение должно продемонстрировать увеличенные лимфатические узлы во многих регионах.
Основной критерий 2: микроскопический анализ биопсии лимфатических узлов в соответствии с iMCD
Микроскопический вид (гистология) биопсии увеличенного лимфатического узла должен демонстрировать совокупность признаков, соответствующих болезни Кастлемана. Существует три модели характерных гистологических особенностей, связанных с iMCD:
- Гиперсосудистые - регрессивные зародышевые центры , выступающие фолликулярные дендритные клетки , гиперваскуляризация в межфолликулярных областях и выступающие зоны мантии, напоминающие кожу лука.
- Плазмоцитоз - увеличение количества фолликулов с большими гиперпластическими зародышевыми центрами и пластинчатым плазмоцитозом (увеличение количества плазматических клеток ).
- Смешанный - признаки как гиперваскулярного, так и плазмоцитарного.
iMCD чаще всего демонстрирует плазмоцитарные свойства; однако гиперваскулярные особенности или сочетание гиперваскулярных и плазмоцитарных признаков также могут наблюдаться в лимфатических узлах iMCD. Клиническая полезность подтипов iMCD по гистологическим признакам неясна, поскольку гистологические подтипы не позволяют однозначно прогнозировать тяжесть заболевания или ответ на лечение.
Окрашивание ядерным антигеном, связанным с латентностью (LANA-1) , маркером инфекции HHV-8, должно быть отрицательным для диагностики iMCD.
Второстепенные критерии
Пациенты должны соответствовать как минимум двум из следующих 11 второстепенных критериев, по крайней мере, один из которых является ненормальным лабораторным тестом.
Лабораторные тесты:
- Повышенная скорость оседания С-реактивного белка или эритроцитов
- Низкий уровень гемоглобина (анемия)
- Аномальное (низкое или высокое) количество тромбоцитов
- Низкий уровень альбумина
- Повышенный креатинин
- Повышенный уровень иммуноглобулинов (гипергаммаглобулинемия)
Клинические признаки:
- Гриппоподобные симптомы
- Увеличение печени и / или селезенки
- Скопление жидкости (отек, асцит, плевральный выпот)
- Находки на коже, такие как вишневые гемангиомы или фиолетовые папулы.
- Лимфоцитарный интерстициальный пневмонит
Заболевания, которые следует исключить
Диагностика требует исключения заболеваний, которые могут проявляться схожими клиническими проявлениями и внешними проявлениями при микроскопическом анализе ткани увеличенного лимфатического узла. Заболевания, которые необходимо исключить при диагностике iMCD, включают инфекционные заболевания, такие как MCD , ассоциированный с HHV-8 , мононуклеоз вируса Эпштейна-Барра и реактивная лимфаденопатия ; аутоиммунные заболевания, такие как системная красная волчанка и ревматоидный артрит ; и раковые заболевания, включая лимфому , множественную миелому и плазмоцитому первичных лимфатических узлов .
Уход
Из-за редкости iMCD данные о лечении ограничены и основаны на комбинации наблюдательных серий случаев, историй болезни и одного рандомизированного клинического исследования. В отличие от UCD, при котором хирургическое вмешательство является методом выбора и лечением для большинства пациентов, операция при iMCD неэффективна. Вместо хирургического лечения используются различные лекарства в зависимости от тяжести заболевания и реакции пациента на предшествующее лечение. Силтуксимаб , моноклональное антитело, нацеленное на IL-6 , является единственным лекарством, одобренным Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для лечения iMCD; однако в литературе сообщалось об успешном использовании других лекарств.
В 2018 году международная группа экспертов в этой области опубликовала первые согласованные рекомендации по лечению iMCD, основанные на доказательствах. В дополнение к созданию алгоритма лечения iMCD, эти руководящие принципы лечения установили общие определения тяжести заболевания и реакции на лечение.
Оценка степени серьезности iMCD
Пациенты с iMCD классифицируются как имеющие тяжелое или нетяжелое заболевание на основании 5 критериев, перечисленных ниже. Пациенты с 2 или более критериями ниже классифицируются как имеющие тяжелое заболевание, тогда как пациенты с критериями 0-1 классифицируются как имеющие нетяжелое заболевание.
- Статус работы Восточной совместной онкологической группы (ECOG) ≥ 2
- Расчетная скорость клубочковой фильтрации (рСКФ) <30 или креатинин> 3,0 мг / дл
- Анасарка и / или асцит, и / или плевральный выпот, и / или перикардиальный выпот
- Гемоглобин ≤ 8,0 г / дл
- Поражение легких (например, интерстициальный пневмонит с одышкой)
Ответ на лечение
Пациенты с iMCD оцениваются на предмет ответа на лечение на основе изменений симптомов, размеров пораженных лимфатических узлов и лабораторных исследований. Каждая категория оценивается как полный ответ, частичный ответ, стабильное заболевание или прогрессирующее заболевание. Общий ответ на лечение определяется оценкой самой низкой категории. Например, пациенту с полным лабораторным ответом, частичным ответом симптомов и полным ответом лимфатических узлов будет дан общий ответ на лечение или частичный ответ. См. Ниже описание критериев и оценки ответов.
Лабораторные испытания
Лабораторные тесты включают все следующее: С-реактивный белок, гемоглобин, альбумин и рСКФ.
- Полный ответ - все лабораторные значения в пределах нормы
- Частичный ответ -> 50% по всем лабораторным значениям
- Стабильное заболевание - все лабораторные показатели от <50% улучшения до <25% ухудшения
- Прогрессирующее заболевание - ухудшение на 25% при любом лабораторном значении
Симптомы
Четыре симптома оцениваются с использованием общих терминологических критериев нежелательных явлений Национального института рака (версия 4): утомляемость, анорексия, лихорадка и масса тела.
- Полный ответ - нормализация до исходного уровня до заболевания
- Частичный ответ - улучшение всех 4 симптомов, но не до исходного уровня до заболевания
- Устойчивое заболевание - улучшение как минимум 1 (но не всех) симптомов
- Прогрессирующее заболевание - ухудшение по крайней мере 1 симптома по 2 или более оценкам.
Лимфатический узел
Ответ на лечение лимфатических узлов оценивается с помощью радиологической визуализации и классифицируется как полный ответ, частичный ответ, стабильное заболевание и прогрессирующее заболевание на основе модифицированных критериев Чесона.
Алгоритм лечения
Алгоритм лечения iMCD основан в первую очередь на тяжести заболевания и реакции на лечение. Из-за высокой частоты рецидивов после прекращения лечения большинство пациентов с iMCD лечатся лекарствами на неопределенный срок.
Нетяжелое заболевание
Силтуксимаб, блокатор ИЛ-6, рекомендуется для лечения всех пациентов с нетяжелой ИМК, независимо от измеренных уровней ИЛ-6. Тоцилизумаб , препарат, который также нацелен на путь IL-6, обычно используется в качестве альтернативы силтуксимабу, когда силтуксимаб недоступен. Кортикостероиды могут быть добавлены к терапии анти-IL-6 в зависимости от клинических проявлений. Ритуксимаб , препарат, нацеленный на В-клетки, в первую очередь рекомендуется в качестве терапии второй линии для пациентов, которые не реагируют на силтуксимаб или тоцилизумаб, но может использоваться в качестве средства первой линии у соответствующих пациентов.
Рекомендации по лечению для пациентов с нетяжелым течением заболевания, которые не реагируют на силтуксимаб, тоцилизумаб и ритуксимаб, четко не определены. Сообщалось, что цитотоксическая химиотерапия вызывает ремиссию у пациентов с нетяжелым iMCD; однако использование цитотоксической химиотерапии в настоящее время не рекомендуется при нетяжелой iMCD из-за высокой вероятности рецидива и профилей тяжелых побочных эффектов. В качестве альтернативы рекомендуются иммуномодуляторы, такие как талидомид, циклоспорин А, сиролимус, бортезомиб и анакинра из-за их сходной скорости ответа и более благоприятных профилей долгосрочных побочных эффектов.
Тяжелое заболевание
Рекомендуемое начальное лечение для всех пациентов с тяжелым iMCD - высокие дозы стероидов в сочетании с анти-IL-6 агентом, таким как силтуксимаб или тоцилизумаб, независимо от измеренных уровней IL-6. Пациентам, у которых сразу же улучшилось состояние при этой схеме, можно постепенно снижать дозу стероидов, но прием анти-IL-6 следует продолжать бесконечно из-за высокой частоты рецидивов после отмены лечения. Из-за высокого риска осложнений, связанных с тяжелым iMCD, если состояние пациента ухудшается или не улучшается при лечении высокими дозами стероидов и анти-IL-6 терапии, рекомендуются режимы цитотоксической химиотерапии. Пациентам с опасным для жизни заболеванием, особенно с синдромом TAFRO, могут потребоваться расширенные меры, такие как поддержка дыхания с помощью аппарата искусственной вентиляции легких или лечение диализом при почечной недостаточности.
После улучшения статуса заболевания поддерживающая терапия препаратом против IL-6 или иммунодепрессантом обычно продолжается бесконечно, поскольку отмена таких препаратов может привести к рецидиву.
Следовать за
Пациентам с iMCD требуется рутинная оценка ответа на лечение и прогрессирования заболевания. Рекомендуется, чтобы последующие посещения включали оценку симптомов, физический осмотр, лабораторные исследования и рентгенологическое обследование.
Прогноз
iMCD может проявляться как острое опасное для жизни заболевание у одних пациентов или хроническое заболевание у других. Некоторые пациенты имеют длительно стабильное заболевание, в то время как другие страдают обострениями тяжелого заболевания, которые могут улучшиться при лечении. Успешное лечение контролирует симптомы и дисфункцию органов, связанных с iMCD, улучшает симптомы и дисфункцию органов во время обострения болезни и предотвращает обострения болезни в будущем.
Наблюдаемая выживаемость в недавнем исследовании пациентов с iMCD составила 92% через 2 года, 76% через 5 лет и 59% через 10 лет.
Эпидемиология
Ежегодно в Соединенных Штатах выявляется примерно 1500-1800 новых случаев iMCD. iMCD может возникнуть в любом возрасте, но средний возраст при обращении составляет приблизительно 50 лет. Заболеваемость iMCD у женщин несколько выше.
Опубликованных эпидемиологических исследований болезни Кастлемана за пределами США не проводилось; однако опубликованных данных, свидетельствующих о повышении или понижении заболеваемости болезнью Кастлемана в определенных регионах или этнических группах, не имеется.
История
Болезнь Кастлмана была впервые описана доктором Бенджамином Кастлеманом в 1956 году. Всемирный день болезни Кастлмана был учрежден в 2018 году и проводится ежегодно 23 июля.
Культура
Сеть сотрудничества по борьбе с болезнью Кастлмана была основана в 2012 году и является крупнейшей организацией, занимающейся болезнью Кастлмана. Это глобальная сеть сотрудничества, занимающаяся исследованиями, информированием и поддержкой пациентов.
Рекомендации
| Классификация |
|---|
