MT-ATP6 - MT-ATP6
МТ-ATP6 (или ATP6 ) представляет собой митохондриальный геном с полным именем «митохондрией кодированной АТФсинтазы мембрана субъединица 6»которая кодирует АТФ - синтазы Р о субъединице 6 (или субъединица / цепи A) . Эта субъединица принадлежит к комплексу F o большой трансмембранной АТФ-синтазы F-типа. Этот фермент, также известный как комплекс V, отвечает за заключительную стадию окислительного фосфорилирования в цепи переноса электронов . В частности, один сегмент АТФ-синтазы позволяет положительно заряженным ионам , называемым протонами , проходить через специализированную мембрану внутри митохондрий. Другой сегмент фермента использует энергию, создаваемую этим потоком протонов, для преобразования молекулы, называемой аденозиндифосфатом (АДФ), в АТФ . Мутации в гене MT-ATP6 были обнаружены примерно у 10-20 процентов людей с синдромом Ли .
Состав
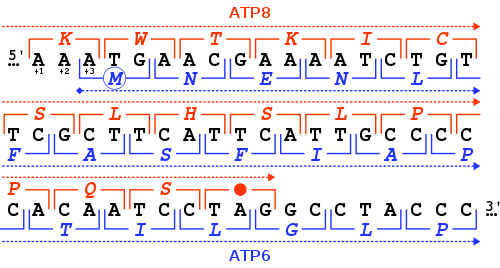
Ген MT-ATP6 предоставляет информацию для создания белка, необходимого для нормальной функции митохондрий. Ген MT-ATP6 человека, расположенный в митохондриальной ДНК , имеет длину 681 пару оснований . Необычной особенностью MT-ATP6 является перекрытие 46- нуклеотидного гена его первых кодонов с концом гена MT-ATP8 . Что касается рамки считывания MT-ATP6 (+3), ген MT-ATP8 заканчивается в рамке считывания +1 стоп-кодоном TAG .
Белок MT-ATP6 весит 24,8 кДа и состоит из 226 аминокислот . Белок является субъединицей F 1 F o АТФазы, также известной как Комплекс V , который состоит из 14 ядерных и 2 митохондриальных субъединиц. Как субъединица A, MT-ATP6 содержится в некаталитической трансмембранной F o части комплекса.
Номенклатура фермента имеет длинную историю. Фракция F 1 получила свое название от термина «Фракция 1», а F o (написанная как нижняя буква «o», а не «ноль») получила свое название от фракции связывания олигомицина , типа природного антибиотика. который способен ингибировать F o- звено АТФ-синтазы. Область F o АТФ-синтазы представляет собой протонную пору, встроенную в митохондриальную мембрану. Он состоит из трех основных субъединиц A, B и C и (у человека) шести дополнительных субъединиц, d , e , f , g , F6 и 8 (или A6L). Трехмерная структура гомолога этой субъединицы E. coli была смоделирована на основании данных электронной микроскопии (цепь M PDB : 1c17 ). Он образует трансмембранный 4-α-пучок.
Функция
Эта субъединица является ключевым компонентом протонного канала и может играть прямую роль в перемещении протонов через мембрану. Катализ в комплексе F 1 зависит от вращения центрального стержня и c-кольца F o , которое, в свою очередь, управляется потоком протонов через мембрану через границу раздела между c-кольцом F 0 и субъединицей A. Периферический стержень связывает субъединицу A с внешней поверхностью домена F 1 и, как полагают, действует как статор, противодействуя тенденции субъединицы A и каталитической части F 1 альфа 3 бета 3 вращаться вместе с центральным вращающимся элементом.
Клиническое значение
Мутации в MT-ATP6 и других генах, влияющих на окислительное фосфорилирование в митохондриях, были связаны с различными нейродегенеративными и сердечно-сосудистыми заболеваниями, включая дефицит митохондриального комплекса V, наследственную оптическую невропатию Лебера (LHON), митохондриальную энцефаломиопатию с инсультоподобными эпизодами ( MELAS ). , синдром Ли и NARP синдром . Большинство клеток организма содержат тысячи митохондрий, каждая из которых имеет одну или несколько копий митохондриальной ДНК . Тяжесть некоторых митохондриальных нарушений связана с процентным содержанием митохондрий в каждой клетке, имеющей определенное генетическое изменение. Люди с синдромом Ли из-за мутации гена MT-ATP6, как правило, имеют очень высокий процент митохондрий с мутацией (от более 90 процентов до 95 процентов). Менее серьезные особенности NARP являются результатом более низкого процента митохондрий с мутацией, обычно от 70 до 90 процентов. Поскольку эти два состояния являются результатом одних и тех же генетических изменений и могут возникать у разных членов одной семьи, исследователи полагают, что они могут представлять собой спектр перекрывающихся признаков вместо двух различных синдромов.
Дефицит митохондриального комплекса V
Митохондриальной комплекс V дефицит дефицит (дефицит) или потерю функции в комплексной V в цепи переноса электронов , которые могут вызвать широкий спектр признаков и симптомов , влияющих на многие органы и системы организма, особенно нервной системы и сердца . Расстройство может быть опасным для жизни в младенчестве или раннем детстве. У больных могут быть проблемы с кормлением, медленный рост, низкий мышечный тонус ( гипотония ), крайняя утомляемость ( вялость ) и задержка в развитии . У них обычно повышается уровень молочной кислоты в крови ( лактоацидоз ), что может вызвать тошноту, рвоту, слабость и учащенное дыхание. Высокий уровень аммиака в крови ( гипераммонемия ) также может возникать у пораженных людей и в некоторых случаях приводить к нарушению функции мозга ( энцефалопатия ) и повреждению других органов. Атаксия , микроцефалия , задержка развития и умственная отсталость наблюдались у пациентов с мутацией сдвига рамки считывания в MT-ATP6. Это вызывает вставку C в положение 8612, что приводит к усеченному белку длиной всего 36 аминокислот и двум однонуклеотидным полиморфизмам T> C в положениях 8610 и 8614, которые приводят к гомополимерному цитозиновому участку.
Еще одна общая черта дефицита митохондриального комплекса V - гипертрофическая кардиомиопатия . Это состояние характеризуется утолщением ( гипертрофией ) сердечной мышцы, что может привести к сердечной недостаточности . Мутация m.8528T> C встречается в перекрывающейся области генов MT-ATP6 и MT-ATP8 и была описана у нескольких пациентов с детской кардиомиопатией. Эта мутация изменяет кодон инициации в MT-ATP6 на треонин, а также заменяет триптофан на аргинин в положении 55 MT-ATP8 . У людей с дефицитом митохондриального комплекса V также могут быть характерные черты лица, в том числе высокий лоб, изогнутые брови, внешние углы глаз, направленные вниз (наклонные глазные щели ), выступающая переносица, низко посаженные уши и т. Д. тонкие губы и маленький подбородок ( микрогнатия ).
Синдром Ли
Известно, что патогенные варианты митохондриального гена MT-ATP6 вызывают мтДНК-ассоциированный синдром Ли , прогрессирующее заболевание головного мозга, которое обычно проявляется в младенчестве или раннем детстве. Больные дети могут испытывать задержку развития , мышечную слабость, проблемы с движением или затрудненное дыхание. Другие варианты, которые, как известно, вызывают синдром Ли, связанный с мтДНК, включают MT-TL1 , MT-TK , MT-TW , MT-TV , MT-ND1 , MT-ND2 , MT-ND3 , MT-ND4 , MT-ND5 , MT-ND6. и MT-CO3 . Нарушения выработки митохондриальной энергии приводят к нейродегенеративным нарушениям, таким как синдром Ли , который характеризуется появлением симптомов в возрасте от 12 месяцев до трех лет. Симптомы часто проявляются после вирусной инфекции и включают двигательные нарушения и периферическую невропатию , а также гипотонию , спастичность и мозжечковую атаксию . Примерно половина больных умирает от дыхательной или сердечной недостаточности к трехлетнему возрасту. Синдром Ли является наследственным заболеванием по материнской линии, и его диагноз устанавливается путем генетического тестирования вышеупомянутых митохондриальных генов, включая MT-ATP6. Мутации гена MT-ATP6, связанные с синдромом Ли, изменяют один строительный блок ДНК ( нуклеотид ) в гене MT-ATP6. Наиболее распространенное генетическое изменение заключается в замене нуклеотида тимина на гуанин в позиции 8993 (записывается как T8993G). Мутации, вызывающие синдром Ли, нарушают функцию или стабильность комплекса АТФ-синтазы , подавляя выработку АТФ и нарушая окислительное фосфорилирование . Хотя точный механизм неясен, исследователи полагают, что нарушение окислительного фосфорилирования может привести к гибели клетки из-за снижения энергии, доступной в клетке. Некоторые ткани, которым требуется большое количество энергии, такие как мозг, мышцы и сердце, кажутся особенно чувствительными к снижению клеточной энергии. Смерть клеток в головном мозге, вероятно, вызывает характерные изменения в мозге, наблюдаемые при синдроме Ли, которые способствуют появлению признаков и симптомов этого состояния. Гибель клеток в других чувствительных тканях также может способствовать развитию синдрома Ли. Heteroplasmic мутация Т → С МТ-ATP6 в положении 9185 приводит к замене высоко консервативный лейцин к пролину в кодоне 220 и heteroplasmic T → C миссенс мутации в положении 9191 преобразуется в высоко консервативный лейцине к пролину в положении 222 полипептид , приводящий к фенотипу типа Ли . Мутация T9185C привела к мягкому и обратимому фенотипу , при этом 97% образцов мышц и крови пациента отражали мутацию. Мутация T9191C имела гораздо более тяжелый фенотип, который привел к смерти пациента в возрасте 2 лет.
НАРП-синдром
Некоторые мутации гена ATP6, вызывающие синдром Ли, также ответственны за аналогичное, но менее тяжелое состояние, называемое невропатией, атаксией и пигментным ретинитом (NARP). Небольшое количество мутаций в гене MT-ATP6 было идентифицировано у людей с NARP. Каждая из этих мутаций изменяет один нуклеотид в гене MT-ATP6. Как и при синдроме Ли, наиболее частым генетическим изменением, связанным с NARP, является замена нуклеотида тимина на гуанин в позиции 8993 (обозначается как T8993G). Мутации, вызывающие NARP, изменяют структуру или функцию АТФ-синтазы , снижая способность митохондрий производить АТФ. Хотя точные эффекты этих мутаций неясны, исследователи продолжают исследовать, как изменения в гене MT-ATP6 влияют на производство АТФ и приводят к мышечной слабости, потере зрения и другим особенностям NARP.
Семейный двусторонний стриарный некроз
Состояние, называемое семейным двусторонним стриатальным некрозом, которое похоже на синдром Ли, также может быть результатом изменений в гене MT-ATP6. В нескольких зарегистрированных случаях с этими мутациями пораженные дети имели задержку развития, проблемы с движением и координацией, слабый мышечный тонус ( гипотония ) и необычно маленький размер головы ( микроцефалия ). Исследователи не определили, почему мутации MT-ATP6 приводят к такому сочетанию признаков и симптомов у детей с двусторонним стриарным некрозом.
Взаимодействия
Было показано, что MT-ATP6 имеет 20 бинарных белок-белковых взаимодействий, включая 17 сопряженных взаимодействий. MT-ATP6, по-видимому, взаимодействует с SP1 .
Исследовать
Фонд SENS Research опубликовал документ с подробным описанием успешного allotopic выражения сменной ДНК для гена MT-ATP6 в клеточной ядерной ДНК.
использованная литература
дальнейшее чтение
- Холм Э., Гретер Дж., Якобсон К.Э., Ларссон Н.Г., Линдстедт С., Нильссон К.О., Олдфорс А., Тулиниус М. (декабрь 1992 г.). «Дефицит митохондриальной АТФ-синтазы у ребенка с 3-метилглутаконовой ацидурией» . Педиатрические исследования . 32 (6): 731–5. DOI : 10.1203 / 00006450-199212000-00022 . PMID 1287564 .
- Торрони А., Ахилли А., Маколей В., Ричардс М., Бандельт Х. Дж. (Июнь 2006 г.). «Сбор плодов дерева мтДНК человека». Тенденции в генетике . 22 (6): 339–45. DOI : 10.1016 / j.tig.2006.04.001 . PMID 16678300 .
- Ingman M, Kaessmann H, Pääbo S, Gyllensten U (декабрь 2000 г.). «Вариации митохондриального генома и происхождение современного человека». Природа . 408 (6813): 708–13. Bibcode : 2000Natur.408..708I . DOI : 10.1038 / 35047064 . PMID 11130070 . S2CID 52850476 .
- Манфреди Дж., Фу Дж., Оджаими Дж., Сэдлок Дж. Э., Квонг Дж. К., Гай Дж., Шон Э. А. (апрель 2002 г.). «Восстановление дефицита синтеза АТФ путем переноса в ядро МТАТР6, гена, кодируемого митохондриальной ДНК». Генетика природы . 30 (4): 394–9. DOI : 10.1038 / ng851 . PMID 11925565 . S2CID 30012532 .
- Торигоэ Т., Изуми Х., Исигучи Х., Урамото Х., Мураками Т., Исэ Т, Йошида Й., Танабэ М., Номото М., Ито Х., Коно К. (сентябрь 2002 г.). «Повышенная экспрессия гена субъединицы c вакуолярной H + -АТФазы человека (ATP6L) в ответ на противораковые агенты» . Журнал биологической химии . 277 (39): 36534–43. DOI : 10.1074 / jbc.M202605200 . PMID 12133827 .
- Мишмар Д., Руис-Песини Е., Голик П., Маколей В., Кларк А.Г., Хоссейни С., Брэндон М., Исли К., Чен Е., Браун, М. Д., Сукерник Р. И., Олкерс А., Уоллес, округ Колумбия (январь 2003 г.). «Естественный отбор сформировал региональные вариации мтДНК у людей» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (1): 171–6. Bibcode : 2003PNAS..100..171M . DOI : 10.1073 / pnas.0136972100 . PMC 140917 . PMID 12509511 .
- Ingman M, Gyllensten U (июль 2003 г.). «Вариации митохондриального генома и история эволюции аборигенов Австралии и Новой Гвинеи» . Геномные исследования . 13 (7): 1600–6. DOI : 10.1101 / gr.686603 . PMC 403733 . PMID 12840039 .
- Kong QP, Yao YG, Sun C, Bandelt HJ, Zhu CL, Zhang YP (сентябрь 2003 г.). «Филогения восточноазиатских линий митохондриальной ДНК, выведенная из полных последовательностей» . Американский журнал генетики человека . 73 (3): 671–6. DOI : 10.1086 / 377718 . PMC 1180693 . PMID 12870132 .
- Temperley RJ, Seneca SH, Tonska K, Bartnik E, Bindoff LA, Lightowlers RN, Chrzanowska-Lightowlers ZM (сентябрь 2003 г.). «Исследование патогенной микроделеции мтДНК показывает трансляционно-зависимый путь распада деаденилирования в митохондриях человека» . Молекулярная генетика человека . 12 (18): 2341–8. DOI : 10,1093 / HMG / ddg238 . PMID 12915481 .
- Reuter TY, Medhurst AL, Waisfisz Q, Zhi Y, Herterich S, Hoehn H, Gross HJ, Joenje H, Hoatlin ME, Mathew CG, Huber PA (октябрь 2003 г.). «Двухгибридные экраны дрожжей предполагают участие белков анемии Фанкони в регуляции транскрипции, передаче сигналов клеток, окислительном метаболизме и клеточном транспорте». Экспериментальные исследования клеток . 289 (2): 211–21. DOI : 10.1016 / S0014-4827 (03) 00261-1 . PMID 14499622 .
- Dubot A, Godinot C, Dumur V, Sablonnière B, Stojkovic T., Cuisset JM, Vojtiskova A, Pecina P, Jesina P, Houstek J (январь 2004 г.). «GUG является эффективным инициирующим кодоном для трансляции митохондриального гена ATP6 человека». Сообщения о биохимических и биофизических исследованиях . 313 (3): 687–93. DOI : 10.1016 / j.bbrc.2003.12.013 . PMID 14697245 .
- Coble MD, Just RS, O'Callaghan JE, Letmanyi IH, Peterson CT, Irwin JA, Parsons TJ (июнь 2004 г.). «Однонуклеотидные полиморфизмы по всему геному мтДНК, повышающие эффективность судебно-медицинских исследований у кавказцев». Международный журнал судебной медицины . 118 (3): 137–46. DOI : 10.1007 / s00414-004-0427-6 . PMID 14760490 . S2CID 8413730 .
- Карроццо Р., Рицца Т., Стрингаро А., Пиерини Р., Мормон Е., Санторелли Ф.М., Малорни В., Матаррезе П. (июль 2004 г.). «Унаследованные от матери мутации, связанные с синдромом Ли, способствуют апоптозу, опосредованному митохондриями». Журнал нейрохимии . 90 (2): 490–501. DOI : 10.1111 / j.1471-4159.2004.02505.x . PMID 15228605 . S2CID 33013529 .
внешние ссылки
- GeneReviews / NCBI / NIH / UW запись о митохондриальном ДНК-ассоциированном синдроме Ли и NARP
- МТ-АТФ6 + белок, + человек по медицинским предметным рубрикам Национальной медицинской библиотеки США (MeSH)
Эта статья включает текст из Национальной медицинской библиотеки США , который находится в общественном достоянии .


