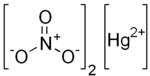
Нитрат ртути (II) - Mercury(II) nitrate
|
|
| Имена | |
|---|---|
|
Имена ИЮПАК
Динитрат
ртути Нитрат ртути (II) |
|
| Другие названия
Нитрат ртути
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.030.126 |
| Номер ЕС | |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
| Номер ООН | 1625 |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| Hg (NO 3 ) 2 | |
| Молярная масса | 324,60 г / моль (безводный) |
| Появление | бесцветные кристаллы или белый порошок |
| Запах | острый |
| Плотность | 4,3 г / см 3 (моногидрат) |
| Температура плавления | 79 ° С (174 ° F, 352 К) (моногидрат) |
| растворимый | |
| Растворимость | растворим в азотной кислоте , ацетоне , аммиаке нерастворим в спирте |
| −74,0 · 10 −6 см 3 / моль | |
| Опасности | |
| Паспорт безопасности | ICSC 0980 |
|
Классификация ЕС (DSD) (устаревшая)
|
Очень токсично ( T + ) Опасно для окружающей среды ( N ) |
| R-фразы (устаревшие) | R26 / 27/28 , R33 , R50 / 53 |
| S-фразы (устаревшие) | (S1 / 2) , S13 , S28 , S45 , S60 , S61 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| Родственные соединения | |
|
Другие анионы
|
Сульфат ртути (II) Хлорид ртути (II) |
|
Другие катионы
|
Нитрат цинка Нитрат кадмия |
|
Родственные соединения
|
Нитрат ртути (I) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Ртуть нитрат (II) , является токсичной бесцветным или белой растворимой кристаллической ртуть (II) , солью из азотной кислоты . Он использовался для обработки меха, чтобы сделать войлок в процессе, называемом « морковкой ». Фраза « сумасшедший как шляпник » связана с психологическим заболеванием, вызванным чрезмерным воздействием нитрата ртути (II). Эта практика продолжалась в Соединенных Штатах до тех пор, пока в декабре 1941 года она не была запрещена Службой общественного здравоохранения Соединенных Штатов . Запрет освободил нитрат ртути (II) для использования в производстве детонаторов во время продолжающейся войны.
Производство
Нитрат ртути (II) получают в результате реакции горячей концентрированной азотной кислоты с металлической ртутью , в этих условиях азотная кислота является окислителем . При разбавлении азотной кислоты образуется нитрат ртути (I) .
Использует
Нитрат ртути используется в реакциях меркурации. В частности, он используется в реакциях с участием кетонов. Одним из наиболее эффективных химикатов является ацетон. В этой реакции используются нитрат ртути, оксид ртути и сульфат кальция для превращения ацетона, который представляет собой CH 3 C (O) CH 3 , в CH 3 C (O) CH 2 Hg. Ацетон - это соединение, для которого большинство других методов меркурации неэффективны. Соединение нитрата ртути работает, потому что это сильный окислитель. Кроме того, когда ртуть растворяется в азотной кислоте, образуется кислотная форма нитрата ртути. Кислая форма способна инвертировать молекулы сахарозы.
Информация о здоровье
Нитрат ртути имеет тенденцию воздействовать на организм как Hg 2+ , которая считается формой неорганической ртути. Формы неорганической ртути можно найти в различных формах, включая крем для осветления кожи. Попадание неорганической ртути внутрь организма может изменить структуру важных белков. Если он попадает в почву, он может абсорбироваться и оставаться для растений. У людей, страдающих от отравления, как правило, самыми ранними симптомами являются рвота и диарея.
Реактивность
Хотя нитрат ртути не горюч, он может ускорить воспламенение, поскольку действует как окислитель. Кроме того, в сочетании со спиртами он может образовывать взрывоопасные соединения.
Смотрите также
Рекомендации
- ^ «Не такой уж безумный Шляпник: профессиональные опасности ртути» .
- ^ Мортон, Эйвери А .; Пеннер, Хельмут П. (1951). «Меркурация кетонов и некоторых других соединений нитратом ртути». Журнал Американского химического общества . 73 (7): 3300–3304. DOI : 10.1021 / ja01151a091 .
- ^ a b «Нитрат ртути» .
- ^ Блит, Александр Винтер; Блит, Мередит Винтер (1903). Продукты питания: их состав и анализ .
- Перейти ↑ Cochran, CB (1907). «Инверсия сахарозы кислым нитратом ртути» . Журнал Американского химического общества . 29 (4): 555–556. DOI : 10.1021 / ja01958a016 .
- ^ «Элементарная ртуть и неорганические соединения ртути: аспекты здоровья человека» (PDF) .
- ^ «Нитрат ртути» .
Внешние ссылки
- ATSDR - Портал токсичных веществ - Ртуть (14.11.2013)
- ATSDR - Заявление об общественном здравоохранении: ртуть (14.11.2013)
- ATSDR - ВНИМАНИЕ! Модели воздействия металлической ртути, 26.06.97 (ссылка не прослеживается 14.11.2013)
- ATSDR - Руководство по медицинскому лечению ртути (14.11.2013)
- ATSDR - Токсикологический профиль: ртуть (14.11.2013)
- Данные по безопасности (MSDS) (ссылка не прослеживается 14.11.2013)
- Нитрат ртути (ICSC)
- Меркурий
- Информационные пакеты Mercury
- How to Make Good Mercury Electrical Connections , Popular Science ежемесячно, февраль 1919 г., ненумерованная страница, сканировано Google Книгами: https://books.google.com/books?id=7igDAAAAMBAJ&pg=PT14

