Множественная миелома - Multiple myeloma
| Множественная миелома | |
|---|---|
| Другие имена | Плазменно-клеточная миелома, миеломатоз, болезнь Келера, миелома |
 | |
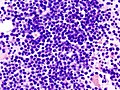
| Микрофотография из плазмоцитома , Н & Е окрашивания | |
| Специальность | Гематология и онкология |
| Симптомы | Боль в костях , утомляемость |
| Осложнения | Амилоидоз , проблемы с почками , переломы костей , синдром гипервязкости , инфекции, анемия |
| Продолжительность | Длительный срок |
| Причины | Неизвестный |
| Факторы риска | Ожирение |
| Диагностический метод | Анализы крови или мочи, биопсия костного мозга , медицинская визуализация |
| Уход | Стероиды , химиотерапия , талидомид , трансплантация стволовых клеток , бисфосфонаты , лучевая терапия |
| Прогноз | Пятилетняя выживаемость 54% / ожидаемая продолжительность жизни 6 лет (США) |
| Частота | 488 200 (пострадали в 2015 году) |
| Летальные исходы | 101 100 (2015) |
Множественная миелома ( ММ ), также известная как плазматические клетки миеломы и просто миеломы , является раком из клеток плазмы , типа белых кровяных клеток , которые обычно производят антитела . Часто изначально никаких симптомов не замечается. По мере прогрессирования могут возникать боли в костях , анемия , дисфункция почек и инфекции. Осложнения могут включать амилоидоз .
Причина множественной миеломы неизвестна. Факторы риска включают ожирение , радиационное облучение, семейный анамнез и некоторые химические вещества. Множественная миелома может развиться в результате моноклональной гаммопатии неопределенного значения, которая прогрессирует в тлеющую миелому . Аномальные плазматические клетки вырабатывают аномальные антитела , которые могут вызвать проблемы с почками и чрезмерно густую кровь . В плазматические клетки могут также образовывать массу в костном мозге или мягкой тканью. Когда присутствует одна опухоль, это называется плазмоцитомой ; более одной называется множественной миеломой. Множественная миелома диагностируется на основании анализов крови или мочи, обнаруживающих аномальные антитела, биопсии костного мозга, обнаруживающей раковые плазматические клетки, и медицинских изображений, обнаруживающих поражения костей. Еще одна частая находка - высокий уровень кальция в крови .
Множественная миелома считается излечимой, но в целом неизлечимой. Ремиссия может быть вызвана стероидами , химиотерапией , таргетной терапией и трансплантацией стволовых клеток . Бисфосфонаты и лучевая терапия иногда используются для уменьшения боли при поражениях костей.
Во всем мире от множественной миеломы пострадали 488 000 человек, и в 2015 году она стала причиной 101 100 случаев смерти. В Соединенных Штатах она развивается у 6,5 случаев на 100 000 человек в год, и 0,7% людей страдают от нее в какой-то момент своей жизни. Обычно это происходит в возрасте около 60 лет и чаще встречается у мужчин, чем у женщин. Это нечасто в возрасте до 40 лет. Без лечения средняя выживаемость в эпоху до химиотерапии составляла около 7 месяцев. После введения химиотерапии прогноз значительно улучшился: средняя выживаемость составила от 24 до 30 месяцев, а 10-летняя выживаемость составила 3%. Даже дальнейшее улучшение прогноза произошло благодаря внедрению новых биологических методов лечения и лучших вариантов спасения, при этом медиана выживаемости в настоящее время превышает 60–90 месяцев. При нынешнем лечении выживаемость обычно составляет 4–5 лет. Выживаемость пяти лет составляет около 54%. Слово миелома происходит от греческого myelo-, означающего «костный мозг», и -oma, что означает «опухоль».
Признаки и симптомы
Поскольку многие органы могут быть поражены миеломой, симптомы и признаки сильно различаются. Наиболее частыми симптомами при обращении являются усталость и боль в костях. Критерии CRAB охватывают наиболее распространенные признаки множественной миеломы:
- С alcium: кальций сыворотки> 0,25 ммоль / л (> 1 мг / дл) выше верхней границы нормы или> 2,75 ммоль / л (> 11 мг / дл)
- R еналя недостаточность: клиренс креатинина <40 мл в минуту или сывороточный креатинин> 1.77mol / л (> 2 мг / дл)
- Немия: Значение гемоглобина> 2 г / дл ниже самого нижнего предела нормальный, или значение гемоглобина <10 г / дл
- Поражения B one: остеолитические поражения при рентгенографии скелета, КТ или ПЭТ / КТ
Боль в костях
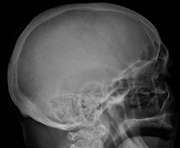
Боль в костях встречается почти у 70% людей с множественной миеломой и является одним из наиболее распространенных симптомов. Миеломная боль в костях обычно затрагивает позвоночник и ребра и усиливается при физической активности. Постоянная локализованная боль может указывать на патологический перелом кости . Вовлечение позвонков может привести к компрессии спинного мозга или кифозу . Миеломная болезнь костей возникает из-за сверхэкспрессии активатора рецептора лиганда ядерного фактора κB ( RANKL ) стромой костного мозга . RANKL активирует остеокласты , резорбирующие кость. Возникающие в результате поражения костей являются литическими (вызывают разрушение) по своей природе и лучше всего видны на простых рентгенограммах, которые могут показать «выбитые» резорбтивные поражения (включая вид «дождевых капель» черепа на рентгенограмме). Разрушение костей также приводит к выбросу ионов кальция в кровь, что приводит к гиперкальциемии и связанным с ней симптомам.
Анемия
Анемия, обнаруживаемая при миеломе, обычно бывает нормоцитарной и нормохромной . Это происходит в результате замещения нормального костного мозга инфильтрирующими опухолевыми клетками и ингибирования цитокинами нормальной выработки красных кровяных телец ( гемопоэза ) .
Нарушение функции почек.
Нарушение функции почек может развиваться как остро, так и хронически , любой степени тяжести.
Наиболее частая причина почечной недостаточности при множественной миеломе связана с белками, секретируемыми злокачественными клетками. Клетки миеломы продуцируют моноклональные белки различных типов, чаще всего иммуноглобулины (антитела) и свободные легкие цепи , что приводит к аномально высоким уровням этих белков в крови. В зависимости от размера этих белков они могут выводиться через почки. Почки могут быть повреждены действием белков или легких цепей. Повышенная резорбция костной ткани приводит к гиперкальциемии и вызывает нефрокальциноз , тем самым способствуя почечной недостаточности. Амилоидоз занимает третье место в причинно-следственной связи. У людей с амилоидозом высокий уровень амилоидного белка, который может выводиться через почки и вызывать повреждение почек и других органов.
Легкие цепи вызывают множество эффектов, которые могут проявляться как синдром Фанкони ( почечный тубулярный ацидоз II типа ).
Инфекционное заболевание
Наиболее частыми инфекциями являются пневмонии и пиелонефрит . Общие возбудители пневмонии включают S. pneumoniae , S. aureus и K. pneumoniae , тогда как общие патогены, вызывающие пиелонефрит, включают E. coli и другие грамотрицательные организмы. Период наибольшего риска возникновения инфекции приходится на первые несколько месяцев после начала химиотерапии. Повышенный риск заражения связан с иммунодефицитом. Хотя общий уровень иммуноглобулинов обычно повышен при множественной миеломе, большинство антител являются неэффективными моноклональными антителами из клональных плазматических клеток. Выбранная группа людей с документально подтвержденной гипогаммаглобулинемией может получить пользу от заместительной терапии иммуноглобулином для снижения риска инфекции.
Неврологические симптомы
Некоторые симптомы (например, слабость , спутанность сознания и утомляемость ) могут быть следствием анемии или гиперкальциемии. Головная боль , визуальные изменения и ретинопатия могут быть результатом повышенной вязкости крови в зависимости от свойств парапротеина . И, наконец, корешковой боли , потеря кишечника или мочевого пузыря (за счет вовлечения спинного мозга , ведущей к компрессии спинного мозга ) или кистевой туннельный синдром , а также другие невропатии (за счет инфильтрации периферических нервов путем амилоида ) может произойти. В поздних случаях это может привести к параплегии .
Когда заболевание находится под хорошим контролем, неврологические симптомы могут возникать в результате текущего лечения, некоторые из которых могут вызывать периферическую невропатию, проявляющуюся онемением или болью в руках, ступнях и голенях.
Рот
Первоначальные симптомы могут включать боль, онемение, отек, расширение челюсти, подвижность зубов и прозрачность. Множественная миелома во рту может имитировать общие проблемы с зубами, такие как периапикальный абсцесс или периодонтальный абсцесс , гингивит , пародонтит или другое увеличение или образование десен.
Причина
Причина множественной миеломы обычно неизвестна.
Факторы риска
- Моноклональная гаммопатия неопределенного значения (MGUS) увеличивает риск развития множественной миеломы. MGUS трансформируется в множественную миелому со скоростью от 1% до 2% в год , и почти всем случаям множественной миеломы предшествует MGUS.
- Тлеющая множественная миелома увеличивает риск развития множественной миеломы. У людей с диагнозом этого предракового заболевания развивается множественная миелома со скоростью 10% в год в течение первых 5 лет, 3% в год в течение следующих 5 лет, а затем 1% в год.
- Ожирение связано с множественной миеломой, при этом каждое увеличение индекса массы тела на пять увеличивает риск на 11%.
Исследования сообщили о семейной предрасположенности к миеломе. Гиперфосфорилирование ряда белков - белков paratarg - тенденция, которая наследуется по аутосомно-доминантному типу, является общим механизмом в этих семьях. Эта тенденция чаще встречается у афроамериканцев с миеломой и может способствовать более высокому уровню миеломы в этой группе.
Вирус Эпштейна-Барра
В редких случаях вирус Эпштейна-Барра (ВЭБ) связан с множественной миеломой, особенно у людей с иммунодефицитом, вызванным, например, ВИЧ / СПИДом , трансплантацией органов или хроническим воспалительным заболеванием, таким как ревматоидный артрит . ВЭБ-положительная множественная миелома классифицируется Всемирной организацией здравоохранения (2016 г.) как одна из форм лимфопролиферативных заболеваний, связанных с вирусом Эпштейна-Барра, и называется миеломой плазматических клеток, ассоциированной с вирусом Эпштейна-Барра . EBV-положительное заболевание чаще встречается при плазмоцитоме , чем при множественной миеломной форме рака плазматических клеток. В тканях, вовлеченных в болезнь EBV +, обычно обнаруживаются очаги EBV + клеток с появлением быстро пролиферирующих незрелых или низкодифференцированных плазматических клеток. Клетки экспрессируют продукты генов EBV, такие как EBER1 и EBER2. Хотя ВЭБ способствует развитию и / или прогрессированию большинства лимфопролиферативных заболеваний, связанных с вирусом Эпштейна-Барра, его роль в развитии множественной миеломы неизвестна. Однако люди с EBV-положительным статусом и локализованной плазмоцитомой с большей вероятностью разовьются до множественной миеломы по сравнению с людьми с EBV-отрицательной плазмоцитомой. Это предполагает, что EBV может играть роль в прогрессировании плазмоцитомы в системную множественную миелому.
Патофизиология
В-лимфоциты начинаются в костном мозге и перемещаются в лимфатические узлы. По мере развития они созревают и отображают различные белки на поверхности своих клеток. Когда они активируются для выделения антител, они известны как плазматические клетки.
Множественная миелома развивается в B-лимфоцитах после того, как они покинули часть лимфатического узла, известную как зародышевый центр . Нормальная клеточная линия, наиболее тесно связанная с клетками ММ, обычно считается либо активированной В-клеткой памяти, либо предшественником плазматических клеток, плазмобластом .
Иммунная система строго контролирует пролиферацию В-клеток и секрецию антител. Когда хромосомы и гены повреждены, часто в результате перестройки, этот контроль теряется. Часто ген-промотор перемещается (или перемещается) в хромосому, где он стимулирует ген антитела к перепроизводству.
Хромосомная транслокация между тяжелой цепью иммуноглобулина геном (на хромосоме 14 , локус Q32) и онкогеном (часто 11q13, 4p16.3, 6p21, 16q23 и 20q11) часто наблюдается у людей с множественной миеломой. Эта мутация приводит к нарушению регуляции онкогена, что считается важным инициирующим событием в патогенезе миеломы. Результатом является распространение клона плазматической клетки и геномная нестабильность, которая приводит к дальнейшим мутациям и транслокациям. Аномалия хромосомы 14 наблюдается примерно в 50% всех случаев миеломы. Делеция (части) хромосомы 13 также наблюдается примерно в 50% случаев.
Производство цитокинов (особенно IL-6 ) плазматическими клетками вызывает большую часть их локализованных повреждений, таких как остеопороз , и создает микросреду, в которой процветают злокачественные клетки. Увеличивается ангиогенез (образование новых кровеносных сосудов).
Полученные антитела откладываются в различных органах, что приводит к почечной недостаточности, полинейропатии и различным другим симптомам, связанным с миеломой.
Эпигенетический
В исследовании, которое изучало профиль метилирования ДНК клеток множественной миеломы и нормальных плазматических клеток , наблюдалось постепенное деметилирование от стволовых клеток к плазматическим клеткам. Наблюдаемый паттерн метилирования CpG в интронных областях с метками хроматина, связанными с энхансером, при множественной миеломе подобен недифференцированным клеткам-предшественникам и стволовым клеткам. Эти результаты могут представлять собой эпигенетическое перепрограммирование de novo при множественной миеломе, ведущее к приобретению паттерна метилирования, связанного со стволовостью. Другие исследования выявили паттерн подавления гена, специфичный для множественной миеломы, связанный с репрессивным комплексом 2 polycomb (PRC2). Повышенная экспрессия субъединицы PRC2, EZH2, как было описано, является общим признаком множественной миеломы, что приводит к накоплению и перераспределению гистонов. Триметилирование лизина H3 27, прогрессирующее с увеличением тяжести заболевания.
Генетика
Хромосомные аномалии, обычно встречающиеся при этом заболевании, такие как трисомия нескольких нечетных хромосом, t (11; 14) и del (13q), не связаны с худшим прогнозом. Однако около 25% пациентов с впервые диагностированным заболеванием имеют аномалии, связанные с худшим прогнозом, такие как t (4; 14), t (14; 16) и del (17p). Другие менее распространенные аномалии, связанные с худшим прогнозом, включают t (14; 20) и ≥4 копий 1q.
Связанные генетические мутации включают ATM , BRAF , CCND1 , DIS3 , FAM46C , KRAS , NRAS и TP53 .
Разработка
Генетические и эпигенетические изменения происходят постепенно. Первоначальное изменение, часто связанное с транслокацией одной хромосомы 14, создает клон плазматических клеток костного мозга, вызывающий бессимптомное заболевание MGUS , предраковое заболевание, характеризующееся повышенным количеством плазматических клеток в костном мозге или циркуляцией миеломного белка иммуноглобулина. . Дальнейшие генетические или эпигенные изменения приводят к образованию нового клона плазматических клеток костного мозга, обычно потомка исходного клона, который вызывает более серьезное, но все еще бессимптомное предраковое заболевание, тлеющее множественной миеломой. Эта миелома характеризуется увеличением количества плазматических клеток костного мозга или уровней циркулирующего миеломного белка выше, чем при MGUS.
Последующие генетические и эпигенетические изменения приводят к новому, более агрессивному клону плазматических клеток, что вызывает дальнейшее повышение уровня циркулирующего миеломного белка, дальнейшее увеличение количества плазматических клеток костного мозга или развитие одного или нескольких из них. специфический набор симптомов «КРАБИНА», которые являются основой для диагностики злокачественной множественной миеломы и лечения заболевания.
В небольшом проценте от нескольких случаев миеломов, дальнейшие генетические и эпигенетические изменения приводят к развитию клона плазматических клеток , что перемещается из костного мозга в кровеносную систему , вторгается отдаленные ткани, и тем самое приводит к наиболее злокачественная все клеткам плазмы дискразий , лейкоз плазматических клеток . Таким образом, фундаментальная генетическая нестабильность плазматических клеток или их предшественников приводит к прогрессированию:
Моноклональная гаммопатия неустановленного значения → тлеющая множественная миелома → множественная миелома → лейкоз плазматических клеток
Бессимптомная моноклональная гаммапатия неустановленного значения и тлеющая множественная миелома обычно диагностируются случайно, обнаруживая белок миеломы в тестах электрофореза белков сыворотки, проводимых для других целей. MGUS - относительно стабильное заболевание, которым страдают 3% людей в возрасте 50 лет и 5% людей в возрасте 70 лет; прогрессирует до множественной миеломы 0,5–1% случаев в год; тлеющая множественная миелома делает это со скоростью 10% в год в течение первых 5 лет, но затем резко падает до 3% в год в течение следующих 5 лет, а затем до 1% в год.
В целом, около 2–4% случаев множественной миеломы в конечном итоге прогрессируют до лейкемии плазматических клеток.
Диагностика
Анализы крови

Уровень глобулина может быть нормальным при установленном заболевании. Врач может запросить электрофорез белков крови и мочи, который может показать наличие полосы парапротеина (моноклонального белка или М-белка ) с или без снижения других (нормальных) иммуноглобулинов (известный как иммунный парез). Одним из типов парапротеинов является белок Бенс-Джонса , который представляет собой парапротеин мочи, состоящий из свободных легких цепей. Количественные измерения парапротеина необходимы для постановки диагноза и наблюдения за заболеванием. Парапротеин - это аномальный иммуноглобулин, продуцируемый клоном опухоли.
Теоретически множественная миелома может продуцировать все классы иммуноглобулинов, но наиболее распространены парапротеины IgG , за которыми следуют IgA и IgM . Миелома IgD и IgE встречается очень редко. Кроме того, легкие и / или тяжелые цепи (строительные блоки антител) могут секретироваться изолированно: κ- или λ-легкие цепи или любой из пяти типов тяжелых цепей (α-, γ-, δ-, ε- или μ-тяжелые цепи). Люди без признаков моноклонального белка могут иметь «несекреторную» миелому (не продуцирующую иммуноглобулины); это составляет около 3% всех людей с множественной миеломой.
Дополнительные результаты могут включать повышенный уровень кальция (когда остеокласты разрушают кость, высвобождая ее в кровоток), повышенный уровень креатинина в сыворотке из-за снижения функции почек , что в основном связано с отложением парапротеинов в почках, хотя гипсовая повязка может также содержат полные иммуноглобулины, белок Тамма-Хорсфалла и альбумин .
Другие полезные лабораторные тесты включают количественное измерение IgA, IgG и IgM для выявления иммунного пареза и бета-2-микроглобулина, который предоставляет прогностическую информацию. В мазке периферической крови обычно наблюдается круговое образование красных кровяных телец , хотя это не специфично.
Недавнее внедрение коммерческого иммуноанализа для измерения свободных легких цепей потенциально предлагает улучшение мониторинга прогрессирования заболевания и ответа на лечение, особенно там, где парапротеин трудно точно измерить электрофорезом (например, при миеломе легких цепей или когда уровень парапротеина очень низкий). Первоначальные исследования также предполагают, что измерение свободных легких цепей также может использоваться в сочетании с другими маркерами для оценки риска прогрессирования MGUS в множественную миелому.
Этот анализ, анализ свободных легких цепей в сыворотке крови, недавно был рекомендован Международной рабочей группой по миеломе для скрининга, диагностики, прогноза и мониторинга дискразий плазматических клеток.
Аспират костного мозга, показывающий гистологический коррелят множественной миеломы под микроскопом, окраска H&E
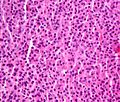
Микрофотография показывает миеломы произнесения нефропатии в биопсии почки : Гиалиновый слепки PAS положительные (темно - розовый / красный - право изображения). Миеломатозные цилиндры PAS-отрицательные (бледно-розовые - слева от изображения), PAS-окраска .
Гистопатология
Биопсии костного мозга , как правило , выполнены , чтобы определить , какой процент костного мозга , занимаемое плазматическими клетками. Этот процент используется в диагностических критериях миеломы. Иммуногистохимия (окрашивание определенных типов клеток с использованием антител против поверхностных белков) может обнаруживать плазматические клетки, которые экспрессируют иммуноглобулин в цитоплазме, а иногда и на поверхности клетки; Клетки миеломы часто являются CD56 , CD38 , CD138 и CD319 положительными и CD19 , CD20 и CD45 отрицательными. Проточная цитометрия часто используется для установления клональной природы плазматических клеток, которые обычно экспрессируют только легкую цепь каппа или лямбда. Цитогенетика также может выполняться при миеломе с прогностическими целями, включая специфическую для миеломы флуоресцентную гибридизацию in situ и виртуальный кариотип .
Плазматические клетки, наблюдаемые при множественной миеломе, имеют несколько возможных морфологий. Во-первых, они могут иметь вид нормальной плазматической клетки, большой клетки, в два или три раза превышающей размер периферических лимфоцитов. Поскольку они активно вырабатывают антитела, аппарат Гольджи обычно создает светлую область, прилегающую к ядру, называемую перинуклеарным ореолом. Одиночное ядро (внутри одно ядрышко с везикулярным ядерным хроматином) эксцентрично, замещено обильной цитоплазмой. Другие распространенные морфологии, которые наблюдаются, но которые не характерны для нормальных плазматических клеток, включают:
- Причудливые многоядерные клетки
- Клетки Мотта, содержащие несколько сгруппированных цитоплазматических капель или других включений (иногда их путают с палочками Ауэра , обычно наблюдаемыми в миелоидных бластах)
- Клетки пламени, имеющие ярко-красную цитоплазму
Исторически CD138 использовался для выделения миеломных клеток в диагностических целях. Однако этот антиген быстро исчезает ex vivo . Однако недавно было обнаружено , что поверхностный антиген CD319 (SLAMF7) значительно более стабилен и позволяет надежно изолировать злокачественные плазматические клетки из отложенных или даже криоконсервированных образцов.
Прогноз широко варьируется в зависимости от различных факторов риска. Клиника Майо разработала модель стратификации риска, названную стратификацией Майо для миеломы и терапией, адаптированной к риску (mSMART), которая делит людей на категории высокого и стандартного риска. Люди с делецией 13 хромосомы или гиподиплоидией с помощью традиционной цитогенетики, t (4; 14), t (14; 16), t (14; 20) или 17p - с помощью молекулярно-генетических исследований или с высоким индексом мечения плазматических клеток (3 % и более) считаются имеющими миелому высокого риска.
Медицинская визуализация
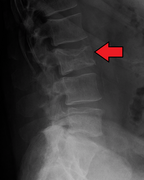
Диагностическое обследование человека с подозрением на множественную миелому обычно включает исследование скелета . Это серия рентгеновских снимков черепа, осевого скелета и проксимальных длинных костей. Миеломная активность иногда проявляется в виде «литических поражений» (с местным исчезновением нормальной кости из-за резорбции). А на рентгенограмме черепа в виде «выбитых очагов» (дождевая капля черепа). Поражения также могут быть склеротическими , что воспринимается как рентгеноконтрастное . В целом радиоплотность миеломы составляет от -30 до 120 единиц Хаунсфилда (HU). Магнитно-резонансная томография более чувствительна, чем простая рентгенография, при обнаружении литических поражений и может заменить обследование скелета, особенно при подозрении на заболевание позвоночника. Иногда выполняется компьютерная томография, чтобы измерить размер плазмоцитомы мягких тканей. Сканирование костей обычно не имеет дополнительной ценности при обследовании людей с миеломой (нет образования новой кости; литические поражения плохо визуализируются при сканировании костей).
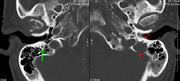
КТ головного мозга показали литическое поражение в левой височной кости (правая сторона изображения), и Petrouš временные кости с участием сосцевидного сегмент лицевого нервом канала. Красные стрелки: поражение; зеленая стрелка: нормальный контрлатеральный канал лицевого нерва. Поражения соответствуют отложению миеломы.
КТ нижнего отдела позвоночника у мужчины с множественной миеломой показывает множественные остеобластические поражения: они более радиоплотные (на этом изображении ярче), чем окружающая губчатая кость , в отличие от остеолитических поражений, которые менее радиоактивны.
Бедренная кость с множественными поражениями миеломы
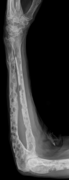
Плечевая кость с множественными поражениями миеломы
Диагностические критерии
В 2003 году IMG согласовала диагностические критерии симптоматической миеломы, бессимптомной миеломы и MGUS, которые впоследствии были обновлены в 2009 году:
- Симптоматическая миелома (должны соблюдаться все три критерия):
- Клональные плазматические клетки> 10% при биопсии костного мозга или (в любом количестве) при биопсии из других тканей ( плазмоцитома )
- Моноклональные белки (белок миеломов) в любой сыворотке или моче , и он должен быть больше , чем 3 г / дл ( за исключение случаев истинных nonsecretory миеломов)
- Доказательства повреждения органа-мишени, связанного с заболеванием плазматических клеток (поражение связанного органа или ткани, КРАБ):
- Hyper С alcemia (скорректированного кальция> 2,75 ммоль / л,> 11 мг / дл)
- R еналь недостаточность (почечная недостаточность)относящийся к миеломам
- Немия (гемоглобин <10 г / дл)
- B one поражения (литические поражения или остеопороз с компрессионными переломами)
Примечание: одних рецидивирующих инфекций у человека, у которого нет ни одного из признаков КРАБ, недостаточно для постановки диагноза миеломы. Людей, у которых отсутствуют признаки КРАБ, но есть признаки амилоидоза, следует рассматривать как амилоидоз, а не миелому. КРАБ-подобные аномалии характерны для многих заболеваний, и следует считать, что эти аномалии напрямую связаны с заболеванием плазматических клеток, и должны быть предприняты все попытки исключить другие основные причины анемии, почечной недостаточности и т. Д.
В 2014 году IMWG обновила свои критерии, включив в них биомаркеры злокачественных новообразований. Эти биомаркеры представляют собой> 60% клональных плазматических клеток, соотношение вовлеченных / не вовлеченных свободных легких цепей в сыворотке ≥ 100 (концентрация вовлеченных свободных легких цепей должна быть ≥ 100 мг / л) и более одного очагового поражения ≥ 5 мм по данным МРТ. Вместе эти биомаркеры и критерии КРАБ известны как события, определяющие миелому (MDE). Чтобы диагностировать миелому, у человека должно быть> 10% клональных плазматических клеток и любые MDE. Критерии биомаркеров были добавлены, чтобы тлеющие люди с множественной миеломой с высоким риском развития множественной миеломы могли быть диагностированы до того, как произошло повреждение органа, чтобы у них был лучший прогноз.
- Бессимптомная / тлеющая миелома:
- Сывороточный белок M > 30 г / л (3 г / дл) или
- Клональные плазматические клетки> 10% при биопсии костного мозга и
- Отсутствие связанных с миеломой поражения органов или тканей
- Моноклональная гаммопатия неустановленного значения (MGUS):
- Парапротеин сыворотки <30 г / л (3 г / дл) и
- Клональные плазматические клетки <10% при биопсии костного мозга и
- Отсутствие связанного с миеломой поражения органа или ткани или связанного с ним лимфопролиферативного нарушения В-клеток
Связанные состояния включают одиночную плазмоцитому (единичную опухоль плазматических клеток, обычно лечатся облучением ), дискразию плазматических клеток (когда только антитела вызывают симптомы, например, амилоидоз AL ) и периферическую невропатию, органегалию, эндокринопатию, моноклональное нарушение плазматических клеток и кожные изменения .
Постановка
При множественной миеломе определение стадии помогает прогнозировать, но не влияет на принятие решения о лечении. Исторически сложилось так, что система стадирования Durie-Salmon была заменена Международной системой стадирования (ISS), опубликованной Международной рабочей группой по миеломе в 2005 году. Пересмотренная версия ISS (R-ISS) была опубликована в 2015 году и включает цитогенетику и лактатдегидрогеназу ( ЛДГ).
- Стадия I: β 2 микроглобулин (β2M) <3,5 мг / л, альбумин ≥ 3,5 г / дл, нормальные цитогенетики, нет повышенного ЛДГ
- Стадия II: не отнесена к стадии I или стадии III.
- Стадия III: β2M ≥ 5,5 мг / л и либо повышенный уровень ЛДГ, либо цитогенетика высокого риска [t (4,14), t (14,16) и / или del (17p)]
Профилактика
Риск множественной миеломы можно немного снизить, если поддерживать нормальную массу тела.
Уход
Лечение показано при миеломе с симптомами. Если симптомы отсутствуют, но присутствует парапротеин, типичный для миеломы и диагностического костного мозга, без повреждения органов-мишеней, лечение обычно откладывают или ограничивают клиническими испытаниями. Лечение множественной миеломы направлено на уменьшение популяции клональных плазматических клеток и, как следствие, уменьшение симптомов заболевания.
Химиотерапия
Исходный
Первоначальное лечение множественной миеломы зависит от возраста человека и других имеющихся заболеваний.
Предпочтительным лечением для лиц моложе 65 лет является химиотерапия в высоких дозах, обычно с использованием схем на основе бортезомиба , и леналидомид- дексаметазон с последующей трансплантацией стволовых клеток. Исследование 2016 года пришло к выводу, что трансплантация стволовых клеток является предпочтительным методом лечения множественной миеломы. Существует два типа трансплантации стволовых клеток для лечения множественной миеломы. При аутологичной трансплантации гемопоэтических стволовых клеток (ASCT) собственные стволовые клетки пациента берутся из собственной крови пациента. Пациенту назначают высокодозную химиотерапию, после чего стволовые клетки пациента трансплантируются обратно пациенту. Этот процесс не излечивает, но продлевает общую выживаемость и полную ремиссию. При аллогенной трансплантации стволовых клеток пораженному человеку пересаживаются стволовые клетки здорового донора. Аллогенная трансплантация стволовых клеток имеет потенциал излечения, но используется у очень небольшого процента людей (и в условиях рецидива, а не как часть начального лечения). Более того, 5–10% связанная с лечением смертность связана с трансплантацией аллогенных стволовых клеток.
Люди старше 65 лет и люди с серьезными сопутствующими заболеваниями часто не переносят трансплантацию стволовых клеток. Для этих людей стандартным лечением была химиотерапия мелфаланом и преднизоном. Недавние исследования среди этой группы населения предполагают улучшение результатов при использовании новых схем химиотерапии, например, бортезомиба. При лечении бортезомибом, мелфаланом и преднизоном общая выживаемость составила 83% через 30 месяцев, леналидомид плюс низкие дозы дексаметазона - 82% через 2 года, а мелфалан, преднизон и леналидомид - 90% через 2 года. Прямые исследования, сравнивающие эти схемы, по состоянию на 2008 г. не проводились.
Поддерживается непрерывная терапия с использованием нескольких комбинаций антимиеломных препаратов бортезомиба , леналидомида и талидомида в качестве начального лечения множественной миеломы, не подходящей для трансплантации. Необходимы дальнейшие клинические исследования, чтобы определить потенциальный вред этих препаратов и их влияние на качество жизни человека. В обзоре 2009 года отмечалось: «Тромбоз глубоких вен и тромбоэмболия легочной артерии являются основными побочными эффектами талидомида и леналидомида. Леналидомид вызывает усиление миелосупрессии, а талидомид вызывает большее седативное действие. Вызванные химиотерапией периферическая нейропатия и тромбоцитопения являются основными побочными эффектами бортезомиба».
Для предотвращения неврологических симптомов или почечной недостаточности может потребоваться лечение связанного с ним синдрома гипервязкости.
Обслуживание
У большинства людей, в том числе получавших ASCT, наблюдается рецидив после первоначального лечения. Для предотвращения рецидива часто используется поддерживающая терапия с использованием длительного курса малотоксичных препаратов. Метаанализ 2017 года показал, что поддерживающая терапия леналидомидом после ASCT улучшила выживаемость без прогрессирования заболевания и общую выживаемость у людей со стандартным риском. Клиническое исследование 2012 года показало, что поддерживающая схема на основе бортезомиба приносит пользу людям с заболеваниями среднего и высокого риска.
Рецидив
Причины рецидива включают в себя развитие болезни либо из-за избирательного давления, оказываемого лечением, либо из-за мутаций de novo и / или из-за того, что заболевание не было адекватно представлено в начальной биопсии. Рецидив в течение первых 18 месяцев после постановки диагноза считается функциональной множественной миеломой высокого риска. В зависимости от состояния человека, использованных ранее методов лечения и продолжительности ремиссии варианты рецидива заболевания включают повторное лечение исходным агентом, использование других агентов (таких как мелфалан, циклофосфамид, талидомид или дексаметазон, отдельно или в комбинации). и второй ASCT.
Позже, по мере развития болезни, он становится невосприимчивым к ранее эффективному лечению. Эта стадия называется рецидивирующей / рефрактерной множественной миеломой (RRMM). Методы лечения, которые обычно используются для лечения RRMM, включают дексаметазон, ингибиторы протеасом (например, бортезомиб и карфилзомиб ), иммуномодулирующие имидные препараты (например, талидомид, леналидомид и помалидомид ) и определенные моноклональные антитела (например, против CD38 и CD319 ). Ожидаемая продолжительность жизни увеличилась в последние годы, и новые методы лечения находятся в стадии разработки.
Почечная недостаточность при множественной миеломе может быть острой (обратимой) или хронической (необратимой). Острая почечная недостаточность обычно проходит, когда уровень кальция и парапротеинов находится под контролем. Лечение хронической почечной недостаточности зависит от типа почечной недостаточности и может включать диализ .
Для лечения запущенного заболевания одобрено несколько новых вариантов:
- белантамаб мафодотин - моноклональное антитело против антигена созревания B-клеток (BCMA), также известное как CD269, предназначенное для лечения взрослых с рецидивирующей или рефрактерной множественной миеломой, которые ранее получали как минимум четыре лечения, включая моноклональные антитела против CD38, a ингибитор протеасом и иммуномодулирующее средство.
-
карфилзомиб - ингибитор протеасом, который показан:
- в качестве единственного агента у людей, получивших одну или несколько линий терапии
- в комбинации с дексаметазоном или с леналидомидом и дексаметазоном у людей, получивших от одной до трех линий терапии
- даратумумаб - моноклональное антитело против CD38, показанное людям, которые получали не менее трех предшествующих линий терапии, включая ингибитор протеасом и иммуномодулирующее средство, или которые обладают двойной резистентностью к ингибитору протеасом и иммуномодулирующему агенту
- элотузумаб - иммуностимулирующее гуманизированное моноклональное антитело против SLAMF7 (также известное как CD319), показанное в комбинации с леналидомидом и дексаметазоном людям, которые ранее получали от одного до трех курсов лечения
- изатуксимаб - моноклональное антитело против CD38, показанное в комбинации с помалидомидом и дексаметазоном для лечения взрослых с множественной миеломой, которые ранее получали как минимум два лечения, включая леналидомид и ингибитор протеасом .
- иксазомиб - ингибитор протеасом, доступный для перорального применения, показан в комбинации с леналидомидом и дексаметазоном людям, которые ранее получали хотя бы одну терапию.
- панобиностат - пероральный ингибитор гистондеацетилазы, используемый в комбинации с бортезомибом и дексаметазоном у людей, которые ранее получали как минимум две схемы химиотерапии, включая бортезомиб и иммуномодулирующее средство
- селинексор - доступный перорально селективный ингибитор ядерного экспорта, показанный в комбинации с дексаметазоном людям, которые ранее получали как минимум четыре курса лечения и чье заболевание не реагирует как минимум на два ингибитора протеасом, два иммуномодулирующих средства и моноклональное антитело к CD38
- idecabtagene vicleucel - первая клеточная генная терапия была одобрена FDA в 2021 году для лечения взрослых с рецидивирующей или рефрактерной множественной миеломой, получивших не менее четырех предшествующих терапий
Пересадка стволовых клеток
Трансплантация стволовых клеток может использоваться для лечения множественной миеломы. Трансплантация стволовых клеток сопряжена с риском болезни "трансплантат против хозяина" . Мезенхимальные стромальные клетки могут снизить общую смертность, если они используются в терапевтических целях, а терапевтическое использование МСК может увеличить полный ответ острой и хронической РТПХ, но доказательства очень сомнительны. Данные свидетельствуют о том, что МСК в профилактических целях практически не приводят к разнице в смертности от всех причин, рецидивах злокачественных заболеваний и частоте острой РТПХ. Данные свидетельствуют о том, что МСК в профилактических целях снижают частоту хронической РТПХ.
Прочие меры
Помимо прямого лечения пролиферации плазматических клеток, для предотвращения переломов обычно вводят бисфосфонаты (например, памидронат или золедроновую кислоту ); они также обладают прямым противоопухолевым действием даже у людей без известных заболеваний скелета. При необходимости для лечения анемии можно использовать переливание эритроцитов или эритропоэтин .
Побочные эффекты
Химиотерапия и трансплантация стволовых клеток могут вызвать нежелательные кровотечения и могут потребовать переливания тромбоцитов. Было замечено, что переливание тромбоцитов людям, проходящим химиотерапию или трансплантацию стволовых клеток для предотвращения кровотечений, по-разному влияло на количество участников с кровотечением, количество дней, в которые происходило кровотечение, смертность, вторичную по отношению к кровотечению. и количество переливаний тромбоцитов в зависимости от того, как они использовались (терапевтические, в зависимости от порогового значения, различные схемы дозирования или профилактические).
Поддерживающее лечение
Добавление физических упражнений к стандартному лечению взрослых пациентов с гематологическими злокачественными новообразованиями, такими как множественная миелома, может практически не повлиять на смертность, качество жизни и физическое функционирование. Эти упражнения могут немного уменьшить депрессию. Кроме того, аэробные упражнения, вероятно, уменьшают утомляемость. Доказательства очень неопределенны в отношении эффекта и серьезных нежелательных явлений.
Паллиативная помощь
Во многих национальных руководствах по лечению рака рекомендуется ранняя паллиативная помощь людям с запущенной множественной миеломой на момент постановки диагноза и всем, у кого есть серьезные симптомы.
Паллиативная помощь подходит на любой стадии множественной миеломы и может предоставляться наряду с лечебным лечением. Помимо устранения симптомов рака, паллиативная помощь помогает справиться с нежелательными побочными эффектами, такими как боль и тошнота, связанные с лечением.
Зубы
Профилактика полости рта, инструкции по гигиене и устранение источников инфекции во рту до начала лечения рака могут снизить риск инфекционных осложнений. Перед началом терапии бисфосфонатами необходимо оценить состояние зубов пациента, чтобы оценить факторы риска, чтобы предотвратить развитие медикаментозного остеонекроза челюсти (MRONJ). Если есть какие-либо симптомы или рентгенологические признаки MRONJ, такие как боль в челюсти, шатающийся зуб, отек слизистой оболочки, рекомендуется раннее направление к хирургу-стоматологу. Следует избегать удаления зубов в период активного лечения и лечить зуб нехирургическим лечением корневых каналов.
Прогноз
В целом 5-летняя выживаемость в США составляет около 54%. При терапии высокими дозами, сопровождаемой ASCT, средняя выживаемость, по оценкам, в 2003 г. составляла около 4,5 лет по сравнению со средним значением около 3,5 лет при «стандартной» терапии.
Международная система стадирования может помочь предсказать выживание, с медианы выживаемости (в 2005 г.) 62 месяцев для этапа 1-заболевания, 45 месяцев для стадии заболевания-2, и 29 месяцев для этапа 3-заболевания. Средний возраст постановки диагноза - 69 лет.
Генетическое тестирование
Кариотипирование массива SNP может обнаруживать прогностически значимые изменения числа копий, которые могут быть пропущены целевой панелью FISH.
Эпидемиология

Во всем мире от множественной миеломы пострадали 488 000 человек, а в 2015 году умерло 101 100 человек. Это больше, чем 49 000 в 1990 году.
Соединенные Штаты
В США в 2016 году было зарегистрировано около 30 330 новых случаев заболевания и 12 650 случаев смерти. Эти цифры основаны на предположениях, сделанных с использованием данных за 2011 год, согласно которым число пострадавших составляет 83 367 человек, количество новых случаев - 6,1 на 100 000 человек в год, а смертность - 3,4 на 100 000 человек в год.
Множественная миелома является вторым по распространенности раком крови (10%) после неходжкинской лимфомы . На него приходится около 1,8% всех новых случаев рака и 2,1% всех случаев смерти от рака.
Множественная миелома поражает мужчин немного чаще, чем женщин. Афроамериканцы и коренные жители тихоокеанских островов имеют наибольшее зарегистрированное количество новых случаев этой болезни в Соединенных Штатах и наименьшее среди азиатов. Результаты одного исследования показали, что количество новых случаев миеломы составило 9,5 случая на 100 000 афроамериканцев и 4,1 случая на 100 000 американцев европеоидной расы. Среди афроамериканцев миелома входит в десятку основных причин смерти от рака.
Соединенное Королевство
Миелома занимает 17-е место по распространенности рака в Великобритании: в 2011 году это заболевание было диагностировано около 4800 человек. Это 16-е место по частоте смерти от рака: в 2012 году от него умерло около 2700 человек.
Другие животные
У собак, кошек и лошадей диагностирована множественная миелома.
У собак множественная миелома составляет около 8% всех гемопоэтических опухолей. Множественная миелома встречается у пожилых собак и не особенно связана ни с кобелями, ни с самками. В проведенных обзорах ни одна из пород не представлена чрезмерно. Диагностика у собак обычно откладывается из-за начальной неспецифичности и ряда возможных клинических признаков. Диагностика обычно включает исследования костного мозга, рентгеновские снимки и исследования белков плазмы. У собак исследования белка обычно показывают, что повышение уровня моноклонального гаммаглобулина составляет IgA или IgG в равном количестве случаев. В редких случаях повышение уровня глобулина составляет IgM, что называется макроглобулинемией Вальденстрема . Прогноз для первоначального контроля и возвращения к хорошему качеству жизни у собак хороший; 43% собак, начавших лечение по протоколу комбинированной химиотерапии, достигли полной ремиссии. Долгосрочная выживаемость нормальная, в среднем 540 дней. Заболевание со временем рецидивирует, становясь устойчивым к доступным методам лечения. Осложнения почечной недостаточности, сепсиса или боли могут привести к смерти животного, часто в результате эвтаназии .
Смотрите также
- Лейкемия
- Дискразия плазматических клеток, спектр нарушений плазматических клеток, которые развиваются от доброкачественных до злокачественных состояний
- Разработка аналогов талидомида
- Международный фонд миеломы
- Консорциум исследований множественной миеломы
- Фонд исследования множественной миеломы
- Макроглобулинемия Вальденстрема
использованная литература
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |