Mycobacterium abscessus -Mycobacterium abscessus
| Микобактерии абсцесс | |
|---|---|
|
|
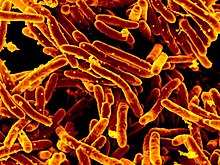
| Штамм Mycobacterium abscessus GD01, выделенный от пациента | |
|
Научная классификация |
|
| Домен: | Бактерии |
| Тип: | Актинобактерии |
| Порядок: | Коринебактерии |
| Семья: | Микобактерии |
| Род: | Микобактерии |
| Разновидность: |
М. абсцесс
|
| Биномиальное имя | |
|
Микобактерии абсцесс (Мур и Фрерихс, 1953 г.) Кусуноки и Эзаки, 1992 г.
|
|
Микобактерии abscessus комплекса (MABSC) представляет собой группу быстро растущих, с множественной лекарственной устойчивостью , нетуберкулезной микобактерий (НТМ) видовкоторые являются общими почвы и водных загрязнений. Хотякомплекс M. abscessus чаще всего вызывает хроническую инфекцию легких и инфекцию кожи и мягких тканей (SSTI), комплекс также может вызывать инфекцию почти во всех органах человека, в основном у пациентов с подавленной иммунной системой . Среди видов NTM, ответственных за заболевание, инфекцию, вызваннуюкомплексом M. abscessus , труднее лечить из-заустойчивостик противомикробным препаратам.

Описание
Клетки Mycobacterium abscessus представляют собой грамположительные неподвижные кислотоустойчивые палочки длиной около 1,0–2,5 мкм и шириной 0,5 мкм. Они могут образовывать колонии на среде Левенштейна-Йенсена, которые выглядят гладкими или шероховатыми, белыми или сероватыми и нефотохромогенными .
Физиология
M. abscessus показывает рост при 28 и 37 ° C через 7 дней, но не при 43 ° C. Он может расти на агаре МакКонки при температуре 28 ° C и даже 37 ° C. Он показывает толерантность к солевым средам (5% NaCl) и гидроксиламину 500 мг / л (яичная среда Огавы) и 0,2% пикрату (агаризованная среда Саутона). Было показано, что штаммы этого вида разрушают p- аминосалицилат антибиотика . M. abscessus также вырабатывает арилсульфатазу , но не нитратредуктазу и гидролазу Твин 80. Он показывает отрицательный результат теста на поглощение железа и отсутствие использования фруктозы , глюкозы , оксалата или цитрата в качестве единственных источников углерода.
Дифференциальные характеристики
M. abscessus и M. chelonae можно отличить от M. fortuitum или M. peregrinum по их неспособности восстанавливать нитраты и поглощать железо. Толерантность к 5% NaCl в среде Левенштейна-Йенсена, толерантность к 0,2% пикрата в агаре Саутона] и неиспользование цитрата в качестве единственного источника углерода - это характеристики, которые отличают M. abscessus от M. chelonae . M. abscessus и M. chelonae sequevar I имеют идентичную последовательность в области 54-510 16S рРНК , хотя оба вида можно дифференцировать по их последовательностям генов hsp65 , ITS или rpoB .
Генетика
Проект последовательности генома M. abscessus subsp. bolletii BD T был завершен в 2012 году. С тех пор были секвенированы геномы большого количества штаммов этого подвида , что привело к уточнению границ подвидов. В 1992 г. M. abscessus был впервые выделен в отдельный вид. В 2006 г. эта группа была разделена на три подвида: M. a. abscessus , М. а. bolletii , М.А. massiliense . В 2011 году последние два были ненадолго объединены в один подвид, но впоследствии были снова разделены после большей доступности данных о последовательности генома, что показало, что три подвида сформировали генетически разные группы.
Эти отдельные группы также соответствуют важным биологическим различиям. Клинически важные различия включают различную чувствительность к антибиотикам. M. abscessus subsp. abscessus и bolletii несут общие устойчивости к антибиотику гена, который придает устойчивость к макролидным антибиотикам , в то время как М. а. Считается, что massiliense несет нефункциональную копию, поэтому он более восприимчив к антибиотикам и легче лечится.
Патогенез
M. abscessus может вызывать заболевания легких , кожные инфекции, инфекции центральной нервной системы , бактериемию , глазные инфекции и другие, менее распространенные заболевания.
Хроническое заболевание легких чаще всего встречается у уязвимых хозяев с основным заболеванием легких, таким как муковисцидоз , бронхоэктазы и туберкулез в анамнезе . Клинические симптомы легочной инфекции различаются по масштабу и интенсивности, но обычно включают хронический кашель, часто с гнойной мокротой. Также может присутствовать кровохарканье . Системные симптомы включают недомогание , утомляемость и потерю веса при запущенном заболевании. Диагноз легочной инфекции M. abscessus требует наличия симптомов, радиологических отклонений и микробиологических культур .
M. abscessus может вызывать кожные инфекции у пациентов с иммунодефицитом, пациентов, которые недавно перенесли операцию, нанесение татуировок или иглоукалывание , а также после контакта с горячими источниками или спа. Это может быть связано с инфекциями среднего уха ( средний отит ).
Заболеваемость инфекциями, вызванными M. abscessus, со временем увеличивается. О вспышках M. abscessus сообщалось в больницах и клинических учреждениях по всему миру. В то время как вспышки, вызывающие серьезную клиническую озабоченность, связаны с передачей (скорее всего, косвенной передачей) между уязвимыми пациентами, такими как те, кто получает трансплантацию легких или лечится от муковисцидоза, о вспышках также сообщалось в клиниках, проводящих косметические операции, липосакцию , мезотерапию и внутривенное вливание клеточной терапии. , хотя это больше связано с загрязненными дезинфицирующими средствами, физиологическим раствором и инструментами, чем с контактом между пациентами.
Управление
Бактериофаговая терапия
Исследование, проведенное в 2019 году, подтвердило способность фагов убивать устойчивые бактерии, которые нельзя лечить антибиотиками. Исследовательские лаборатории объединились, чтобы найти эти фаги путем сбора, выделения и воздействия на них резистентного M. abscessus , который был изолирован от пациента в Лондоне.
В пробирке
Бактериофаг, известный как Мадди, доказал свою эффективность в уничтожении особого штамма M. abscessus (GD01), в то время как фаги, такие как ZoeJ и BPs, обладали пониженной способностью заражать GD01. Однако смесь фагов, Muddy и сконструированных версий ZoeJ и BP полностью заразила и убила GD01.
В естественных условиях
Смесь бактериофагов Muddy, ZoeJ и BP эффективно убила штамм M. abscessus in vitro . Потенциал, который это продемонстрировал, стимулировал начало лечения пациентов с инфекцией GD01. Каждые 12 часов пациенту вводили коктейль с бактериофагами.
Один день лечения показал высокий уровень бактериофагов в кровотоке. Это предполагало, что они попадают в кровоток и размножаются, чтобы заразить бактерии. О значительных побочных эффектах не сообщалось. У этого пациента были найдены нужные фаги, но другой штамм может быть чувствительным к разным фагам.
Тип штамма
Типовой штамм M. abscessus , чаще всего обозначаемый как ATCC19977, был выделен в 1953 году от инфекции коленного сустава человека с абсцессоподобными поражениями, в результате чего штамм получил название « абсцесс ». Штамм не был признан отдельным видом до 1992 года, однако, когда работа по гибридизации ДНК идентифицировала его как генетически отличный от своего родственника, M. chelonae . Геном типового поезда был опубликован в 2009 году.
ATCC 19977 = CCUG 20993 = CIP 104536 = DSM 44196 = JCM 13569 = NCTC 13031
Этимология
От латинского ab- («прочь») + cedere («идти») абсцесс назван в честь того, что жидкость покидает тело через гной. M. abscessus был впервые выделен из ягодичных абсцессов у 62-летней пациентки, которая в детстве повредила колено и 48 лет спустя заболела диссеминированной инфекцией. Вид M. bolletii , названный в честь покойного микробиолога и систематика Клода Болле , был описан в 2006 году.
Смотрите также
использованная литература
Эта статья включает текст из общественного достояния из CDC, как процитировано.
внешние ссылки
- Типовой штамм Mycobacterium abscessus в Bac Dive - база метаданных по разнообразию бактерий
- Руководство для пациентов и врачей - AIT Therapeutics
- Mabellini - аннотированный, смоделированный структурный протеом Mycobacterium abscessus
- https://www.hhmi.org/news/phage-therapy-treats-patient-with-drug-resistant-bacterial-infection
