Римонабант - Rimonabant
 | |
 | |
| Клинические данные | |
|---|---|
| AHFS / Drugs.com | Информация о лекарствах для потребителей |
| Данные лицензии | |
Категория беременности |
|
| Пути администрирования |
Устный |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Биодоступность | Неопределенный |
| Связывание с белками | Почти 100% |
| Метаболизм | Печеночный , вовлечен CYP3A4 |
| Ликвидация Период полураспада | Переменная: от 6 до 9 дней при нормальном ИМТ 16 дней при ИМТ> 30 |
| Экскреция | Фекальные (86%) и почечные (3%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard |
100.210.978 |
| Химические и физические данные | |
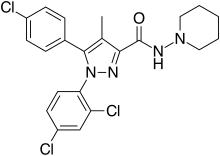
| Формула | C 22 H 21 Cl 3 N 4 O |
| Молярная масса | 463,79 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
| (проверять) | |
Римонабант (также известный как SR141716 ; торговые названия Acomplia , Zimulti ) - это лекарство от анорексии против ожирения, которое было впервые одобрено в Европе в 2006 году, но было отменено во всем мире в 2008 году из-за серьезных психиатрических побочных эффектов; он никогда не был одобрен в Соединенных Штатах. Римонабант является обратным агонистом для каннабиноидных рецепторов CB 1 и был первым препаратом , одобренным в этом классе.
История
Римонабант представляет собой селективный CB 1 рецепторов блокатор и был обнаружен и разработан с Sanofi-Aventis ;
21 июня 2006 года Европейская комиссия одобрила продажу римонабанта в Европейском союзе, который на тот момент состоял из 25 членов, в качестве лекарственного средства, отпускаемого по рецепту, для использования в сочетании с диетой и физическими упражнениями для пациентов с индексом массы тела (ИМТ) более 30 кг / м 2. 2 , или пациентов с ИМТ более 27 кг / м 2 и сопутствующими факторами риска, такими как диабет 2 типа или дислипидемия . Он был первым в своем классе, получившим одобрение в любой точке мира.
Римонабант был представлен Управлению по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) на одобрение в США в 2005 году; В 2007 году Консультативный комитет FDA по эндокринным и метаболическим препаратам (EMDAC) пришел к выводу, что Санофи-Авентис не смог продемонстрировать безопасность римонабанта, и проголосовал против рекомендации препарата против ожирения для утверждения, а через две недели компания отозвала заявку.
Препарат был одобрен в Бразилии в апреле 2007 года.
В октябре 2008 года Европейское агентство по лекарственным средствам рекомендовало приостановить действие Acomplia после того, как Комитет по лекарственным средствам для человека (CHMP) определил, что риски Acomplia перевешивают его преимущества из-за риска серьезных психических проблем, включая самоубийство. В ноябре 2008 года консультативный комитет в Бразилии также рекомендовал приостановку, и в том же месяце Санофи-Авентис приостановила продажу препарата по всему миру. Разрешение EMA было отозвано в январе 2009 года. В 2009 году Индия запретила производство и продажу этого препарата.
Побочные эффекты
Данные клинических исследований, представленные регулирующим органам, показали, что римонабант вызывал депрессивные расстройства или изменения настроения у 10% пациентов и суицидальные мысли примерно у 1%, а в Европе он противопоказан людям с любым психическим расстройством, включая депрессивных или суицидальных людей. .
Кроме того, очень частыми побочными эффектами были тошнота и инфекции верхних дыхательных путей (встречающиеся у более чем 10% людей); общие побочные эффекты (встречающиеся у 1-10% людей) включали гастроэнтерит , беспокойство, раздражительность, бессонницу и другие нарушения сна, приливы, диарею, рвоту, сухость или зуд кожи, тендинит, мышечные спазмы и спазмы, усталость, грипп. -подобные симптомы и повышенный риск падения.
Консультативный комитет FDA выразил озабоченность тем, что, основываясь на данных о животных, оказалось, что терапевтическое окно в отношении токсичности ЦНС, и в частности судорог, практически отсутствует; терапевтическая доза и доза, вызывающая судороги у животных, оказались одинаковыми.
Когда EMA проанализировало данные постмаркетингового наблюдения , оно обнаружило, что риск психических расстройств у людей, принимающих римонабант, увеличился вдвое.
Химия
Химический синтез римонабанта описывается следующим образом:
Исследование
Наряду с клиническими испытаниями при ожирении, в результате которых были получены данные, представленные регулирующим органам, римонабант также изучался в клинических испытаниях как потенциальное средство для лечения других состояний, включая диабет, атеросклероз и отказ от курения.

