Тейкопланин - Teicoplanin
 | |
| Клинические данные | |
|---|---|
| Произношение |
/ ˌ т aɪ к oʊ р л eɪ п ɪ п / TY -koh- ИГРЫ -nin |
| Торговые наименования | Таргоцид |
| AHFS / Drugs.com | Международные названия лекарств |
Категория беременности |
|
| Пути администрирования |
Внутривенно , внутримышечно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Биодоступность | 90% (с учетом IM ) |
| Связывание с белками | От 90% до 95% |
| Метаболизм | Ноль |
| Ликвидация Период полураспада | От 70 до 100 часов |
| Экскреция | Почки (97% без изменений) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| NIAID ChemDB | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула | Переменная |
| Молярная масса | От 1564,3 до 1907,7 г / моль |
| Температура плавления | 260 ° C (500 ° F) (разл.) |
| |
|
| |
Тейкопланин - это антибиотик, используемый для профилактики и лечения серьезных инфекций, вызываемых грамположительными бактериями , включая устойчивый к метициллину Staphylococcus aureus и Enterococcus faecalis . Это полусинтетический гликопептидный антибиотик со спектром действия, аналогичным ванкомицину . Его механизм действия заключается в подавлении синтеза клеточной стенки бактерий.
Тейкопланин продается компанией Санофи-Авентис под торговым наименованием Targocid . Другие торговые названия включают Ticocin, продаваемый Cipla (Индия).
Было продемонстрировано, что пероральный тейкопланин эффективен при лечении псевдомембранозного колита и диареи, вызванной Clostridium difficile , с сопоставимой эффективностью с ванкомицином.
Считается, что его сила обусловлена длиной углеводородной цепи.
Данные о восприимчивости
Тейкопланин нацелен на синтез пептидогликана, что делает его эффективным противомикробным средством против грамположительных бактерий, включая Staphylococci и Clostridium spp. Ниже представлены данные о чувствительности к МПК для нескольких значимых с медицинской точки зрения патогенов:
- Clostridium difficile : 0,06 мкг / мл - 0,5 мкг / мл
- Золотистый стафилококк : ≤0,06 мкг / мл - ≥128 мкг / мл
- Эпидермальный стафилококк : ≤0,06 мкг / мл - 32 мкг / мл
Химия
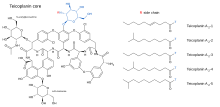
Тейкопланин (TARGOCID, продается компанией Sanofi Aventis Ltd) на самом деле представляет собой смесь нескольких соединений, пяти основных (называемых тейкопланином от A 2 -1 до A 2 -5 ) и четырех второстепенных (называемых тейкопланином от R S -1 до R S -4 ). Все тейкопланины имеют одно и то же гликопептидное ядро, называемое тейкопланином А 3 -1 - слитую кольцевую структуру, к которой присоединены два углевода ( манноза и N- ацетилглюкозамин ). Главный и второстепенный компоненты также содержат третий углеводный фрагмент - β- D- глюкозамин - и различаются только длиной и конформацией присоединенной к нему боковой цепи .
Структуры ядра тейкопланина и боковых цепей, которые характеризуют пять основных соединений тейкопланина, показаны ниже.

Тейкопланин относится к комплексу родственных природных продуктов, выделенных из ферментационного бульона штамма Actinoplanes teichomyceticus , состоящему из группы из пяти структур. Эти структуры имеют общий агликон, или ядро, состоящее из семи аминокислот, связанных пептидными и эфирными связями, с образованием четырехкольцевой системы. Эти пять структур различаются идентичностью жирной ацильной боковой цепи, присоединенной к сахару. Происхождение этих семи аминокислот в биосинтезе тейкопланина было изучено с помощью ядерного магнитного резонанса 1 H и 13 C. Исследования показывают, что аминокислоты 4-Hpg , 3-Cl-Tyr и 3-хлор-β-гидрокситирозин являются производными тирозина, а аминокислота 3,5-дигидроксифенилглицин (3,5-Dpg) - производным ацетата. Тейкопланин содержит 6 непротеиногенных аминокислот и три сахарных фрагмента, N- ацил-β-D-глюкозамин, N- ацетил-β-D-глюкозамин и D-маннозу.
Генный кластер
Изучение генетического кластера, кодирующего биосинтез тейкопланина, выявило 49 предполагаемых открытых рамок считывания (ORF), участвующих в биосинтезе, экспорте, устойчивости и регуляции соединения. Тридцать пять из этих ORF похожи на те, что обнаружены в других кластерах гликопептидных генов. Функция каждого из этих генов описана Ли и сотрудниками. Краткое описание структуры и назначения гена показано ниже.
Генная раскладка . Гены пронумерованы. Буквы L и R обозначают направление транскрипции. Наличие символа * означает, что ген обнаружен после NRP, которые представлены буквами A, B, C и D. На основании рисунка из: Li, TL .; Хуанг, Ф .; Haydock, SF; Мироненко, Т .; Leadlay, PF; Спенсер, Дж. Б. Химия и биология. 2004, 11, с. 109.
[11-левый] [10-левый] [9-левый] [8-левый] [7-левый] [6-левый] [5-левый] [4-левый] [3-левый] [2-левый] [1-R] [AR] [BR] [CR] [DR] [1 * -R] [2 * -R] [3 * -R] [4 * -R] [5 * -R] [6 * -R] [7 * -R] [8 * -R] [9 * -R] [10 * -R] [11 * -R] [12 * -R] [13 * -R] [14 * -R ] [15 * -R] [16 * -R] [17 * -R] [18 * -R] [19 * -R] [20 * -R] [21 * -R] [22 * -R] [ 23 * -R] [24 * -R] [25 * -L] [26 * -L] [27 * -R] [28 * -R] [29 * -R] [30 * -R] [31 * -R] [32 * -L] [33 * -L] [34 * -R]
| Фермент, продуцируемый последовательностью гена | Регуляторные белки | Другие ферменты | Устойчивые ферменты | Ферменты биосинтеза Β-гидрокситирозина и 4-гидроксифенилглицина | Гликозилтрансферазы | Пептид синтетазы | P450 оксигеназы | Галогеназа | Ферменты биосинтеза 3,5-дигидроксифенилглицина |
| Гены | 11, 10, 3, 2, 15 *, 16 *, 31 * | 9, 8, 1 *, 2 *, 4 *, 11 *, 13 *, 21 *, 26 *, 27 *, 30 *, 32 *, 33 *, 34 * | 7, 6, 5 | 4, 12 *, 14 *, 22 *, 23 *, 24 *, 25 *, 28 *, 29 * | 1, 3 *, 10 * | А, Б, В, D | 5 *, 6 *, 7 *, 9 * | 8 * | 17 *, 18 *, 19 *, 20 *, 23 * |
Синтез гептапептидного остова
Гептапептидный каркас тейкопланина собирается с помощью нерибосомных пептидных синтетаз (NRPS) TeiA, TeiB, TeiC и TeiD. Вместе они включают семь модулей, каждый из которых содержит несколько доменов, каждый из которых отвечает за включение одной аминокислоты. Модули 1, 4 и 5 активируют L-4-Hpg как аминоацил-AMP, модули 2 и 6 активируют L-Tyr, а модули 3 и 7 активируют L-3,5-Dpg. Активированные аминокислоты ковалентно связаны с NRPS в виде тиоэфиров с помощью кофактора фосфопантетеина, который присоединен к домену белка-носителя пептидила (PCP). Связанные с ферментом аминокислоты затем соединяются амидными связями под действием домена конденсации (C).
Гептапетид тейкопланина содержит 4 D-аминокислоты, образованные эпимеризацией активированных L-аминокислот. Каждый из модулей 2, 4 и 5 содержит домен эпимеризации (E), который катализирует это изменение. Модуль 1 не содержит домена E, и предполагается, что эпимеризация будет катализироваться доменом C. В целом, шесть из семи общих аминокислот основной цепи тейкопланина состоят из небелковых или модифицированных аминокислот. Одиннадцать ферментов координированно индуцируются для образования этих шести требуемых остатков. Тейкопланин содержит два хлорированных положения: 2 (3-Cl-Tyr) и 6 (3-Cl-β-Hty). Галогеназа Tei8 * катализирует галогенирование обоих остатков тирозина. Хлорирование происходит на уровне аминоацил-PCP во время биосинтеза, до фенольного окислительного связывания, при этом тирозин или β-гидрокситирозин могут быть субстратом хлорирования. Гидроксилирование остатка тирозина модуля 6 также происходит в транс во время сборки гептапептидного остова.
Модификация после образования гептапептидного остова
Как только гептапептидный остов сформирован, линейный промежуточный продукт, связанный с ферментом, подвергается циклизации. Исследования разрушения генов показывают, что оксигеназы цитохрома P450 являются ферментами, осуществляющими реакции связывания. X-домен в конечном модуле NRPS необходим для рекрутирования ферментов оксигеназы. OxyB образует первое кольцо путем связывания остатков 4 и 6, а OxyE затем соединяет остатки 1 и 3. OxyA соединяет остатки 2 и 4 с последующим образованием связи CC между остатками 5 и 7 посредством OxyC. Было высказано предположение, что региоселективность и селективность атропоизомера этих вероятных реакций одноэлектронного связывания обусловлены требованиями к укладке и ориентации частично перекрестно-связанных субстратов в активном центре фермента. Реакции сочетания показаны ниже.
Было показано, что специфическое гликозилирование происходит после образования гептпептидного агликона. Для гликозилирования агликона тейкопланина необходимы три отдельные гликозилтрансферазы. Tei10 * катализирует добавление GlcNAc к остатку 4 с последующим деацетилированием Tei2 *. Затем к ацильной цепи (образованной действием Tei30 * и Tei13 *) добавляется Tei11 *. Затем Tei1 добавляет второй GlcNAc к β-гидроксильной группе остатка 6 с последующим маннозилированием остатка 7, катализируемым Tei3 *.

