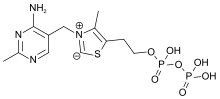
Пирофосфат тиамина - Thiamine pyrophosphate

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
2- [3 - [(4-амино-2-метилпиримидин-5-ил) метил] -4-метил-1,3-тиазол-3-иум-5-ил] этилфосфоно гидрофосфат
|
|
| Другие имена
Дифосфат тиамина
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ChemSpider | |
| MeSH | Тиамин + пирофосфат |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| C 12 H 19 N 4 O 7 P 2 S + | |
| Молярная масса | 425,314382 г / моль |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Пирофосфат тиамина ( TPP или ThPP ), или дифосфат тиамина ( ThDP ), или кокарбоксилаза - это производное тиамина (витамина B 1 ) , которое вырабатывается ферментом тиаминдифосфокиназой . Пирофосфат тиамина - кофактор , присутствующий во всех живых системах, в котором он катализирует несколько биохимических реакций.
Пирофосфат тиамина синтезируется в цитозоле и необходим в цитозоле для активности транскетолазы и в митохондриях для активности пируват-, оксоглутарат- и дегидрогеназ кетокислот с разветвленной цепью. На сегодняшний день дрожжевой переносчик ThPP (Tpc1p), человеческий Tpc и Drosophila melanogaster , были идентифицированы как ответственные за митохондриальный транспорт ThPP и ThMP. Впервые он был обнаружен в качестве важного питательного вещества ( витамина ) у людей благодаря его связи с заболеванием периферической нервной системы бери-бери , которое возникает в результате дефицита тиамина в рационе .
TPP действует как кофермент во многих ферментативных реакциях, таких как:
- Пируватдегидрогеназный комплекс
- Пируватдекарбоксилаза при ферментации этанола
- Альфа-кетоглутаратдегидрогеназный комплекс
- Комплекс дегидрогеназы аминокислот с разветвленной цепью
- 2-гидроксифитаноил-CoA лиаза
- Транскетолаза
Химия
Химически TPP состоит из пиримидинового кольца, которое связано с тиазольным кольцом, которое, в свою очередь, связано с пирофосфатной (дифосфатной) функциональной группой .
Часть молекулы TPP, которая чаще всего участвует в реакциях, - это тиазольное кольцо, содержащее азот и серу . Таким образом, тиазольное кольцо является «реагентной частью» молекулы. C2 этого кольца способен действовать как кислота , отдавая свой протон и образуя карбанион . Обычно реакции, в которых образуются карбанионы, крайне неблагоприятны, но положительный заряд четырехвалентного азота, непосредственно примыкающего к карбаниону, стабилизирует отрицательный заряд, делая реакцию намного более благоприятной. Соединение с положительными и отрицательными зарядами на соседних атомах называется илидом , поэтому иногда карбанионную форму TPP называют «илидной формой».
Механизмы реакции
В нескольких реакциях, включая реакцию пируватдегидрогеназы, альфа-кетоглутаратдегидрогеназы и транскетолазы, TPP катализирует реакцию обратимого декарбоксилирования (также известного как расщепление соединения субстрата по углерод-углеродной связи, соединяющей карбонильную группу с соседней реакционной группой - обычно карбоксильной группой. кислота или спирт ). Это достигается за четыре основных шага:
- Карбанион ТПП-илида нуклеофильно атакует карбонильную группу на субстрате. (Это образует одинарную связь между TPP и подложкой.)
- Связь мишени на подложке разрывается, и ее электроны выталкиваются в сторону TPP. Это создает двойную связь между углеродом подложки и углеродом TPP и толкает электроны в двойной связи NC в TPP полностью на атом азота, переводя его из положительной в нейтральную форму.
- В том, что по существу является обратным шагу два, электроны отталкиваются в противоположном направлении, образуя новую связь между углеродом подложки и другим атомом. (В случае декарбоксилаз это создает новую связь углерод-водород. В случае транскетолазы она атакует новую молекулу субстрата, образуя новую связь углерод-углерод.)
- В том, что по существу является обратным шагу один, связь ТФФ-субстрат разрывается, реформируя ТФФ-илид и карбонил субстрата.