Цитратлиаза АТФ - ATP citrate lyase
| Цитратлиаза АТФ человека | |||||||
|---|---|---|---|---|---|---|---|
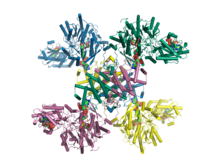 Кристаллическая структура цитратлиазы АТФ человека в комплексе с цитратом, коферментом А и Mg.ADP.
| |||||||
| Идентификаторы | |||||||
| Условное обозначение | ACLY | ||||||
| Альт. символы | ACL | ||||||
| Ген NCBI | 47 | ||||||
| HGNC | 115 | ||||||
| OMIM | 108728 | ||||||
| PDB | 3MWE, 3PFF, 5TDE, 5TDF, 5TDM, 5TDZ, 5TE1, 5TEQ, 5TES, 5TET, 6HXH, 6HXK, 6HXL, 6HXM, 6O0H, 6QFB 3MWD, 3MWE, 3PFF, 5TDE, 5TDTD, 5TDTES , 5TET, 6HXH, 6HXK, 6HXL, 6HXM, 6O0H, 6QFB | ||||||
| RefSeq | NM_001096 | ||||||
| UniProt | P53396 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 2.3.3.8 | ||||||
| Locus | Chr. 17 q21.2 | ||||||
| |||||||
Цитратлиаза АТФ (ACLY) - это фермент, который у животных представляет собой важный этап биосинтеза жирных кислот . Преобразуя цитрат в ацетил-КоА , фермент связывает углеводный обмен , который дает цитрат в качестве промежуточного продукта , с биосинтезом жирных кислот , который потребляет ацетил-КоА. У растений цитратлиаза АТФ генерирует цитозольные предшественники ацетил-КоА тысяч специализированных метаболитов , включая воски , стерины и поликетиды .
Функция
Цитратлиаза АТФ - основной фермент, ответственный за синтез цитозольного ацетил-КоА во многих тканях. Фермент представляет собой тетрамер, состоящий из идентичных субъединиц. У животных продукт, ацетил-КоА, используется в нескольких важных биосинтетических путях, включая липогенез и холестерогенез . Активируется инсулином.
У растений цитратлиаза АТФ генерирует ацетил-КоА для цитозольных метаболитов; Ацетил-КоА не переносится через субклеточные мембраны растений. Такие метаболиты включают: удлиненные жирные кислоты (используемые в маслах семян, фосфолипидах мембран , церамидных составляющих сфинголипидов , кутикуле , кутине и суберине ); флавоноиды ; малоновая кислота ; ацетилированные фенольные соединения , алкалоиды , изопреноиды , антоцианы и сахара ; и изопреноиды, производные мевалоната (например, сесквитерпены , стеролы, брассиностероиды ); малонил и ацилпроизводные (d-аминокислоты, малонилированные флавоноиды, ацилированные, пренилированные и малонированные белки). Биосинтез жирных кислот de novo у растений происходит в пластидах ; таким образом, цитратлиаза АТФ не имеет отношения к этому пути.
Реакция
Цитратлиаза АТФ отвечает за катализ превращения цитрата и кофермента А (КоА) в ацетил-КоА и оксалоацетат за счет гидролиза АТФ . В присутствии АТФ и КоА цитратлиаза катализирует расщепление цитрата с образованием ацетил-КоА, оксалоацетата , аденозиндифосфата (АДФ) и ортофосфата (P i ):
- цитрат + АТФ + КоА → оксалоацетат + Ацетил-КоА + АДФ + P i
Этому ферменту ранее был присвоен номер ЕС 4.1.3.8.
Расположение
Фермент цитозольный у растений и животных.
Структура
Фермент состоит из двух субъединиц зеленых растений (включая Chlorophyceae , Marchantimorpha , Bryopsida , Pinaceae , однодольные и эвдикоты ), видов грибов , глаукофитов , хламидомонад и прокариот .
Ферменты ACL животных гомомерные; слияние генов Acla и ACLB , вероятно , произошло в начале эволюционной истории этого царства.
АТФ-цитратлиаза млекопитающих имеет N-концевой цитрат-связывающий домен, который принимает складку Россмана , за которой следуют CoA-связывающий домен и CoA-лигазный домен и, наконец, C-концевой домен цитрат-синтазы. Разрыв между доменами связывания CoA и цитрат-синтазы образует активный сайт фермента, где связываются как цитрат, так и ацетил-кофермент A.
В 2010 году структура усеченной цитратлиазы АТФ человека была определена с помощью дифракции рентгеновских лучей с разрешением 2,10 Å . В 2019 году методом рентгеновской кристаллографии с разрешением 3,2 Å была определена полноразмерная структура человеческого ACLY в комплексе с субстратами - коферментом А, цитратом и Mg.ADP. Более того, в 2019 г. полноразмерная структура ACLY в комплексе с ингибитором была определена методами крио-ЭМ с разрешением 3,7 Å. Дополнительные структуры гетеромерных ACLY-A / B из зеленых серных бактерий Chlorobium limicola и архей Methanosaeta concilii показывают, что архитектура ACLY эволюционно консервативна . Полноразмерные структуры ACLY показали, что тетрамерный белок олигомеризуется через свой C-концевой домен. С-концевой домен не наблюдался в ранее определенных усеченных кристаллических структурах. C-концевой участок ACLY собирается в тетрамерный модуль, который структурно подобен цитрил-CoA-лиазе (CCL), обнаруженной у глубоко ветвящихся бактерий. Этот модуль CCL катализирует расщепление промежуточного соединения цитрил-КоА на продукты ацетил-КоА и оксалоацетат.
Фармакология
Действие фермента можно ингибировать с помощью кофермента А-конъюгата бемпедоевой кислоты , соединения, которое снижает уровень холестерина ЛПНП у людей. Препарат был одобрен Управлением по контролю за продуктами и лекарствами в феврале 2020 года для использования в США.
Рекомендации
дальнейшее чтение
- Ловелл С.К., Дэвис И.В., Арендалл В.Б., де Баккер П.И., Уорд Дж.М., Присант М.Г. и др. (Февраль 2003 г.). «Подтверждение структуры по геометрии Calpha: отклонения фи, пси и Сбета». Белки . 50 (3): 437–50. DOI : 10.1002 / prot.10286 . PMID 12557186 .
внешние ссылки
- Цитрат-лиаза ATP в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
Эта статья включает текст из Национальной медицинской библиотеки США , которая находится в свободном доступе .
