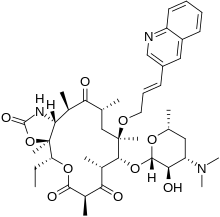
Цетромицин - Cethromycin
 | |
| Клинические данные | |
|---|---|
| Пути администрирования |
Устный |
| Код УВД | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | От 35,8 до 60% в исследованиях на животных. |
| Метаболизм | Печень |
| Ликвидация Период полураспада | 1,6, 3,0, 4,5, 5,9 и 6 часов. Мышь, Обезьяна, Крыса, Собака и Человек соответственно. |
| Экскреция | 7,0% моча 87,2% фекалии |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Химические и физические данные | |
| Формула | C 42 H 59 N 3 O 10 |
| Молярная масса | 765,945 г · моль -1 |
| 3D модель ( JSmol ) | |
| Температура плавления | От 211 до 213 ° C (от 412 до 415 ° F) |
| |
| |
|
| |
Цетромицин , торговое название Restanza (первоначально известный как ABT-773 ), представляет собой кетолидный антибиотик, который проходит исследования для лечения внебольничной пневмонии (ВП) и для профилактики постконтактной ингаляционной сибирской язвы , и ему был присвоен статус « орфанного препарата » для это указание. Первоначально открытый и разработанный Abbott , он был приобретен Advanced Life Sciences Inc. для дальнейшего развития.
1 октября 2008 г. компания Advanced Life Sciences подала в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) новую заявку на лекарство (NDA ) на цетромицин для лечения внебольничной пневмонии легкой и средней степени тяжести.
3 декабря 2008 г. компания Advanced Life Sciences объявила, что эта заявка на новый лекарственный препарат была принята для подачи FDA.
В июне 2009 года обзор Консультативного комитета FDA по противоинфекционным лекарственным средствам обнаружил недостаточные доказательства эффективности цетромицина в лечении внебольничной пневмонии, поскольку клиническое испытание фазы 3 соответствовало стандартам, которые были обновлены после клинического испытания, но за три месяца до обзора. Однако комитет посчитал препарат безопасным для использования.
