Клавулановая кислота - Clavulanic acid
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | / ˌ к L Ae v J ʊ л æ п ɪ к / |
| AHFS / Drugs.com | Международные названия лекарств |
Категория беременности |
|
| Пути администрирования |
Оральный, IV |
| Код УВД | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | «Хорошо впитывается» |
| Метаболизм | Печеночный (обширный) |
| Ликвидация Период полураспада | 1 час |
| Экскреция | Почечный (30-40%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard |
100.055.500 |
| Химические и физические данные | |
| Формула | C 8 H 9 N O 5 |
| Молярная масса | 199,162 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
| (проверять) | |
Клавулановая кислота - это β-лактамный препарат, который действует как механический ингибитор β-лактамаз . Хотя он не эффективен сам по себе в качестве антибиотика , в сочетании с антибиотиками группы пенициллина он может преодолеть устойчивость к антибиотикам у бактерий, которые секретируют β-лактамазу , которая в противном случае инактивирует большинство пенициллинов.
В наиболее распространенных препаратах клавуланат калия (клавулановая кислота в виде соли калия) сочетается с:
- амоксициллин ( ко-амоксиклав , торговые названия Аугментин, Тыцлав, Клавамокс ( ветеринарный ), Синулокс ( ветеринарный ) и другие)
- тикарциллин ( тикарцлав , торговое название тиментин)
Клавулановая кислота была запатентована в 1974 году.
Медицинское использование
Амоксициллин-клавулановая кислота является препаратом первой линии для лечения многих типов инфекций, включая инфекции носовых пазух и инфекции мочевыводящих путей, включая пиелонефрит . Отчасти это связано с его эффективностью против грамположительных бактерий, которые, как правило, сложнее контролировать, чем грамотрицательные бактерии с помощью химиотерапевтических антибиотиков.
Побочные эффекты
Использование клавулановой кислоты с пенициллинами было связано с увеличением частоты холестатической желтухи и острого гепатита во время терапии или вскоре после нее . Сопутствующая желтуха обычно проходит самостоятельно и очень редко приводит к летальному исходу.
Великобритания Комитет по безопасности лекарственных средств (CSM) рекомендует , чтобы процедуры , такие как амоксициллин / кислотные препараты клавулановых быть зарезервированы для бактериальных инфекций , вероятно, вызванных штаммами амоксициллин устойчивости β-лактамаз-продуцирующего, и что лечение обычно не должно превышать 14 дней.
Сообщений об аллергии не поступало.
Источники
Название происходит от штамма Streptomyces clavuligerus , который производит клавулановую кислоту.
Биосинтез
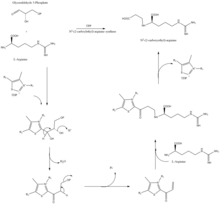
Β-лактам , как структура клавулановой кислоты выглядит структурно близок к пенициллину , но биосинтез этой молекулы включает различные биохимические пути. Клавулановая кислота продуцируется бактерией Streptomyces clavuligerus с использованием глицеральдегид-3-фосфата и L- аргинина в качестве исходных материалов. Хотя каждый из промежуточных продуктов пути известен, точный механизм всех ферментативных реакций полностью не изучен. В этом процессе в основном задействованы 3 фермента: клаваминатсинтаза , β- лактамсинтетаза и N 2 - (2-карбоксиэтил) -L-аргинин (СЕА) синтаза . Клаваминатсинтаза является негемовой оксигеназой, зависящей от железа и α-кетоглутарата, и кодируется orf5 кластера генов клавулановой кислоты . Конкретный механизм работы этого фермента до конца не изучен, но этот фермент регулирует 3 стадии в общем синтезе клавулановой кислоты. Все 3 стадии происходят в одной и той же области каталитического железосодержащего реакционного центра, но не происходят последовательно и влияют на разные области структуры клавулановой кислоты.
β-лактамсинтетаза представляет собой белок 54,5 кДа, который кодируется orf3 кластера генов клавулановой кислоты и проявляет сходство с аспарагинсинтазой - ферментами класса B. Точный механизм того, как этот фермент работает для синтеза β-лактама , не доказан, но считается, что он происходит в координации с СЕА-синтазой и АТФ .
СЕА-синтаза представляет собой белок 60,9 кДа и является первым геном, обнаруженным в кластере генов биосинтеза клавулановой кислоты, кодируемом orf2 кластера генов клавулановой кислоты. Конкретный механизм работы этого фермента все еще исследуется; однако известно, что этот фермент обладает способностью связывать глицеральдегид-3-фосфат с L-аргинином в присутствии тиаминдифосфата (TDP или тиаминпирофосфата ), что является первой стадией биосинтеза клавулановой кислоты.
История
Клавулановая кислота была открыта примерно в 1974-75 годах британскими учеными, работавшими в фармацевтической компании Beecham, из бактерий Streptomyces clavuligerus . После нескольких попыток Бичем наконец подал заявку на патентную защиту препарата в США в 1981 году, и в 1985 году были выданы патенты США 4525352, 4529720 и 4560552.
Клавулановая кислота обладает незначительной внутренней антимикробной активностью, несмотря на то, что у нее есть бета-лактамное кольцо, которое характерно для бета-лактамных антибиотиков . Однако подобие химической структуры позволяет молекуле взаимодействовать с ферментом β-лактамазой, секретируемым некоторыми бактериями, чтобы придать устойчивость к β-лактамным антибиотикам.
Клавулановая кислота является суицидным ингибитором , ковалентно связывающимся с остатком серина в активном центре β-лактамазы. Это реструктурирует молекулу клавулановой кислоты, создавая гораздо более активные формы, которые атакуют другую аминокислоту в активном центре, навсегда инактивируя ее и, таким образом, инактивируя фермент.
Это ингибирование восстанавливает антимикробную активность β-лактамных антибиотиков в отношении резистентных бактерий, секретирующих лактамазы. Несмотря на это, появились штаммы бактерий, устойчивые даже к таким комбинациям.