Бромид золота (III) - Gold(III) bromide

|
|

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Бромид золота (III)
|
|
| Другие названия
Бромид ауриновой кислоты Бромид
золота Бромид золота (III) Трибромид золота Гексабромид дигольда |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard |
100.030.582 |
|
PubChem CID
|
|
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| AuBr 3 | |
| Молярная масса | 436,69 г / моль |
| Появление | от темно-красного до черного кристаллического |
| Температура плавления | 97,5 ° С (207,5 ° F, 370,6 К) |
| Слабо растворим | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Бромид золота (III) представляет собой кристаллическое твердое вещество от темно-красного до черного цвета. Он имеет эмпирическую формулу AuBr 3 , но существует в основном в виде димера с молекулярной формулой Au 2 Br 6, в которой два атома золота соединены двумя атомами брома. Его обычно называют бромидом золота (III), трибромидом золота и редко, но традиционно, бромидом ауры, а иногда и гексабромидом диголда. Как и другие галогениды золота, это соединение уникально тем, что является координационным комплексом переходного металла группы 11, который устойчив в степени окисления три, тогда как комплексы меди или серебра сохраняются в степенях окисления один или два.
История
Первые упоминания о каких-либо исследованиях или изучении галогенидов золота относятся к началу-середине 19 века, и есть три основных исследователя, связанных с обширным исследованием этой конкретной области химии: Томсен, Шоттлендер и Крюсс.
Состав
Димер, диголд гексабромид, имеет структурные свойства, аналогичные свойствам других димерных соединений тригалогенида золота, таких как хлорид золота (III) . Золотые центры демонстрируют плоскую квадратную координацию с валентными углами примерно 90 градусов.
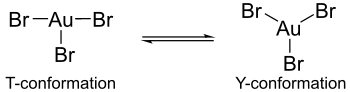
Расчеты показывают, что в гипотетических мономерных формах тригалогенидов золота эффект Яна-Теллера вызывает различия в структурах галогенидных комплексов золота. Например, бромид золота (III) содержит одну длинную и две короткие связи золото-бром, тогда как хлорид золота (III) и фторид золота (III) состоят из двух длинных и одной короткой связи золото-галоген. Более того, трибромид золота не проявляет такой же координации вокруг центрального атома золота, как трихлорид золота или трифторид золота. В последних комплексах координация проявляет Т-конформацию, но в трибромиде золота координация существует как более динамический баланс между Y-конформацией и Т-конформацией. Это различие в координации может быть связано с эффектом Яна-Теллера, но в большей степени с уменьшением π-обратной связи атомов золота с бромными лигандами по сравнению с обратной π-связью, обнаруженной с лигандами фтора и хлора. Это также уменьшение π-обратной связи, которое объясняет, почему трибромид золота менее стабилен, чем его трифторидные и трихлоридные аналоги.
Подготовка
Наиболее распространенный метод синтеза бромида золота (III) - нагревание золота и избытка жидкого брома при 140 ° C:
- 2 Au + 3 Br 2 → Au 2 Br 6
В качестве альтернативы, реакция галогенидного обмена хлорида золота (III) с бромистоводородной кислотой также оказалась успешной при синтезе бромида золота (III):
- Au 2 Cl 6 + 6 HBr → 6 HCl + Au 2 Br 6
Эта реакция вызвана образованием относительно более стабильной соляной кислоты по сравнению с бромистоводородной кислотой .
Химические свойства
Нейтральный мономер AuBr 3 , а также другие нейтральные разновидности тригалогенида золота не были выделены в газовой фазе, что указывает на то, что координационное число три не является предпочтительным. Преимущественно золото (III) демонстрирует плоско-квадратную координацию, соответствующую предпочтительному координационному числу четыре.
В частности, в растворах тригалогениды золота (III) имеют тенденцию добавлять четвертый лиганд с образованием более предпочтительного четырехкоординированного комплекса. Что касается трибромида золота, обычно покупают гидрат бромида золота (III), AuBr 3 ⋅H 2 O, где центральный атом золота имеет координационное число четыре, а не безводную форму соединения, которая демонстрирует координационную номер три.
В качестве альтернативы, если четвертый лиганд не добавлен, трибромид золота будет олигомеризоваться с образованием димерного комплекса с галогеновой мостиковой связью, упомянутого ранее.
- 2 AuBr 3 → Au 2 Br 6
Кроме того, как и хлорид золота (III) , трибромид золота является кислотой Льюиса и может образовывать несколько комплексов. Например, в присутствии бромистоводородной кислоты димер растворяется и образуется бромяуровая кислота.
- HBr (водн.) + AuBr 3 (водн.) → H + AuBr 4 - (водн.)
Димер также быстро гидролизуется во влажном воздухе.
Использует
Каталитическая химия
Бромид золота (III) используется в качестве катализатора в различных реакциях, но одно из его наиболее интересных применений находится в реакции Дильса-Альдера . В частности, соединение катализирует реакцию между единичным звеном и карбонильными соединениями с образованием шестичленного циклического соединения.
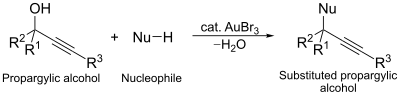
Другое каталитическое применение трибромида золота - это реакция нуклеофильного замещения пропаргиловых спиртов. В этой реакции комплекс золота действует как спирт-активирующий агент, облегчая замещение.
Обнаружение кетамина
Бромид золота (III) можно использовать в качестве реагента для тестирования на присутствие кетамина .
0,25% AuBr 3 0,1 М NaOH готовят с получением коричневато-желтого раствора. Две капли этого добавляются в пластину для пятен и добавляется небольшое количество кетамина. Смесь дает темно-фиолетовый цвет в течение приблизительно одной минуты, который превращается в темный, черно-пурпурный цвет в течение приблизительно двух минут.
Ацетаминофен , аскорбиновая кислота , героин , лактоза , маннит , морфин и сахароза вызывают мгновенное изменение цвета на пурпурный, как и другие соединения с фенольными и гидроксильными группами.
Ничто, обычно встречающееся в сочетании с кетамином, не дает такого же изменения цвета за одно и то же время.
"Первоначальный пурпурный цвет может быть следствием образования комплекса между золотом и кетамином. Причина изменения цвета с пурпурного на темно-черно-пурпурный неизвестна; однако это может быть связано с окислительно-восстановительной реакцией, которая дает небольшое количество коллоидного золота ».