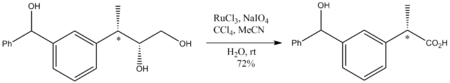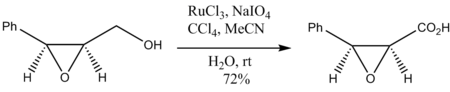Четырехокись рутения - Ruthenium tetroxide
|
|
|||
| Имена | |||
|---|---|---|---|
|
Название ИЮПАК
Оксид рутения (VIII)
|
|||
| Идентификаторы | |||
|
3D модель ( JSmol )
|
|||
| ECHA InfoCard |
100.039.815 |
||
|
PubChem CID
|
|||
| UNII | |||
|
Панель управления CompTox ( EPA )
|
|||
|
|||
|
|||
| Характеристики | |||
| RuO 4 | |||
| Молярная масса | 165,07 г / моль | ||
| Появление | желтое легко плавящееся твердое вещество | ||
| Запах | острый | ||
| Плотность | 3,29 г / см 3 | ||
| Температура плавления | 25,4 ° С (77,7 ° F, 298,5 К) | ||
| Точка кипения | 40,0 ° С (104,0 ° F, 313,1 К) | ||
| 2% мас. / Об. При 20 ° C | |||
| Растворимость в других растворителях | Растворим в четыреххлористом углероде хлороформе |
||
| Структура | |||
| четырехгранный | |||
| нуль | |||
| Опасности | |||
| Паспорт безопасности | внешний лист MSDS | ||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
|
Родственные соединения
|
RuO 2 RuCl 3 |
||
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|||
|
|
|||
| Ссылки на инфобоксы | |||
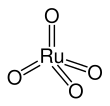
Четырехокись рутения представляет собой неорганическое соединение с формулой RuO 4 . Это желтое летучее твердое вещество, плавящееся при комнатной температуре. Имеет запах озона. Образцы обычно черные из-за примесей. Аналогичный OsO 4 более широко используется и известен. Одним из немногих растворителей, в которых RuO 4 образует стабильные растворы, является CCl 4 .
Подготовка
RuO 4 получают путем окисления рутения (III) хлорида с NaIO 4 .
- 8 Ru 3+ (водн.) + 5 IO 4 - (водн.) + 12 H 2 O (l) → 8 RuO 4 (т.) + 5 I - (водн.) + 24 H + (водн.)
Из-за дороговизны, токсичности и высокой реакционной способности RuO 4 он часто образуется in situ и используется в каталитических количествах в органических реакциях с использованием субстехиометрического количества предшественника рутения (III) или - (IV) и стехиометрического количества метапериодат натрия в качестве конечного окислителя для непрерывной регенерации небольших количеств RuO 4 . В типичных реакциях с RuO 4 в качестве окислителя многие формы рутения служат прекурсорами RuO 4 , чаще всего используются RuCl 3 · x H 2 O или RuO 2 · x H 2 O.
Структура
RuO 4 образует две кристаллические структуры, одна с кубической симметрией, а другая с моноклинной симметрией, изотипная OsO 4 . Молекула имеет тетраэдрическую геометрию с расстояниями Ru – O от 169 до 170 пм.
Использует
Выделение рутения из руд
Основная коммерческая ценность RuO 4 заключается в том, что он является промежуточным продуктом при производстве соединений рутения и металла из руд. Как и другие металлы платиновой группы (МПГ), рутений встречается в низких концентрациях и часто смешивается с другими МПГ. Вместе с OsO 4 он отделяется от других МПГ путем перегонки экстракта, окисленного хлором. Рутений отделяют от OsO 4 путем уменьшения RuO 4 с соляной кислотой , процесс , который использует высоко положительный восстановительный потенциал для [RuO 4 ] 0 / - пара.
Органическая химия
RuO 4 представляет особую ценность в органической химии, поскольку окисляет практически любой углеводород. Например, он окисляет адамантан до 1-адамантанола. Поскольку это такой агрессивный окислитель, условия реакции должны быть мягкими, обычно при комнатной температуре. Хотя RuO 4 является сильным окислителем, он не нарушает стереоцентры , которые не окисляются. Иллюстративным является окисление следующего диола до карбоновой кислоты :
Окисление эпоксидных спиртов также происходит без разрушения эпоксидного кольца:
В более мягких условиях окислительная реакция дает вместо этого альдегиды . RuO 4 легко превращает вторичные спирты в кетоны . Хотя аналогичные результаты могут быть достигнуты с другими более дешевыми окислителями , такими как PCC - или ДМСО основанные окислители, RuO - идеально подходит , когда очень энергичный окислитель требуется, но должны быть сохранены мягкие условия. Он используется в органическом синтезе для окисления внутренних алкинов до 1,2- дикетонов и концевых алкинов вместе с первичными спиртами до карбоновых кислот . При использовании таким образом оксид рутения (VIII) используется в каталитических количествах и регенерируется путем добавления периодата натрия к хлориду рутения (III) и смеси растворителей, состоящей из ацетонитрила , воды и четыреххлористого углерода . RuO 4 легко расщепляет двойные связи с образованием карбонильных продуктов аналогично озонолизу . OsO 4 , более известный окислитель, который структурно похож на RuO 4 , не расщепляет двойные связи, вместо этого образуя продукты вицинального диола. Однако при коротком времени реакции и тщательно контролируемых условиях RuO 4 также можно использовать для дигидроксилирования.
Поскольку RuO 4 разрушает «двойные связи» аренов (особенно богатых электронами) путем дигидроксилирования и расщепления связи CC способом, которым могут воспользоваться немногие другие реагенты, его можно использовать в качестве реагента «снятия защиты» для карбоновых кислот, которые замаскированы как арильные группы (обычно фенил или п- метоксифенил ). Поскольку образующиеся фрагменты сами легко окисляются RuO 4 , значительная часть атомов углерода арена подвергается исчерпывающему окислению с образованием диоксида углерода. Следовательно, для достижения полного превращения в карбоновую кислоту требуется несколько эквивалентов концевого окислителя (часто более 10 эквивалентов на арильное кольцо), что ограничивает практичность превращения.
Несмотря на то, что он используется в качестве прямого окислителя , из-за относительно высокой стоимости RuO 4 также используется каталитически с охлаждающим агентом. Для окисления циклических спиртов с RuO 4 в качестве катализатора и броматом в качестве окислителя в основных условиях RuO 4 сначала активируется гидроксидом:
- RuO 4 + OH - → HRuO 5 -
Реакция протекает через гликолятный комплекс.
Другое использование
Четырехокись рутения является потенциальным окрашивающим агентом. Он используется для выявления скрытых отпечатков пальцев, превращаясь в коричневый / черный диоксид рутения при контакте с жирными маслами или жирами, содержащимися в сальных загрязнителях отпечатка.
Выбросы газов при ядерных авариях
Из-за очень высокой летучести четырехокиси рутения ( RuO
4) радиоактивные изотопы рутения с их относительно коротким периодом полураспада считаются вторыми по опасности газообразными изотопами после йода-131 в случае выброса в результате ядерной аварии. Двумя наиболее важными изотопами рутения являются 103 Ru и 106 Ru. У них период полураспада 39,6 дня и 373,6 дня соответственно.
использованная литература
дальнейшее чтение
- Коттон, С.А. (1997). Химия драгоценных металлов . Лондон: Чепмен и Холл. ISBN 978-0-7514-0413-5.
- Фермер, В .; Велтон, Т. (2002). «Окисление спиртов в замещенных имидазолиевых ионных жидкостях с использованием рутениевых катализаторов». Зеленая химия . 4 (2): 97. DOI : 10.1039 / B109851A .
- Singh, B .; Шривастава, С. (1991). «Кинетика и механизм катализируемого четырехокись рутения окисления циклических спиртов броматом в основании». Химия переходных металлов . 16 (4): 466. DOI : 10.1007 / BF01129466 .
- Кортни, JL; Swansbor, KF (1972). «Окисление четырехокиси рутения». Обзоры теоретической и прикладной химии . 22 : 47.