Аконитаза - Aconitase
| аконитатгидратаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
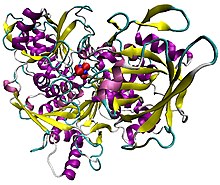 Иллюстрация аконитазы свиньи в комплексе с кластером [Fe 4 S 4 ]. Белок окрашен вторичной структурой, атомы железа синего цвета, а серы - красного цвета.
| |||||||||
| Идентификаторы | |||||||||
| ЕС нет. | 4.2.1.3 | ||||||||
| № CAS | 9024-25-3 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
| Семейство аконитаз (аконитатгидратаза) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Структура аконитазы.
| |||||||||
| Идентификаторы | |||||||||
| Символ | Аконитаза | ||||||||
| Pfam | PF00330 | ||||||||
| ИнтерПро | IPR001030 | ||||||||
| ПРОФИЛЬ | PDOC00423 | ||||||||
| SCOP2 | 1aco / SCOPe / SUPFAM | ||||||||
| |||||||||
Аконитаза (аконитатгидратазы; EC 4.2.1.3 ) является ферментом , который катализирует стерео-специфической изомеризация из цитрата в изоцитрат с помощью цис - aconitate в кислотах цикла трикарбонового , A не- редокса - -активный процесс.
Структура
Аконитаза, отображаемая в структурах на правом поле этой страницы, имеет две немного разные структуры, в зависимости от того, активирована она или деактивирована. В неактивном виде его структура разделена на четыре домена. Считая от N-конца , только первые три из этих доменов вовлечены в тесные взаимодействия с кластером [3Fe-4S], но активный сайт состоит из остатков из всех четырех доменов, включая более крупный C-концевой домен. Кластер Fe-S и анион SO 4 2- также находятся в активном центре. Когда фермент активируется, он получает дополнительный атом железа, создавая кластер [4Fe-4S]. Однако структура остального фермента почти не изменилась; законсервированные атомы между двумя формами находятся по существу в одних и тех же положениях с разницей до 0,1 ангстрем.
Функция
В отличие от большинства белков железо-сера, которые функционируют как переносчики электронов, кластер железо-сера аконитазы непосредственно реагирует с субстратом фермента. Аконитаза имеет активный кластер [Fe 4 S 4 ] 2+ , который может превращаться в неактивную форму [Fe 3 S 4 ] + . Было показано, что три остатка цистеина (Cys) являются лигандами центра [Fe 4 S 4 ]. В активном состоянии лабильный ион железа кластера [Fe 4 S 4 ] координируется не Cys, а молекулами воды.
Железо реагирует элемент-связывающий белок (ИРЭ-ВР) и 3-изопропилмалат дегидратаз (α-изопропилмалат изомеразы; EC 4.2.1.33 ), фермент , катализирующий вторую стадию в биосинтезе лейцина , известен аконитазом гомологов. Регуляторные элементы железа (IRE) представляют собой семейство некодирующих структур «стебель-петля» из 28 нуклеотидов, которые регулируют накопление железа, синтез гема и захват железа. Они также участвуют в связывании рибосом и контролируют оборот мРНК (деградацию). Специфический белок-регулятор, IRE-BP, связывается с IRE как в 5 ', так и в 3' областях, но только с РНК в апо-форме, без кластера Fe-S. Экспрессия IRE-BP в культивируемых клетках показала, что белок функционирует либо как активная аконитаза, когда клетки насыщены железом, либо как активный связывающий РНК белок, когда клетки истощены по железу. Мутантные IRE-BP, в которых любой или все три остатка Cys, участвующие в образовании Fe-S, заменены серином , не обладают аконитазной активностью, но сохраняют РНК-связывающие свойства.
Аконитаза ингибируется фторацетатом , поэтому фторацетат ядовит. Фторацетат, входящий в цикл лимонной кислоты, может незаметно войти в качестве фторцитрата. Однако аконитаза не может связывать этот субстрат, и, таким образом, цикл лимонной кислоты останавливается. Кластер железа и серы очень чувствителен к окислению супероксидом .
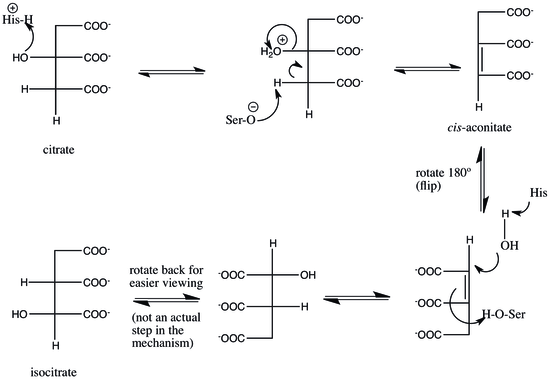
Механизм
Аконитаза использует механизм дегидратации-гидратации. Каталитические остатки представляют собой His-101 и Ser-642. His-101 протонирует гидроксильную группу на C3 цитрата, позволяя ему уйти в виде воды, а Ser-642 одновременно отщепляет протон на C2, создавая двойную связь между C2 и C3 и образуя так называемый промежуточный цис -конитат ( две карбоксильные группы по двойной связи являются цис ). Атом углерода, из которого удален водород, - это тот, который образовался из оксалоацетата на предыдущем этапе цикла лимонной кислоты, а не тот, который произошел от ацетил-КоА , даже если эти два атома углерода эквивалентны, за исключением того, что один является « про- R "и другие" про- S "(см. Prochirality ). В этот момент промежуточное звено поворачивается на 180 °. Это вращение называется «переворот». Говорят, что из-за этого интермедиата он переходит из «цитратного режима» в «изоцитратный режим».
Как именно происходит этот переворот, остается спорным. Одна из теорий состоит в том, что на стадии ограничения скорости этого механизма цис -аконитат высвобождается из фермента, а затем повторно присоединяется в изоцитратном режиме для завершения реакции. Этот этап ограничения скорости гарантирует, что в конечном продукте формируется правильная стереохимия , в частности (2R, 3S). Другая гипотеза заключается в том, что цис- кононитат остается связанным с ферментом, пока он переключается из цитратного в изоцитратный режим.
В любом случае переворачивание цис- кононитата позволяет стадиям дегидратации и гидратации происходить на противоположных сторонах промежуточного продукта. Аконитаза катализирует транс- элиминирование / добавление воды, и переворот гарантирует формирование правильной стереохимии в продукте. Для завершения реакции остатки серина и гистидина меняют свое первоначальное каталитическое действие: гистидин, теперь основной, отрывает протон от воды, направляя его как нуклеофил для атаки на C2, а протонированный серин депротонируется двойным цис- конатитатом. связь для завершения гидратации с образованием изоцитрата.
Члены семьи
У человека аконитазы экспрессируются в бактериях. Люди экспрессируют следующие два изофермента аконитазы :
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.
использованная литература
дальнейшее чтение
- Фришман Д., Хентце М. В. (июль 1996 г.). «Сохранение остатков аконитазы, выявленных с помощью анализа множественных последовательностей. Влияние на взаимосвязь структура / функция» . Европейский журнал биохимии / FEBS . 239 (1): 197–200. DOI : 10.1111 / j.1432-1033.1996.0197u.x . PMID 8706708 .
внешние ссылки
- Аконитаза в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Proteopedia аконитаза - структура аконитаза в интерактивном 3D