Альдостерон-синтаза - Aldosterone synthase
Альдостерон-синтаза , также называемая стероид-18-гидроксилазой , кортикостерон-18-монооксигеназой или P450C18 , представляет собой фермент цитохрома P450 стероид- гидроксилазы, участвующий в биосинтезе минералокортикоидного альдостерона и других стероидов. Фермент катализирует последовательное гидроксилирование стероидной угловой метильной группы у C18 после начального 11β-гидроксилирования (фермент обладает активностью стероид-18-гидроксилазы, а также активностью стероид-11-бета-гидроксилазы). Он кодируется геном CYP11B2 у человека.
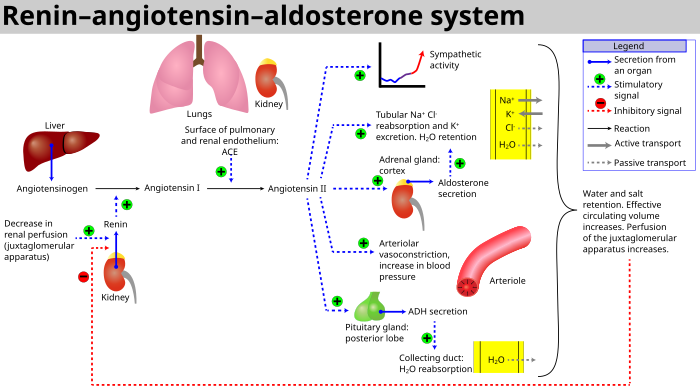
Альдостерон-синтаза - это белок, который экспрессируется только в клубочковой зоне коры надпочечников и в первую очередь регулируется ренин-ангиотензиновой системой . Это единственный фермент, способный синтезировать альдостерон у человека, и он играет важную роль в балансе электролитов и артериальном давлении .
Генетика
Альдостерон-синтаза кодируется на хромосоме 8q 22 геном CYP11B2. Ген содержит 9 экзонов и охватывает примерно 7000 пар оснований ДНК. CYP11B2 тесно связан с CYP11B1 . Два гена демонстрируют 93% гомологии друг с другом и оба кодируются на одной и той же хромосоме. Исследования показали, что ионы кальция активируют факторы транскрипции на CYP11B2 посредством четко определенных взаимодействий в 5'-фланкирующей области CYP11B2.
Альдостерон-синтаза является членом суперсемейства ферментов цитохрома P450. Белки цитохрома P450 представляют собой монооксигеназы, которые катализируют многие реакции, участвующие в метаболизме лекарств и синтезе холестерина , стероидов и других липидов .
Функция
Альдостерон-синтаза - это фермент, который обладает активностью стероид-18-гидроксилазы, а также активностью стероид-11-бета-гидроксилазы. Активность 18-гидроксилазы заключается в катализе последовательных гидроксилирований стероидной угловой метильной группы по C18.
В то время как стероид 11β-гидроксилаза (кодируемая геном CYP11B1 ) катализирует гидроксилирование только в положении 11 бета (в основном 11-дезоксикортикостерона и 11-дезоксикортизола), альдостерон-синтаза (кодируемая геном CYP11B2 ) катализирует синтез альдостерона из дезоксикортикостерона, который последовательно перерабатывает требует гидроксилирования в положениях 11 бета и 18 и окисления в положении 18.
Предполагается, что адренокортикотропный гормон играет роль в регуляции альдостерон-синтазы, вероятно, за счет стимуляции синтеза 11-дезоксикортикостерона, который является исходным субстратом ферментативного действия альдостерон-синтазы.
Метаболизм
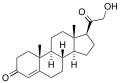
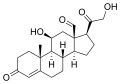
Альдостерон-синтаза превращает 11-дезоксикортикостерон в кортикостерон , в 18-гидроксикортикостерон и, наконец, в альдостерон :
В метаболизме человека биосинтез альдостерона во многом зависит от метаболизма холестерина . Холестерин метаболизируется так называемым ранним путем синтеза альдостерона и представляет собой гидроксилированный (20R, 22R) -дигидроксихолестерин, который затем метаболизируется как прямой предшественник прегненолона . Затем прегненолон может идти по одному из двух путей, которые включают метаболизм прогестерона или биосинтез тестостерона и эстрадиола . Альдостерон синтезируется путем метаболизма прогестерона .
В потенциальном случае, когда альдостерон-синтаза не метаболически активна, в организме накапливается 11-дезоксикортикостерон . Это увеличивает задержку солей, что приводит к усилению гипертонии .
Субстраты
Альдостерон-синтаза проявляет различную каталитическую активность при метаболизме своих субстратов. Вот некоторые из субстратов, сгруппированных по каталитической активности фермента:
- сильный:
- средний:
- слабый:
- очень слаб:
Дефицит метилоксидазы
Недостаток метаболически активной альдостерон-синтазы приводит к недостаточности кортикостерон-метилоксидазы I и II типа. Дефицит клинически характеризуется потерей солей, недостаточностью роста и задержкой роста. Неактивные белки вызваны аутосомно-рецессивным наследованием дефектных генов CYP11B2, в которых генетические мутации нарушают ферментативную активность альдостерон-синтазы. Недостаточная активность альдостерон-синтазы приводит к нарушению биосинтеза альдостерона, в то время как кортикостерон в клубочковой зоне чрезмерно продуцируется как при дефиците кортикостерон-метилоксидазы I, так и II типа. Оба дефицита кортикостерон-метилоксидазы разделяют этот эффект, однако тип I вызывает общий дефицит 18-гидроксикортикостерона, в то время как тип II вызывает его избыточное производство.
Ферментативное ингибирование
Ингибирование альдостерон-синтазы в настоящее время исследуется в качестве лекарственного средства для лечения гипертонии , сердечной недостаточности и почечных заболеваний . Деактивация ферментативной активности снижает концентрацию альдостерона в плазме и тканях, что снижает зависимые от минералокортикоидных рецепторов и независимые эффекты в сердечно-сосудистых и почечных органах-мишенях. Показано, что ингибирование приводит к снижению концентрации альдостерона в плазме и моче на 70-80%, быстрой коррекции гипокалиемии , умеренному снижению артериального давления и повышению активности ренина в плазме у пациентов, соблюдающих диету с низким содержанием натрия. Текущие медицинские исследования сосредоточены на синтезе ингибиторов альдостерон-синтазы второго поколения для создания идеально селективного ингибитора, поскольку текущий перорально вводимый LCl699 оказался неспецифичным для альдостерон-синтазы.
Смотрите также
использованная литература
дальнейшее чтение
- Хельмберг А. (август 1993 г.). «Гены-близнецы и эндокринные заболевания: гены CYP21 и CYP11B». Acta Endocrinologica . 129 (2): 97–108. DOI : 10,1530 / acta.0.1290097 . PMID 8372604 .
- Slight SH, Джозеф Дж., Ганджам В.К., Вебер К.Т. (июнь 1999 г.). «Внеадреналовые минералокортикоиды и сердечно-сосудистая ткань». Журнал молекулярной и клеточной кардиологии . 31 (6): 1175–84. DOI : 10,1006 / jmcc.1999.0963 . PMID 10371693 .
- Стоуассер М., Гунасекера Т.Г., Гордон Р.Д. (декабрь 2001 г.). «Семейные разновидности первичного альдостеронизма». Клиническая и экспериментальная фармакология и физиология . 28 (12): 1087–90. DOI : 10.1046 / j.1440-1681.2001.03574.x . PMID 11903322 . S2CID 23091842 .
- Падманабхан Н., Падманабхан С., Коннелл Дж. М. (декабрь 2000 г.). «Генетическая основа сердечно-сосудистых заболеваний - ренин-ангиотензин-альдостероновая система как парадигма» . Журнал системы ренин-ангиотензин-альдостерон . 1 (4): 316–24. DOI : 10,3317 / jraas.2000.060 . PMID 11967817 .
- Лифтон Р.П., Длухи Р.Г., Пауэрс М., Рич Г.М., Гуткин М., Фалло Ф. и др. (Сентябрь 1992 г.). «Наследственная гипертензия, вызванная дупликациями химерных генов и эктопической экспрессией альдостерон-синтазы». Генетика природы . 2 (1): 66–74. DOI : 10.1038 / ng0992-66 . PMID 1303253 . S2CID 975796 .
- Мицуучи Ю., Кавамото Т., Наики Ю., Мияхара К., Тода К., Курибаяси И. и др. (Январь 1992 г.). «Врожденно дефектный биосинтез альдостерона у людей: участие точечных мутаций гена P-450C18 (CYP11B2) у пациентов с дефицитом CMO II». Сообщения о биохимических и биофизических исследованиях . 182 (2): 974–9. DOI : 10.1016 / 0006-291X (92) 91827-D . PMID 1346492 .
- Паско Л., Керноу К.М., Слуцкер Л., Коннелл Дж. М., Шпайзер П. У., Нью-Мичиган, Белый ПК (сентябрь 1992 г.). «Гиперальдостеронизм, подавляемый глюкокортикоидами, является результатом гибридных генов, созданных в результате неравных кроссоверов между CYP11B1 и CYP11B2» . Труды Национальной академии наук Соединенных Штатов Америки . 89 (17): 8327–31. Bibcode : 1992PNAS ... 89.8327P . DOI : 10.1073 / pnas.89.17.8327 . PMC 49911 . PMID 1518866 .
- Паско Л., Курноу К.М., Слуцкер Л., Рёслер А., White PC (июнь 1992 г.). «Мутации в гене человеческого CYP11B2 (альдостерон-синтазы), вызывающие дефицит кортикостерон-метилоксидазы II» . Труды Национальной академии наук Соединенных Штатов Америки . 89 (11): 4996–5000. Bibcode : 1992PNAS ... 89.4996P . DOI : 10.1073 / pnas.89.11.4996 . PMC 49215 . PMID 1594605 .
- Кавамото Т., Мицуучи Ю., Тода К., Йокояма Ю., Мияхара К., Миура С. и др. (Февраль 1992 г.). «Роль стероид-11-бета-гидроксилазы и стероид-18-гидроксилазы в биосинтезе глюкокортикоидов и минералокортикоидов у человека» . Труды Национальной академии наук Соединенных Штатов Америки . 89 (4): 1458–62. Bibcode : 1992PNAS ... 89.1458K . DOI : 10.1073 / pnas.89.4.1458 . PMC 48470 . PMID 1741400 .
- Curnow KM, Tusie-Luna MT, Pascoe L, Natarajan R, Gu JL, Nadler JL, White PC (октябрь 1991 г.). «Продукт гена CYP11B2 необходим для биосинтеза альдостерона в коре надпочечников человека» . Молекулярная эндокринология . 5 (10): 1513–22. DOI : 10.1210 / Менд-5-10-1513 . PMID 1775135 .
- Кавайното Т., Мицуучи Ю., Охниши Т., Итикава Ю., Йокояма Ю., Сумимото Н. и др. (Ноябрь 1990 г.). «Клонирование и экспрессия кДНК человеческого цитохрома P-450aldo в связи с первичным альдостеронизмом». Сообщения о биохимических и биофизических исследованиях . 173 (1): 309–16. DOI : 10.1016 / S0006-291X (05) 81058-7 . PMID 2256920 .
- Mornet E, Dupont J, Vitek A, White PC (декабрь 1989 г.). «Характеристика двух генов, кодирующих человеческий стероид 11 бета-гидроксилазу (P-450 (11) бета)» . Журнал биологической химии . 264 (35): 20961–7. DOI : 10.1016 / S0021-9258 (19) 30030-4 . PMID 2592361 .
- Марцев С.П., Чащин В.Л., Ахрем А.А. (февраль 1985 г.). «[Реконструкция и исследование мультиферментной системы с помощью 11 стероидов бета-гидроксилазы]». Биохимия . 50 (2): 243–57. PMID 3872685 .
- Шизута Ю., Кавамото Т., Мицуучи Ю., Мияхара К., Рёслер А., Улик С., Имура Х. (январь 1995 г.). «Врожденные ошибки биосинтеза альдостерона у человека». Стероиды . 60 (1): 15–21. DOI : 10.1016 / 0039-128X (94) 00023-6 . PMID 7792802 . S2CID 23433739 .
- Мицуучи Ю., Кавамото Т., Мияхара К., Улик С., Мортон Д.Х., Наики Ю. и др. (Февраль 1993 г.). «Врожденно дефектный биосинтез альдостерона у людей: инактивация гена P-450C18 (CYP11B2) из-за делеции нуклеотидов у пациентов с дефицитом CMO I». Сообщения о биохимических и биофизических исследованиях . 190 (3): 864–9. DOI : 10.1006 / bbrc.1993.1128 . PMID 8439335 .
- Фарделла К.Э., Родригес Х., Монтеро Дж., Чжан Дж., Виньоло П., Рохас А. и др. (Декабрь 1996 г.). «Генетическая изменчивость P450c11AS у чилийских пациентов с гипертензией с низким содержанием ренина». Журнал клинической эндокринологии и метаболизма . 81 (12): 4347–51. DOI : 10,1210 / jc.81.12.4347 . PMID 8954040 .
- Номото С., Масса Дж., Митани Ф., Ишимура Й., Мияхара К., Тода К. и др. (Май 1997 г.). «Дефицит CMO I, вызванный точечной мутацией в экзоне 8 гена CYP11B2 человека, кодирующего стероид-18-гидроксилазу (P450C18)». Сообщения о биохимических и биофизических исследованиях . 234 (2): 382–5. DOI : 10.1006 / bbrc.1997.6651 . PMID 9177280 .
- Taymans SE, Pack S, Pak E, Torpy DJ, Zhuang Z, Stratakis CA (март 1998 г.). «Человеческий CYP11B2 (альдостерон-синтаза) отображается на хромосоме 8q24.3» . Журнал клинической эндокринологии и метаболизма . 83 (3): 1033–6. DOI : 10,1210 / jc.83.3.1033 . PMID 9506770 .
внешние ссылки
- Альдостерон + синтаза в медицинских предметных рубриках Национальной медицинской библиотеки США (MeSH)
- Расположение генома человека CPN2 и страница сведений о гене CPN2 в браузере генома UCSC .
- Расположение генома человека CYP11B2 и страница сведений о гене CYP11B2 в браузере генома UCSC .