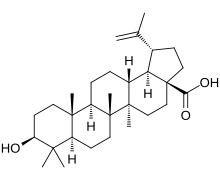
Бетулиновая кислота - Betulinic acid
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
(3β) -3-Гидрокси-lup-20 (29) -ен-28-овая кислота
|
|
|
Предпочтительное название IUPAC
(1 R , 3a S , 5a R , 5b R , 7a R , 9 S , 11a R , 11b R , 13a R , 13b R ) -9-гидрокси-5a, 5b, 8,8,11a-пентаметил-1- (проп-1-ен-1-ил) икозагидро-3a H -циклопента [ a ] хризен-3a-карбоновая кислота |
|
| Другие названия
Бетулиновая кислота
Майрин |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard |
100.006.773 |
| Номер ЕС | |
|
PubChem CID
|
|
| UNII | |
|
|
|
|
| Характеристики | |
| С 30 Н 48 О 3 | |
| Молярная масса | 456,711 г · моль -1 |
| Температура плавления | От 316 до 318 ° C (от 601 до 604 ° F; от 589 до 591 K) |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Бетулиновая кислота представляет собой встречающийся в природе пентациклический тритерпеноид, который обладает антиретровирусными , противомалярийными и противовоспалительными свойствами, а также недавно обнаруженным потенциалом в качестве противоракового агента путем ингибирования топоизомеразы . Он содержится в коре нескольких видов растений, в основном белой березы ( Betula pubescens ), от которой он получил свое название, а также бердерева ( Ziziphus mauritiana ), самолечения ( Prunella vulgaris ), тропических плотоядных растений Triphyophyllum peltatum и Ancistrocladus heyneanus , Diospyros leucomelas , представитель семейства хурмы , Tetracera boiviniana , джамбул ( Syzygium formosanum ), цветущая айва ( Pseudocydonia sinensis , бывший Chaenomeles sinensis KOEHNE ), розмарин и Pulsatilla chin .
Противоопухолевое действие
В 1995 году о бетулиновой кислоте сообщили как о селективном ингибиторе меланомы человека . Затем было продемонстрировано, что он индуцирует апоптоз в нейробластоме человека in vitro и in vivo в модельных системах. Одно время он находился в процессе разработки лекарств при поддержке программы Rapid Access to Intervention Development Национального института рака . Кроме того, было обнаружено, что бетулиновая кислота активна in vitro против нейроэктодермальных ( нейробластома , медуллобластома , саркома Юинга ) и злокачественных опухолей головного мозга, карциномы яичников , в клетках лейкемии человека HL-60 и злокачественных клеточных линий плоскоклеточной карциномы головы и шеи SCC25 и SCC9. Напротив, эпителиальные опухоли, такие как рак груди , толстой кишки , мелкоклеточного рака легких и почечно-клеточного рака , а также клетки Т-клеточного лейкоза полностью не реагировали на лечение бетулиновой кислотой.
Установлено, что действие бетулиновой кислоты как противоракового агента при раке груди зависит от каннабиноидного рецептора . Бетулиновая кислота действует как антагонист CB 1 и агонист CB 2 .
Способ действия
Что касается механизма действия бетулиновой кислоты, мало что известно о ее антипролиферативном и индуцирующем апоптоз механизмах. В нейроэктодермальных опухолевых клетках апоптоз, вызванный бетулиновой кислотой, сопровождается активацией каспаз , изменениями митохондриальной мембраны и фрагментацией ДНК . Каспазы продуцируются как неактивные проферменты , которые протеолитически процессируются до их активных форм. Эти протеазы могут взаимодействовать в протеолитических каскадах, в которых каспазы активируют себя и друг друга. Инициирование каскада каспаз может привести к активации эндонуклеаз, таких как ДНКаза, активируемая каспазой (CAD). После активации CAD способствует деградации ДНК. Бетулиновая кислота вызывает апоптоз путем прямого воздействия на митохондрии, что приводит к высвобождению цитохрома-С, который, в свою очередь, регулирует активацию каспазы «ниже по течению». Бетулиновая кислота обходит резистентность к CD95 и доксорубицин- опосредованному апоптозу из-за другого молекулярного механизма апоптоза, индуцированного бетулиновой кислотой.
Роль p53 в апоптозе, вызванном бетулиновой кислотой, противоречива. Фульда предположил p53-независимый механизм апоптоза, основанный на отсутствии накопления p53 дикого типа, обнаруженного при обработке бетулиновой кислотой, тогда как белок p53 дикого типа сильно увеличился после обработки доксорубицином. Предложение подтверждается исследованиями Раисовой. С другой стороны, Рибер предположил, что бетулиновая кислота оказывает ингибирующее действие на метастатическую меланому человека частично за счет увеличения p53.
Исследование также продемонстрировало преимущественный апоптотический эффект бетулиновой кислоты на метастатические клетки меланомы C8161 с большей фрагментацией ДНК и остановкой роста и более ранней потерей жизнеспособности, чем их неметастатический аналог C8161 / neo 6.3. Сравнивая бетулиновую кислоту с другими методами лечения, Зуко продемонстрировал, что она менее чем на 10% эффективнее доксорубицина и продемонстрировала антипролиферативную активность in vitro в отношении линий клеток меланомы и немеланомы, включая те, которые устойчивы к доксорубицину. В нормальной линии клеток дерматобласта человека бетулиновая кислота была от половины до одной пятой токсичнее доксорубицина. Способность бетулиновой кислоты вызывать два разных эффекта (цитотоксический и цитостатический) на два клона, происходящих от одного и того же метастаза меланомы человека, предполагает, что развитие клонов, устойчивых к этому агенту, будет более маловероятным, чем к обычным цитотоксическим препаратам. Более того, несмотря на более низкую эффективность по сравнению с доксорубицином, бетулиновая кислота, по-видимому, является селективной в отношении опухолевых клеток с минимальной токсичностью в отношении нормальных клеток. Эффект бетулиновой кислоты на клеточные линии меланомы сильнее, чем ее ингибирующий рост эффект на первичные меланоциты. Исследование комбинации бетулиновой кислоты с γ-облучением показало явно аддитивные эффекты и указывало, что они различаются по способам действия.
Этерификация бетулиновой кислоты C-3 привела к открытию бевиримата , ингибитора созревания ВИЧ-1 , запатентованного Rhone-Poulenc (теперь Sanofi-Aventis). Однако клиническая разработка была остановлена из-за плохих фармакодинамических свойств.
Биосинтез
Saccharomyces cerevisiae был разработан для производства бетулиновой кислоты мевалонатным путем со сквален-2,3-эпоксидом в качестве промежуточного продукта. Ацетил-СоА превращается в сквален посредством использования редуктазы 3-гидрокси-3-метилглутарил-КоА (HMGR) и бифункциональным фарнезил-дифосфат фарнезилтрансферазы и сквален - синтазы (ERG9) и окисление NADPH в NADP + . Это затем дополнительно окисленный с помощью сквален монооксигеназной (ERG1) к сквален - 2,3-эпоксида. Это циклизуют лупеолу по Резуховидке Таль лупеолы синтазы (AtLUP1). Наконец, лупеол превращается в бетулиновую кислоту через монооксигеназу P450 (CrAO) Catharanthus roseus при окислении НАДФН до НАДФ + .
Противоопухолевые производные
Основное неудобство для будущей клинической разработки бетулиновой кислоты и аналогов заключается в их плохой растворимости в водных средах, таких как сыворотка крови и полярные растворители, используемые для биоанализов. Чтобы обойти эту проблему водорастворимости и улучшить фармакологические свойства, многие производные были синтезированы и оценены на цитотоксическую активность. Одно исследование показало, что модификации C-20 приводят к потере цитотоксичности. Другое исследование продемонстрировало важность присутствия группы -COOH, поскольку соединения, замещенные в этом положении, такие как лупеол и метил бетулинат, были менее активны в отношении меланомы человека, чем бетулиновая кислота. Более того, некоторые производные C-28 аминокислот и фталатов C-3 проявляли более высокую цитотоксическую активность против линий раковых клеток с улучшенной селективной токсичностью и растворимостью в воде. Чаттерджи и др. получили 28-O-β-D-глюкопиранозид бетулиновой кислоты путем микробной трансформации с использованием видов Cunninghamella , тогда как Baglin et al. получил его путем органического синтеза. Этот глюкозид не проявлял какой-либо значительной активности in vitro в отношении клеточных линий меланомы человека (MEL-2) и колоректальной аденокарциномы человека (HT-29), что подтверждает важность функции карбоновой кислоты для сохранения цитотоксичности. Недавно Gauthier et al. синтезировал серию 3- O- гликозидов бетулиновой кислоты, которые проявляли сильную противораковую активность in vitro против линий раковых клеток человека.

