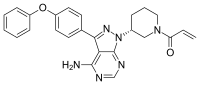
Ибрутиниб - Ibrutinib
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Имбрувица и др. |
| Другие имена | PCI-32765, CRA-032765 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a614007 |
| Данные лицензии | |
Категория беременности |
|
| Пути администрирования |
Внутрь ( капсулы ) |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Связывание с белками | 97,3% |
| Метаболизм | Печеночные ( CYP3A и CYP2D6 ) |
| Ликвидация Период полураспада | 4–6 часов |
| Экскреция | Кал (80%), моча (10%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard |
100.232.543 |
| Химические и физические данные | |
| Формула | C 25 H 24 N 6 O 2 |
| Молярная масса | 440,507 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
Ибрутиниб , продаваемый, среди прочего, под торговой маркой Imbruvica , представляет собой низкомолекулярный препарат, который подавляет пролиферацию и выживание В-клеток путем необратимого связывания тирозинкиназы белка Брутона (BTK). Блокирование BTK подавляет путь B-клеточного рецептора , который часто аномально активен при B-клеточном раке . Поэтому ибрутиниб используется для лечения таких видов рака, включая лимфому из клеток мантии , хронический лимфоцитарный лейкоз и макроглобулинемию Вальденстрема .
Он включен в Список основных лекарственных средств Всемирной организации здравоохранения . Он доступен как универсальный препарат .
Медицинское использование
Ибрутиниб используется для лечения хронического лимфолейкоза (ХЛЛ), макроглобулинемией Вальденстрема , а в качестве второй линии терапии для мантии клеточной лимфомы , маргинальной зоны лимфомы и хронический трансплантат против хозяина . Ингибирование BTK ибрутинибом нарушает сигнальный путь BCR, который является ключевой зависимостью злокачественных B-клеток, но было показано, что ингибирование BTK также препятствует передаче сигналов CD40, адгезии и миграции B-клеток.
В Соединенных Штатах ибрутиниб показан для лечения взрослых с лимфомой из клеток мантии (MCL), которые ранее получали хотя бы одну терапию, взрослых с хроническим лимфолейкозом (CLL) / малой лимфоцитарной лимфомой (SLL) с делецией 17p или без нее, взрослых с макроглобулинемией Вальденстрема (WM), взрослые с лимфомой маргинальной зоны (MZL), которым требуется системная терапия и которые получали по крайней мере одну предшествующую терапию на основе анти-CD20, взрослые с хронической болезнью трансплантата против хозяина (cGVHD) после неудачи одной или нескольких линий системной терапии.
Это лечение первой линии для пациентов с ХЛЛ, которым требуется лечение и которым недавно поставлен диагноз. Его также можно использовать при рецидивах ХЛЛ.
Побочные эффекты
Очень частые (частота> 10%) побочные эффекты включают пневмонию , инфекцию верхних дыхательных путей , синусит , кожную инфекцию, низкое количество нейтрофилов , низкое количество тромбоцитов , головную боль, кровотечение, синяки, диарею, рвоту, воспаление рта и губ , тошноту, запор. , сыпь, боль в суставах , мышечные спазмы, скелетно-мышечная боль, лихорадка и отек .
Общие (частота 1–10%) побочные эффекты включают сепсис , инфекцию мочевыводящих путей , немеланомный рак кожи ( базальноклеточный рак , плоскоклеточный рак ), низкое количество лейкоцитов , низкое количество лимфоцитов , интерстициальное заболевание легких , синдром лизиса опухоли, высокий уровень мочевого пузыря. уровень кислоты , головокружение , помутнение зрения, фибрилляция предсердий , субдуральная гематома , кровотечение из носа, небольшие синяки из разорванных кровеносных сосудов , высокое кровяное давление , крапивница , покраснение или покраснение кожи.
Фармакология
Биодоступность ибрутиниба при пероральном приеме составляет 3,9% натощак, 8,4% после еды и 15,9% после употребления грейпфрутового сока .
Механизм
Ибрутиниб - мощный необратимый ингибитор тирозинкиназы Брутона (BTK). Он образует ковалентную связь с остатком цистеина C481 в активном сайте BTK, что приводит к устойчивому ингибированию ферментативной активности BTK. BTK является важной сигнальной молекулой пути рецептора B-клеточного антигена (BCR), который играет роль в патогенезе нескольких B-клеточных злокачественных новообразований, включая лимфому из мантийных клеток (MCL), диффузную крупноклеточную B-клеточную лимфому (DLBCL), фолликулярная лимфома и хронический лимфолейкоз (ХЛЛ). Доклинические исследования показали, что ибрутиниб эффективно подавляет пролиферацию и выживаемость злокачественных В-клеток in vivo, а также миграцию клеток и адгезию субстрата in vitro.
В ранних клинических исследованиях было описано, что активность ибрутиниба включает быстрое снижение лимфаденопатии, сопровождающееся преходящим лимфоцитозом , что позволяет предположить, что препарат может оказывать прямое воздействие на возвращение клеток или миграцию к факторам в тканевом микроокружении.
В доклинических исследованиях клеток хронического лимфоцитарного лейкоза (ХЛЛ) сообщалось, что ибрутиниб способствует апоптозу, ингибирует пролиферацию, а также предотвращает реакцию клеток ХЛЛ на стимулы выживания, обеспечиваемые микросредой. Это также приводит к снижению уровня MCL1 (антиапоптотический белок) в злокачественных В-клетках. Обработка активированных клеток CLL ибрутинибом приводила к ингибированию фосфорилирования тирозина BTK, а также эффективно устраняла нижестоящие пути выживания, активированные этой киназой, включая ERK1 / 2 , PI3K и NF-κB . Кроме того, ибрутиниб ингибировал пролиферацию клеток CLL in vitro, эффективно блокируя сигналы выживания, поступающие в клетки CLL извне из микроокружения, включая растворимые факторы ( BAFF , IL-6 , IL-4 и TNF-α ), взаимодействие фибронектина и контакт со стромальными клетками.
Сообщалось также, что ибрутиниб снижает хемотаксис клеток хронического лимфоцитарного лейкоза по отношению к хемокинам CXCL12 и CXCL13 и ингибирует клеточную адгезию после стимуляции рецептора B-клеток (BCR). Кроме того, ибрутиниб подавляет экспрессию CD20 (мишень ритуксимаба / офатумумаба ), воздействуя на ось CXCR4 / SDF1. Вместе эти данные согласуются с механистической моделью, согласно которой ибрутиниб блокирует передачу сигналов BCR, что приводит клетки к апоптозу и / или нарушает миграцию клеток и их прилипание к защитному микроокружению опухоли.
История
Ибрутиниб был создан учеными Celera Genomics в качестве инструментального средства для изучения функции BTK; он ковалентно связывает свою мишень, что идеально подходит для реагента, но обычно не считается идеальным для лекарств.
В 2006 году, в ходе приобретения программы, ориентированной на HDAC, у Celera после того, как ее собственная первоначальная программа исследований провалилась, Pharmacyclics также приобрела программу обнаружения низкомолекулярных ингибиторов BTK от Celera за 2 миллиона долларов наличными и 1 миллион долларов на складе и назвала инструмент составом. PCI-32765. В 2011 году, после завершения фазы II испытаний препарата, Johnson & Johnson и Pharmacyclics согласились участвовать в совместной разработке препарата, и J&J выплатила Pharmacyclics авансом 150 миллионов долларов и 825 миллионов долларов в качестве промежуточных этапов. Pharmacyclics была приобретена AbbVie в мае 2015 года, и Abbvie прогнозировала глобальные продажи в 1 миллиард долларов США в 2016 году и 5 миллиардов долларов в 2020 году.
Он был одобрен Управлением по контролю за продуктами и лекарствами США (FDA) 13 ноября 2013 года для лечения лимфомы из клеток мантии . 12 февраля 2014 г. FDA расширило разрешенное использование ибрутиниба на хронический лимфолейкоз (ХЛЛ). Он был одобрен для лечения макроглобулинемии Вальденстрема в 2015 году.
В марте 2015 года Pharmacyclics и AbbVie договорились, что Abbvie приобретет Pharmacyclics за 21 миллиард долларов; сделка была завершена в мае того же года.
В марте 2016 года в США было одобрено новое показание к применению ибрутиниба для пациентов с хроническим лимфолейкозом (ХЛЛ).
В мае 2016 года в США было одобрено новое показание к применению ибрутиниба при хроническом лимфолейкозе (ХЛЛ) и малой лимфоцитарной лимфоме (SLL).
В январе 2017 года в США было одобрено новое показание к применению ибрутиниба для лечения взрослых с рецидивирующей / рефрактерной (R / R) лимфомой маргинальной зоны (MZL), которым требуется системная терапия и которые ранее получали как минимум одно анти-CD20- основанная терапия.
В августе 2017 года FDA одобрило новое показание для ибрутиниба для лечения болезни трансплантат против хозяина . Это был первый препарат, одобренный FDA для лечения этого состояния.
В феврале 2018 года таблетированная форма ибрутиниба была одобрена для использования в США.
В августе 2018 года ибрутиниб в сочетании с ритуксимабом был одобрен в США для лечения взрослых с макроглобулинемией Вальденстрема (WM), редким и неизлечимым типом неходжкинской лимфомы (НХЛ).
В январе 2019 года ибрутиниб в комбинации с обинутузумабом был одобрен для лечения взрослых с ранее нелеченым хроническим лимфолейкозом / малой лимфоцитарной лимфомой (CLL / SLL).
В апреле 2020 года FDA расширило показания ибрутиниба, включив его комбинацию с ритуксимабом для начального лечения взрослых с хроническим лимфолейкозом (CLL) или малой лимфоцитарной лимфомой (SLL). Одобрение было основано на исследовании E1912 (NCT02048813), рандомизированном, многоцентровом, открытом, активно контролируемом исследовании 2: 1 ибрутиниба с ритуксимабом по сравнению с флударабином, циклофосфамидом и ритуксимабом (FCR) у 529 взрослых субъектов в возрасте 70 лет или моложе с ранее нелеченный CLL или SLL, требующий системной терапии.
Расходы
Типичная стоимость ибрутиниба в США составляет около 148 000 долларов в год. Предварительное исследование, посвященное PK / PD, показало, что люди потенциально могут быть переведены на более дешевый и более дешевый режим ибрутиниба без потери эффективности; однако данных, показывающих эффективность более низких доз, опубликовано не было.
В первой половине 2018 года Janssen Pharmaceutica и Pharmacyclics представили новую формулу таблеток для однократной дозы с фиксированной ценовой структурой и прекратили выпуск капсул. Это вызвало бурю негодования, поскольку считалось, что стоимость препарата для среднего пациента выросла в три раза. Пациенты, получающие одобренные и рекомендованные FDA дозы, не увидят ни изменения цен, ни снижения цен в связи со структурой цен на таблетки.
С тех пор Janssen Pharmaceutica и Pharmacyclics отменили решение о прекращении выпуска капсульной композиции с лекарством, которое в настоящее время доступно как в капсульной, так и в таблетированной форме.
Ибрутиниб был добавлен в Австралийскую схему предоставления фармацевтических льгот в 2018 году.
Дженерик ибрутиниб был добавлен в Индийскую схему фармацевтических льгот в 2020 году.
использованная литература
внешние ссылки
- «Ибрутиниб» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- Ибрутиниб , Словарь лекарств Национального института рака
