Гидроксид магния - Magnesium hydroxide

|
|
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Гидроксид магния
|
|
| Другие имена
Дигидроксид магния
Молоко магнезии |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard |
100.013.792 |
| Номер ЕС | |
| Номер E | E528 (регуляторы кислотности, ...) |
| 485572 | |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| Мг (ОН) 2 | |
| Молярная масса | 58,3197 г / моль |
| Появление | Белое твердое вещество |
| Запах | Без запаха |
| Плотность | 2,3446 г / см 3 |
| Температура плавления | 350 ° С (662 ° F, 623 К) разлагается |
|
Произведение растворимости ( K уд )
|
5,61 × 10 −12 |
| −22,1 · 10 −6 см 3 / моль | |
|
Показатель преломления ( n D )
|
1,559 |
| Состав | |
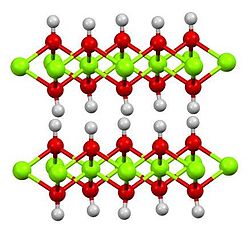
| Шестиугольный, hP3 | |
| П 3 м1 №164 | |
|
а = 0,312 нм, с = 0,473 нм
|
|
| Термохимия | |
|
Теплоемкость ( C )
|
77,03 Дж / моль · К |
|
Стандартная мольная
энтропия ( S |
64 Дж · моль −1 · K −1 |
|
Std энтальпия
формации (Δ F H ⦵ 298 ) |
−924,7 кДж · моль −1 |
|
Свободная энергия Гиббса (Δ f G ˚)
|
−833,7 кДж / моль |
| Фармакология | |
| A02AA04 ( ВОЗ ) G04BX01 ( ВОЗ ) | |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Пиктограммы GHS |

|
| Сигнальное слово GHS | Предупреждение |
| H315 , H319 , H335 | |
| P261 , P280 , P305 + 351 + 338 , P304 + 340 , P405 , P501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| Смертельная доза или концентрация (LD, LC): | |
|
LD 50 ( средняя доза )
|
8500 мг / кг (крыса, перорально) |
| Родственные соединения | |
|
Другие анионы
|
Оксид магния |
|
Другие катионы
|
|
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Гидроксид магния - это неорганическое соединение с химической формулой Mg (OH) 2 . Встречается в природе как минерал брусит . Это белое твердое вещество с низкой растворимостью в воде ( K уд = 5,61 × 10 -12 ). Гидроксид магния является обычным компонентом антацидов , таких как молоко магнезии .
Подготовка
Объединение раствора многих солей магния с щелочной водой вызывает осаждение твердого Mg (OH) 2 :
- Mg 2+ + 2OH - → Mg (OH) 2
В промышленных масштабах Mg (OH) 2 получают путем обработки морской воды известью (Ca (OH) 2 ). 600 м 3 (158 503 галлона США) морской воды дает около одной тонны Mg (OH) 2 . Ca (OH) 2 гораздо более растворим, чем Mg (OH) 2 , поэтому последний осаждается в виде твердого вещества:
Использует
Предшественник MgO
Большая часть Mg (OH) 2 , производимого промышленным способом, а также небольшое количество добываемого преобразуется в плавленую магнезию (MgO). Магнезия ценна, потому что она является плохим проводником электричества и отличным проводником тепла.
Здоровье
Метаболизм
Гидроксид магния используется в виде суспензии как антацидное или слабительное средство , в зависимости от концентрации.
В качестве антацида гидроксид магния вводится взрослым в дозе примерно 0,5–1,5 г и действует путем простой нейтрализации , при которой ионы гидроксида из Mg (OH) 2 соединяются с кислыми ионами H + , вырабатываемыми в форме соляной кислоты париетальными клетками. в желудке , чтобы производить воду.
В качестве слабительного средства гидроксид магния используется в дозировке 2–5 г и действует по-разному. Во-первых, Mg 2+ плохо всасывается из кишечного тракта, поэтому он вытягивает воду из окружающих тканей путем осмоса . Это увеличение содержания воды не только смягчает кал, но и увеличивает объем фекалий в кишечнике (внутрипросветный объем), что естественным образом стимулирует перистальтику кишечника . Кроме того, ионы Mg 2+ вызывают высвобождение холецистокинина (ХЦК), что приводит к внутрипросветному накоплению воды, электролитов и увеличению перистальтики кишечника. Некоторые источники утверждают, что сами гидроксид-ионы не играют значительной роли в слабительных эффектах молока магнезии, поскольку основные растворы (т.е. растворы гидроксид-ионов) не являются сильным слабительным, а неосновные растворы Mg 2+ , такие как MgSO. 4 , одинаково сильные слабительные, родинка за родинкой.
Лишь небольшое количество магния из гидроксида магния обычно всасывается в кишечнике (если только он не испытывает дефицита магния). Однако магний в основном выводится почками, поэтому длительное ежедневное употребление магнезиального молока человеком, страдающим почечной недостаточностью, теоретически может привести к гипермагниемии . Неабсорбированный препарат выводится с калом; абсорбированный препарат быстро выводится с мочой.

История молока магнезии
4 мая 1818 года американский изобретатель Джон Каллен получил патент (№ X2952) на гидроксид магния. В 1829 году сэр Джеймс Мюррей использовал «концентрированный раствор жидкой магнезии» собственного дизайна для лечения боли в животе лорда-лейтенанта Ирландии маркиза Англси. Это было настолько успешным (рекламируемое в Австралии и одобренное Королевским колледжем хирургов в 1838 году), что он был назначен врачом-резидентом Англси и двумя последующими лордами-лейтенантами и посвящен в рыцари. Его продукт с жидкой магнезией был запатентован через два года после его смерти в 1873 году.
Термин «магнезийное молоко» впервые использовал Чарльз Генри Филлипс в 1872 году для обозначения суспензии гидроксида магния, составленной примерно с 8 % масс. / Об . Оно продавалось под торговой маркой Phillips 'Milk of Magnesia для использования в лечебных целях.
Хотя название могло когда-то принадлежать GlaxoSmithKline , регистрации USPTO показывают, что «Молоко магнезии» и «Молоко магнезии Филлипса» были присвоены Bayer с 1995 года. В Великобритании небрендовое (родовое) название из «Молока магнезии» и «Молока магнезии Филипса» является «Крем магнезии» (смесь гидроксида магния, BP ).
Он был использован в первом короткометражном фильме Стивена Спилберга « Амблин» .
Как пищевая добавка
Он добавляется непосредственно в пищу человека, и утверждается , как правило , признан безопасным в FDA . Он известен как номер E E528 .
Гидроксид магния продается для медицинского применения в виде жевательных таблеток, капсул, порошка и жидких суспензий , иногда с ароматизаторами. Эти продукты продаются как антациды для нейтрализации желудочного сока и облегчения расстройства желудка и изжоги . Это также слабительное средство для облегчения запоров . Осмотическая сила магнезии действует как слабительное, вытягивая жидкости из организма. Высокие дозы могут вызвать диарею и истощить запасы калия в организме , что иногда приводит к мышечным спазмам .
Некоторые продукты гидроксида магния, продаваемые для использования в качестве антацидов (например, маалокс ), разработаны для минимизации нежелательных слабительных эффектов за счет включения гидроксида алюминия , который ингибирует сокращения гладкомышечных клеток в желудочно-кишечном тракте, тем самым уравновешивая сокращения, вызванные осмотическим действием гидроксид магния.
Другое нишевое использование
Гидроксид магния также входит в состав антиперспиранта . Гидроксид магния полезен против язвы (афтозный язвы) при местном применении.
Очистки сточных вод
Порошок гидроксида магния используется в промышленности для нейтрализации кислых сточных вод. Это также компонент метода Biorock для создания искусственных рифов .
Огнестойкий материал
Природный гидроксид магния ( брусит ) коммерчески используется как антипирен. Гидроксид магния, чаще всего используемый в промышленности, получают синтетическим путем. Как и гидроксид алюминия, твердый гидроксид магния обладает дымовыми и огнезащитными свойствами. Это свойство связано с эндотермическим разложением, которому он подвергается при 332 ° C (630 ° F):
- Mg (OH) 2 → MgO + H 2 O
Тепло, поглощаемое реакцией, замедляет возгорание, задерживая возгорание связанного вещества. Вытекающая вода разбавляет горючие газы. Обычно гидроксид магния в качестве антипирена включает добавки в изоляцию кабелей (например, кабели для высококачественных автомобилей, подводных лодок , Airbus A380 и Sony PlayStation ), изоляционные пластмассы, кровельные покрытия (например, Олимпийский стадион в Лондоне ) и различные огнезащитные покрытия. Другие минеральные смеси, которые используются в аналогичных антипиренах, представляют собой природные смеси хантита и гидромагнезита .
Минералогия

Брусит , минеральная форма Mg (OH) 2, обычно встречающаяся в природе, также встречается в глинистых минералах 1: 2: 1, среди прочего, в хлорите , в котором он занимает промежуточное положение, обычно заполненное одновалентными и двухвалентными катионами, такими как Na +. , K + , Mg 2+ и Ca 2+ . Как следствие, прослойки хлорита цементируются бруситом и не могут набухать или сжиматься.
Брусит, в котором некоторые из катионов Mg 2+ были замещены катионами Al 3+ , становится положительно заряженным и составляет основную основу слоистого двойного гидроксида (СДГ). Минералы СДГ, такие как гидроталькит, являются мощными анионными сорбентами, но относительно редки в природе.
Брусит также может кристаллизоваться в цементе и бетоне при контакте с морской водой . Действительно, катион Mg 2+ является вторым по распространенности катионом в морской воде, сразу после Na + и перед Ca 2+ . Поскольку брусит представляет собой набухающий минерал, он вызывает локальное объемное расширение, ответственное за растягивающее напряжение в бетоне. Это приводит к образованию трещин и трещин в бетоне, что ускоряет его разрушение в морской воде.
По той же причине доломит нельзя использовать в качестве строительного заполнителя для изготовления бетона. Реакция карбоната магния со свободными гидроксидами щелочных металлов, присутствующими в поровой воде цемента, также приводит к образованию расширяющегося брусита.
- MgCO 3 + 2 NaOH → Mg (OH) 2 + Na 2 CO 3
Эта реакция, одна из двух основных реакций щелочь – агрегат (AAR), также известна как реакция щелочь – карбонат .


