Матери против декапентаплегического гомолога 4 - Mothers against decapentaplegic homolog 4
SMAD4 , также называемый членом семейства SMAD 4 , Матери против декапентаплегического гомолога 4 , или DPC4 (удаленный при раке поджелудочной железы-4) является высококонсервативным белком, присутствующим у всех многоклеточных животных . Он принадлежит к семейству белков факторов транскрипции SMAD , которые действуют как медиаторы передачи сигнала TGF-β. TGF - beta семейства цитокинов регулирует важнейшие процессы в течение всего жизненного цикла многоклеточных, причем важную роль в процессе развития эмбриона, гомеостаза тканей, регенерации и иммунной регуляции.
SMAD 4 принадлежит к группе co-SMAD ( общий медиатор SMAD), второму классу семейства SMAD. SMAD4 - единственный известный co-SMAD у большинства многоклеточных животных. Он также принадлежит к семейству белков Дарвина, которые модулируют членов суперсемейства белков TGFβ , семейства белков, которые все играют роль в регуляции клеточных ответов. Млекопитающие SMAD4 является гомологом из Drosophila белка « Матери против decapentaplegic » по имени Медея.
SMAD4 взаимодействует с R-Smads, такими как SMAD2 , SMAD3 , SMAD1 , SMAD5 и SMAD8 (также называемым SMAD9), с образованием гетеротримерных комплексов. Попадая в ядро, комплекс SMAD4 и двух R-SMADS связывается с ДНК и регулирует экспрессию различных генов в зависимости от клеточного контекста. Внутриклеточные реакции с участием SMAD4 запускаются связыванием на поверхности клеток факторов роста из семейства TGFβ . Последовательность внутриклеточных реакций с участием SMADS называется путем SMAD или путем трансформирующего фактора роста бета (TGF-β), поскольку последовательность начинается с распознавания TGF-β клетками.
Ген
У млекопитающих SMAD4 кодируется геном, расположенным на 18 хромосоме . У человека ген SMAD4 содержит 54 829 пар оснований и расположен от пары № 51 030 212 до пары 51 085 041 в области 21.1 хромосомы 18.
Протеин
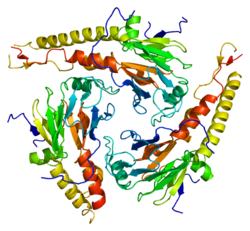
SMAD4 представляет собой полипептид из 552 аминокислот с молекулярной массой 60,439 Да . SMAD4 имеет два функциональных домена, известных как MH1 и MH2 .
Комплекс двух SMAD3 (или двух SMAD2) и одного SMAD4 связывается непосредственно с ДНК посредством взаимодействия их доменов MH1. Эти комплексы рекрутируются в сайты по всему геному факторами транскрипции, определяющими клеточный клон (LDTF), которые определяют контекстно-зависимую природу действия TGF-β. Раннее понимание специфичности связывания ДНК белков Smad было получено в результате скрининга связывания олигонуклеотидов, который идентифицировал палиндромный дуплекс 5'-GTCTAGAC-3 'как высокоаффинную связывающую последовательность для доменов SMAD3 и SMAD4 MH1. Другие мотивы также были идентифицированы в промоторах и энхансерах. Эти дополнительные сайты содержат мотив CAGCC и консенсусные последовательности GGC (GC) | (CG), последние также известны как сайты 5GC. Мотивы 5GC широко представлены в виде кластеров сайтов в SMAD-связанных областях по всему геному. Эти кластеры также могут содержать сайты CAG (AC) | (CC). Комплекс SMAD3 / SMAD4 также связывается с элементами промотора TPA-чувствительного гена, которые имеют мотив последовательности TGAGTCAG.
Структуры
Комплексы домена MH1 с мотивами ДНК
Первой структурой SMAD4, связанной с ДНК, был комплекс с палиндромным мотивом GTCTAGAC. Недавно также были определены структуры домена MH1 SMAD4, связанного с несколькими мотивами 5GC. Во всех комплексах взаимодействие с ДНК включает консервативную β-шпильку, присутствующую в домене MH1. Шпилька частично гибкая в растворе, а ее высокая степень конформационной гибкости позволяет распознавать различные последовательности из 5 п.н. Эффективные взаимодействия с GC-сайтами происходят только в том случае, если нуклеотид G расположен глубоко в большой рощице и устанавливает водородные связи с гуанидиниевой группой Arg81. Это взаимодействие способствует дополнительному поверхностному контакту между шпилькой, связывающей ДНК Smad, и большой бороздой ДНК. Другие прямые взаимодействия включают Lys88 и Gln83. Рентгеновская кристаллическая структура доменов Trichoplax adhaerens SMAD4 MH1, связанных с мотивом GGCGC, указывает на высокую сохранность этого взаимодействия у многоклеточных животных.
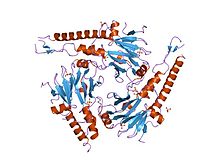
Доменные комплексы MH2
Домен MH2, соответствующий С-концу , отвечает за распознавание рецептора и ассоциацию с другими SMAD. Он взаимодействует с доменом MH2 R-SMADS и образует гетеродимеры и гетеротримеры . Некоторые опухолевые мутации, обнаруженные в SMAD4, усиливают взаимодействия между доменами MH1 и MH2.
Номенклатура и происхождение названия
SMAD являются высококонсервативными у разных видов, особенно в N-концевом домене MH1 и C-концевом домене MH2 . Белки SMAD являются гомологами как белка MAD дрозофилы, так и белка SMA C. elegans . Название представляет собой комбинацию двух. Во время исследования дрозофилы было обнаружено, что мутация в гене MAD у матери репрессировала ген decapentaplegic в эмбрионе. Была добавлена фраза «Матери против», поскольку матери часто создают организации, выступающие против различных проблем, например, « Матери против вождения в нетрезвом виде» (MADD), что отражает «усиление материнского эффекта dpp »; и основан на традиции необычного именования в исследовательском сообществе. SMAD4 также известен как DPC4, JIP или MADH4.
Функция и механизм действия
SMAD4 - это белок, который определен как важный эффектор в пути SMAD. SMAD4 служит посредником между внеклеточными факторами роста из семейства TGFβ и генами внутри ядра клетки . Аббревиатура co в co-SMAD означает общий посредник . SMAD4 также определяется как преобразователь сигналов.
В пути TGF-β димеры TGF-β распознаются трансмембранным рецептором, известным как рецептор типа II. Как только рецептор типа II активируется связыванием TGF-β, он фосфорилирует рецептор типа I. Рецептор типа I также является рецептором клеточной поверхности . Затем этот рецептор фосфорилирует регулируемый внутриклеточным рецептором SMADS (R-SMADS), такой как SMAD2 или SMAD3. Затем фосфорилированный R-SMADS связывается с SMAD4. Ассоциация R-SMADs-SMAD4 представляет собой гетеромерный комплекс. Этот комплекс переместится из цитоплазмы в ядро: это транслокация. SMAD4 может образовывать гетеротримерные, гетерогексамерные или гетеродимерные комплексы с R-SMADS.
SMAD4 является субстратом киназы Erk / MAPK и GSK3 . Стимуляция пути FGF ( фактора роста фибробластов ) приводит к фосфорилированию Smad4 с помощью Erk канонического сайта MAPK, расположенного на треонине 277. Это событие фосфорилирования оказывает двойное влияние на активность Smad4. Во-первых, он позволяет Smad4 достичь пика транскрипционной активности путем активации регулируемого фактором роста домена активации транскрипции, расположенного в линкерной области Smad4, SAD (Smad-Activation Domain). Во-вторых, MAPK праймирует Smad4 для GSK3- опосредованного фосфорилирования, которое вызывает ингибирование транскрипции, а также генерирует фосфодегрон, используемый в качестве места стыковки бета-трансдуцином, содержащим повторы убиквитина E3 ( бета-TrCP ), который полиубиквитинирует Smad4 и нацеливает его на деградацию в протеасоме. . Было высказано предположение, что фосфорилирование Smad4 GSK3 регулирует стабильность белка во время прогрессирования рака поджелудочной железы и толстой кишки .
В ядре гетеромерный комплекс связывает промоторы и взаимодействует с активаторами транскрипции. Комплексы SMAD3 / SMAD4 могут напрямую связывать SBE. Эти ассоциации слабые и требуют дополнительных факторов транскрипции, таких как члены семейства AP-1 , TFE3 и FoxG1, для регулирования экспрессии генов .
Многие лиганды TGFβ используют этот путь, и впоследствии SMAD4 участвует во многих клеточных функциях, таких как дифференцировка , апоптоз , гаструляция , эмбриональное развитие и клеточный цикл .
Клиническое значение
Генетические эксперименты, такие как нокаут гена (KO), которые заключаются в модификации или инактивации гена, могут быть проведены для того, чтобы увидеть влияние дисфункционального SMAD 4 на исследуемый организм. Часто эксперименты проводят на домашней мыши ( Mus musculus ).
Было показано , что у мышей KO из SMAD4 , в зернистых клетках , которые секретируют гормоны и факторы роста в течение ооцитов развития, подвергаются преждевременному лютеинизацию и выражать более низкие уровни фолликулостимулирующего гормона рецепторов (FSHR) и более высокие уровни лютеинизирующего гормона рецепторов (LHR). Это может быть частично связано с нарушением эффектов костного морфогенетического белка-7, поскольку BMP-7 использует сигнальный путь SMAD4.
Делеции в генах, кодирующих SMAD1 и SMAD5 , также были связаны с метастазирующими опухолями гранулезных клеток у мышей.
SMAD4 часто мутирует при многих раковых заболеваниях. Мутация может быть унаследована или приобретена в течение жизни человека. В случае передачи по наследству мутация затрагивает как соматические клетки, так и клетки репродуктивных органов. Если мутация SMAD 4 приобретена, она будет существовать только в определенных соматических клетках. Действительно, SMAD 4 синтезируется не всеми клетками. Белок присутствует в клетках кожи, поджелудочной железы, толстой кишки, матки и эпителия. Он также продуцируется фибробластами . Функциональный SMAD 4 участвует в регуляции пути передачи сигнала TGF-β, который негативно регулирует рост эпителиальных клеток и внеклеточного матрикса (ECM). Когда структура SMAD 4 изменяется, экспрессия генов, участвующих в росте клеток, больше не регулируется, и пролиферация клеток может продолжаться без какого-либо подавления. Большое количество клеточных делений приводит к образованию опухолей, а затем к мультиплоидному колоректальному раку и карциноме поджелудочной железы . Он инактивирован как минимум в 50% случаев рака поджелудочной железы.
Было показано, что соматические мутации, обнаруженные при раке человека в домене MH1 SMAD 4, ингибируют ДНК-связывающую функцию этого домена.
СМАД 4 также обнаружили , мутировали в аутосомно - доминантным заболеванием синдром ювенильного полипоза (JPS). JPS характеризуется наличием гамартоматозных полипов желудочно-кишечного тракта. Эти полипы обычно доброкачественные, однако они подвержены большему риску развития рака желудочно-кишечного тракта , в частности рака толстой кишки . Идентифицировано около 60 мутаций, вызывающих JPS. Они были связаны с производством SMAD 4 меньшего размера с отсутствующими доменами, которые препятствуют связыванию белка с R-SMADS и образованию гетеромерных комплексов.
Мутации в SMAD4 (в основном замены) могут вызывать синдром Мюре , редкое наследственное заболевание, характеризующееся умственными недостатками, низким ростом, необычными чертами лица и различными костными аномалиями.
использованная литература
дальнейшее чтение
- Миязоно К. (2000). «Передача сигналов TGF-бета белками Smad». Обзоры цитокинов и факторов роста . 11 (1–2): 15–22. DOI : 10.1016 / S1359-6101 (99) 00025-8 . PMID 10708949 .
- Врана Дж. Л., Аттисано Л. (2000). «Путь Смада». Обзоры цитокинов и факторов роста . 11 (1–2): 5–13. DOI : 10.1016 / S1359-6101 (99) 00024-6 . PMID 10708948 .
- Verschueren K, Huylebroeck D (2000). «Замечательная универсальность белков Smad в ядре клеток, активированных трансформирующим фактором роста бета». Обзоры цитокинов и факторов роста . 10 (3–4): 187–99. DOI : 10.1016 / S1359-6101 (99) 00012-X . PMID 10647776 .
- Massagué J (1998). «Передача сигнала TGF-бета» . Ежегодный обзор биохимии . 67 : 753–91. DOI : 10.1146 / annurev.biochem.67.1.753 . PMID 9759503 .
- Klein-Scory S, Zapatka M, Eilert-Micus C, Hoppe S, Schwarz E, Schmiegel W, Hahn SA, Schwarte-Waldhoff I (2008). «Высокий уровень индуцируемой реэкспрессии Smad4 в линии клеток рака шейки матки C4-II связан с профилем экспрессии гена, который предсказывает предпочтительную роль Smad4 в составе внеклеточного матрикса» . BMC Рак . 7 : 209. DOI : 10.1186 / 1471-2407-7-209 . PMC 2186346 . PMID 17997817 .
- Kalo E, Buganim Y, Shapira KE, Besserglick H, Goldfinger N, Weisz L, Stambolsky P, Henis YI, Rotter V (декабрь 2007 г.). «Мутантный p53 ослабляет SMAD-зависимый путь передачи сигнала трансформирующего фактора роста бета1 (TGF-beta1) путем репрессии экспрессии рецептора TGF-бета типа II» . Молекулярная и клеточная биология . 27 (23): 8228–42. DOI : 10.1128 / MCB.00374-07 . PMC 2169171 . PMID 17875924 .
- Aretz S, Stienen D, Uhlhaas S, Stolte M, Entius MM, Loff S, Back W, Kaufmann A, Keller KM, Blaas SH, Siebert R, Vogt S, Spranger S, Holinski-Feder E, Sunde L, Propping P, Фридл В. (ноябрь 2007 г.). «Высокая доля крупных геномных делеций и обновление фенотипа генотипа в 80 неродственных семьях с синдромом ювенильного полипоза» . Журнал медицинской генетики . 44 (11): 702–9. DOI : 10.1136 / jmg.2007.052506 . PMC 2752176 . PMID 17873119 .
- Али С., Коэн С., Литтл СП, Секейра Дж. Х., Мосунжак МБ, Сиддики М.Т. (октябрь 2007 г.). «Применение SMAD4 в качестве диагностического иммуногистохимического маркера аденокарциномы поджелудочной железы и его экспрессия в других солидных опухолях». Диагностическая цитопатология . 35 (10): 644–8. DOI : 10.1002 / dc.20715 . PMID 17854080 . S2CID 36682992 .
- Милет Дж, Дехаис В., Бургейн С., Жуаноль А.М., Моссер А., Перрин М., Морсет Дж., Бриссо П., Дэвид В., Дюнье Ю., Моссер Дж. (Октябрь 2007 г.). «Общие варианты генов BMP2, BMP4 и HJV пути регуляции гепсидина модулируют пенетрантность гемохроматоза HFE» . Американский журнал генетики человека . 81 (4): 799–807. DOI : 10.1086 / 520001 . PMC 2227929 . PMID 17847004 .
- Салек С., Бенесова Л., Заворал М., Носек В., Касперова Л., Рыска М., Стрнад Р., Трабулси Е., Минарик М. (июль 2007 г.). «Оценка клинической значимости исследования мутаций K-ras, p16 и p53 вместе с аллельными потерями на 9p и 18q в образцах тонкой иглы под контролем EUS у пациентов с хроническим панкреатитом и раком поджелудочной железы» . Всемирный журнал гастроэнтерологии . 13 (27): 3714–20. DOI : 10,3748 / wjg.v13.i27.3714 . PMC 4250643 . PMID 17659731 .
- Себастьен А., Хайду М., Кис Л., Барна Г., Коппер Л. (сентябрь 2007 г.). «Smad4-независимый, PP2A-зависимый апоптотический эффект экзогенного трансформирующего фактора роста бета 1 в клетках лимфомы». Экспериментальные исследования клеток . 313 (15): 3167–74. DOI : 10.1016 / j.yexcr.2007.05.028 . PMID 17643425 .
- Мартин М.М., Бакенбергер Дж. А., Цзян Дж., Малана Г. Э., Ноелл Д. Л., Фельдман Д. С., Элтон Т. С. (сентябрь 2007 г.). «TGF-beta1 стимулирует экспрессию человеческого рецептора AT1 в фибробластах легких посредством перекрестной связи между сигнальными путями Smad, p38 MAPK, JNK и PI3K» . Американский журнал физиологии. Клеточная и молекулярная физиология легких . 293 (3): L790–9. DOI : 10,1152 / ajplung.00099.2007 . PMC 2413071 . PMID 17601799 .
- Леви Л., Хауэлл М., Дас Д., Харкин С., Эпископу В., Хилл С.С. (сентябрь 2007 г.). «Аркадия активирует Smad3 / Smad4-зависимую транскрипцию, запуская индуцированную сигналом деградацию SnoN» . Молекулярная и клеточная биология . 27 (17): 6068–83. DOI : 10.1128 / MCB.00664-07 . PMC 1952 153 . PMID 17591695 .
- Grijelmo C, Rodrigue C, Svrcek M, Bruyneel E, Hendrix A, de Wever O, Gespach C (август 2007 г.). «Проинвазивная активность BMP-7 через SMAD4 / src-независимые и ERK / Rac / JNK-зависимые сигнальные пути в раковых клетках толстой кишки». Сотовая сигнализация . 19 (8): 1722–32. DOI : 10.1016 / j.cellsig.2007.03.008 . PMID 17478078 .
- Сонегава Х., Нукуи Т., Ли Д.В., Такаиси М., Сакагути М., Хах Нью-Хэмпшир (июль 2007 г.). «Участие ухудшения S100C / A11-опосредованного пути в устойчивости линий клеток плоскоклеточного рака человека к подавлению роста, индуцированному TGFbeta» . Журнал молекулярной медицины . 85 (7): 753–62. DOI : 10.1007 / s00109-007-0180-7 . PMID 17476473 . S2CID 15667203 .
- Шейх А.А., Вималачандран Д., Томпсон С.К., Дженкинс Р.Э., Неджади Т., Шекоу А., Кэмпбелл Ф., Додсон А., Прайм В., Црногорак-Юрчевич Т., Лемуан Н.Р., Костелло Е. (июнь 2007 г.). «Экспрессия S100A8 в моноцитах, связанных с раком поджелудочной железы, связана со статусом Smad4 раковых клеток поджелудочной железы». Протеомика . 7 (11): 1929–40. DOI : 10.1002 / pmic.200700072 . PMID 17469085 . S2CID 35648264 .
- Попович Хадзия М., Королия М., Якич Разумович Дж., Павкович П., Хадзия М., Капитанович С. (апрель 2007 г.). «Мутации K-ras и Dpc4 при хроническом панкреатите: серия случаев» . Хорватский медицинский журнал . 48 (2): 218–24. PMC 2080529 . PMID 17436386 .
- Лози Л., Бузурен Х., Бенхаттар Дж. (Май 2007 г.). «Потеря экспрессии Smad4 предсказывает метастазирование в печень при колоректальном раке человека» . Отчеты онкологии . 17 (5): 1095–9. doi : 10.3892 / или 17.5.1095 . PMID 17390050 .
- Карлссон Г., Бланк Ю., Муди Дж. Л., Эхингер М., Сингбрант С., Дэн С. Х., Карлссон С. (март 2007 г.). «Smad4 имеет решающее значение для самообновления гемопоэтических стволовых клеток» . Журнал экспериментальной медицины . 204 (3): 467–74. DOI : 10,1084 / jem.20060465 . PMC 2137898 . PMID 17353364 .
- Такано С., Канаи Ф., Джазаг А., Иджичи Х., Яо Дж., Огава Х., Эномото Н., Омата М., Накао А. (март 2007 г.). «Smad4 необходим для подавления E-кадгерина, индуцированного TGF-бета, в линии клеток рака поджелудочной железы PANC-1». Журнал биохимии . 141 (3): 345–51. DOI : 10.1093 / Jb / mvm039 . PMID 17301079 .