Олестра - Olestra
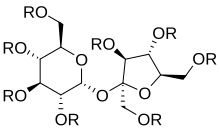 | |

Вверху : общая 2D-структура олестры, где R = H или группа жирных кислот, C (O) C n H m
Внизу : стереоскопическая анимация репрезентативной молекулы олестры с 8 группами ненасыщенных жирных кислот | |
| Клинические данные | |
|---|---|
| Торговые наименования | Олеан |
| Правовой статус | |
| Правовой статус | |
| Идентификаторы | |
| ChemSpider | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула |
C п +12ЧАС 2 п +22О 13 (где жирные кислоты насыщены) |
| Молярная масса | Переменная |
|
| |
Olestra (также известная под своим брендом Olean ) - это заменитель жира, который не добавляет калорий в продукты. Его использовали при приготовлении продуктов с высоким содержанием жира, таких как картофельные чипсы , тем самым снижая или устраняя их содержание жира. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) первоначально одобрило олестру для использования в США в качестве замены жиров и масел в расфасованных готовых к употреблению закусках в 1996 году, сделав вывод, что такое использование «соответствует стандарту безопасности пищевых добавок, разумная уверенность в том, что Никакого вреда". В конце 1990-х годов олестра потеряла свою популярность из-за побочных эффектов и была в значительной степени прекращена, но продукты, содержащие этот ингредиент, все еще можно купить в продуктовых магазинах в некоторых странах.
Коммерциализация
Олестра была обнаружена случайно исследователями Procter & Gamble (P&G) Ф. Маттсоном и Р. Вольпенхейном в 1968 году при исследовании жиров, которые могут легче усваиваться недоношенными детьми. В 1971 году компания P&G встретилась с Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), чтобы выяснить, какие тесты потребуются для введения олестры в качестве пищевой добавки .
Во время следующих тестов компания P&G заметила снижение уровня холестерина в крови как побочный эффект замены олестры натуральными диетическими жирами. Следуя этой потенциально прибыльной возможности, в 1975 году P&G подала новый запрос в FDA на использование олестры в качестве «лекарства», особенно для снижения уровня холестерина. Однако последовавшая за этим длительная серия исследований не смогла продемонстрировать снижение на 15%, требуемое FDA для утверждения в качестве лечения. Дальнейшая работа над олестрой зачахла.
В 1984 году FDA разрешило Kellogg публично заявить, что их хлопья для завтрака с высоким содержанием клетчатки эффективны в снижении риска рака . P&G немедленно начала еще одну серию испытаний, которая длилась три года. Когда эти испытания были завершены, P&G подала заявку на одобрение в качестве пищевой добавки для замены до 35% жиров в домашней кулинарии и 75% для коммерческого использования.
Одной из основных проблем FDA по поводу олестры было то, что она может побудить потребителей есть больше продуктов « вершины пирамиды » из-за того, что они считают их более полезными для здоровья. Это может привести к чрезмерному потреблению потребителями, считая, что добавление олестры устранит негативные последствия. В свете этой возможности, одобрение его в качестве добавки означало бы, что потребители будут потреблять пищу с относительно большим количеством добавки, долгосрочное воздействие которой на здоровье не было задокументировано. Это заставило FDA особенно нерешительно одобрять продукт, а также побочные эффекты, такие как диарея , и беспокойство по поводу потери жирорастворимых витаминов. В августе 1990 года P&G сосредоточила свое внимание на «пикантных закусках», картофельных чипсах , чипсах из тортильи , крекерах и аналогичных продуктах.
К этому моменту срок действия первоначальных патентов приближался к 1995 году. P&G лоббировала продление, которое они получили в декабре 1993 года. Это продление продлилось до 25 января 1996 года. Под давлением P&G разрешение было наконец предоставлено 24 января, за день до истечения срока действия патента, что автоматически продлило срок действия патента на два года.
Во время постановления 1996 года FDA пришло к выводу, что «во избежание неправильной маркировки ... продукты, содержащие олестру, должны иметь маркировку, чтобы информировать потребителей о возможном воздействии олестры на желудочно-кишечный тракт. что добавленные витамины присутствуют для компенсации любых пищевых эффектов олестры, а не для обеспечения повышенной питательной ценности ». Позже FDA удалило этикетку, заявив, что «нынешняя этикетка не совсем точно передает информацию потребителям». FDA также согласилось с P&G в том, что «заявление на этикетке может вводить в заблуждение и заставлять потребителей олестры приписывать серьезные проблемы олестре, хотя это маловероятно».
Продукты, снятые с производства
Olestra была одобрена Управлением по контролю за продуктами и лекарствами для использования в качестве пищевой добавки в 1996 году и первоначально использовалась в картофельных чипсах под торговой маркой WOW компанией Frito Lay . В 1998 году первый год олестры стали продаваться на национальном уровне после того, как Консультативный комитет FDA по пищевым продуктам подтвердил решение, вынесенное двумя годами ранее, продажи превысили 400 миллионов долларов. Однако к 2000 году продажи снизились до 200 миллионов долларов. P&G отказалась от попыток расширить использование олестры и в феврале 2002 года продала свой завод в Цинциннати компании Twin Rivers Technologies . В 2004 году чипы WOW были переименованы в Lay's Light.
По состоянию на 2013 год чипсы Lay's Light все еще были доступны, и олестра была указана в качестве ингредиента; однако они были сняты с производства к 2016 году. В картофельных чипсах Pringles Light, производимых Kellogg's (хотя одно время являвшимися продуктом P&G), использовалась олестра марки Olean, а в 2015 году они были сняты с производства.
Побочные эффекты
Начиная с 1996 года, этикетка с предупреждением о вреде для здоровья, предписанная Управлением по контролю за продуктами и лекарствами (FDA), гласит: «Этот продукт содержит олестру. Олестра может вызывать спазмы в животе и жидкий стул . Олестра препятствует всасыванию некоторых витаминов и других питательных веществ. Витамины A , D , E и K были добавлен".
Эти симптомы, обычно возникающие только при чрезмерном употреблении в течение короткого периода времени, известны как стеаторея и вызваны избытком жира в стуле.
FDA отменило требование предупреждения в 2003 году, поскольку оно «провело научный обзор нескольких исследований после выхода на рынок, представленных P&G, а также отчетов о побочных эффектах, представленных P&G и Центром науки в интересах общества . FDA пришло к выводу, что заявление на этикетке больше не было оправдано ". FDA также согласилось с P&G в том, что «заявление на этикетке может вводить в заблуждение и заставлять потребителей олестры приписывать серьезные проблемы олестре, хотя это [было] маловероятно».
Удаляя предупреждающую этикетку о олестре, FDA процитировало шестинедельное исследование P&G с участием более 3000 человек, показавшее, что у группы, употреблявшей олестру, наблюдалось лишь небольшое увеличение частоты испражнения по сравнению с контрольной группой. FDA пришло к выводу, что «субъекты, употребляющие олестру-содержащие чипсы, с меньшей вероятностью сообщали о жидком стуле, спазмах в животе или любых других симптомах со стороны желудочно-кишечного тракта по сравнению с субъектами, употребляющими такое же количество [картофельных] чипсов».
Помимо воздействия предупреждений о вреде для здоровья на общественное восприятие продукта, олестра, возможно, не оправдала ожиданий потребителей в отношении быстрых результатов. Если бы потребители считали, что они могут есть больше, чтобы компенсировать «сэкономленные» жирные калории, олестра не была бы эффективным способом улучшить общий рацион. Производители утверждают, что аутентичный вкус олестры компенсирует эту тенденцию, а некоторые исследования показали, что люди, потребляющие продукты с олестрой, не едят больше, чтобы компенсировать потерю калорий. P&G провела рекламные кампании, чтобы подчеркнуть преимущества olestra, в том числе работая напрямую с медицинским сообществом.
Olestra запрещена к продаже на многих рынках, включая Европейский Союз и Канаду.
Употребление олестры может побудить крыс съесть слишком много продуктов, содержащих обычные жиры, из-за изучения неправильной связи между потреблением жира и калориями. Крысы, которых кормили обычными картофельными чипсами, а также чипсами, приготовленными с олестрой, набирали больше веса при последующем питании с высоким содержанием жиров, чем крысы, которые получали только обычные чипсы.
Химия
Триглицериды , диетические жиры , дающие энергию , состоят из трех жирных кислот, связанных в форме сложных эфиров с глицериновым остовом. Olestra использует сахарозу в качестве основы вместо глицерина, и она может образовывать сложные эфиры, содержащие до восьми жирных кислот. Olestra представляет собой смесь гекса-, гепта- и октаэфиров сахарозы с различными длинноцепочечными жирными кислотами. Получающееся в результате радиальное расположение слишком велико и нерегулярно, чтобы проходить через стенку кишечника и всасываться в кровоток. Олестра имеет тот же вкус и ощущение во рту, что и жир, но проходит через желудочно-кишечный тракт непереваренной, не добавляя калорий или питательной ценности к рациону.
С механической точки зрения ученые смогли манипулировать составом таким образом, чтобы его можно было использовать вместо кулинарных масел при приготовлении многих видов пищи.
Поскольку олестра содержит функциональные группы жирных кислот , она способна растворять жирорастворимые витамины , такие как витамин D , витамин E , витамин K и витамин A , а также каротиноиды . Жирорастворимые питательные вещества, потребляемые с продуктами олестры, выводятся с непереваренными молекулами олестры. Чтобы противодействовать этой потере питательных веществ, продукты, изготовленные с олестрой, обогащены жирорастворимыми витаминами.
Приложения
P&G продает свои продукты на основе сложного эфира сахарозы под торговой маркой "Sefose" для использования в качестве промышленных смазок и присадок к краскам. Поскольку олестра производится путем химического соединения сахара и растительного масла, она не выделяет токсичных паров и потенциально может стать безопасной и экологически чистой заменой нефтехимии в этих применениях. В настоящее время он используется в качестве основы для пятен на палубе и смазки для небольших электроинструментов, и есть планы использовать его на более крупном оборудовании.
Существуют предварительные данные, указывающие на то, что прием олестры может ускорить выведение гидрофобных токсинов, хотя рандомизированных контролируемых клинических испытаний для определения эффективности этого потенциального лечения не проводилось. Токсины, которые были изучены в сочетании с лечением олестрой, включают диоксины , гексахлорбензол и полихлорированные бифенилы (ПХБ).
