Гистидинкиназа - Histidine kinase
| протеин гистидинкиназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
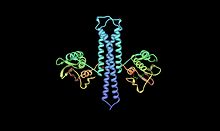
Кристаллографическая структура АТФ: протеин-L-гистидин-N-фосфотрансфераза на основе координат PDB : 2c2a .
| |||||||||
| Идентификаторы | |||||||||
| ЕС нет. | 2.7.13.3 | ||||||||
| № CAS | 99283-67-7 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
Гистидинкиназы ( HK ) многофункциональны, и в царстве животных, как правило, трансмембранных , белки класса ферментов трансфераз играют роль в передаче сигнала через клеточную мембрану. Подавляющее большинство HK являются гомодимерами, которые проявляют активность аутокиназы , фосфотрансфера и фосфатазы. HK могут действовать как клеточные рецепторы для сигнальных молекул аналогично рецепторам тирозинкиназы (RTK). Многофункциональные рецепторные молекулы, такие как HK и RTK, обычно имеют части снаружи клетки ( внеклеточный домен), которые связываются с молекулами, подобными гормонам или фактору роста, части, которые охватывают клеточную мембрану ( трансмембранный домен ), и части внутри клетки ( внутриклеточный домен), которые обладают ферментативной активностью. В дополнение к киназной активности внутриклеточные домены обычно имеют области, которые связываются со вторичной эффекторной молекулой или комплексом молекул, которые дополнительно распространяют передачу сигнала внутри клетки. В отличие от других классов протеинкиназ , HK обычно являются частью двухкомпонентных механизмов передачи сигнала, в которых HK переносит фосфатную группу с АТФ на остаток гистидина внутри киназы, а затем на остаток аспартата в домене-приемнике ответа. белок- регулятор (а иногда и сама киназа). Совсем недавно в клетках человека было обнаружено широкое распространение гистидинового фосфорилирования белка, отличного от фосфорилирования двухкомпонентных гистидинкиназ. В отличие от фосфорилирования Ser, Thr и Tyr, анализ фосфорилированного гистидина с использованием стандартных биохимических и масс-спектрометрических подходов является гораздо более сложной задачей, и для их сохранения требуются специальные процедуры и методы разделения наряду с классическим фосфорилированием Ser, Thr и Tyr на выделенных белках. из клеток человека.
С точки зрения энзимологии , гистидина киназы ( ЕС 2.7.13.3 , EnvZ , гистидин протеинкиназа , белок гистидинкиназа , протеинкиназа (гистидин) , HK1 , HP165 , Sln1p ) представляет собой фермент , который катализирует в химическую реакцию
- АТФ + белок L-гистидин АДФ + белок N-фосфо-L-гистидин.
Таким образом, двумя субстратами этого фермента являются АТФ и белок L- гистидин , тогда как двумя его продуктами являются АДФ и белок N-фосфо-L-гистидин.
Этот тип ферментов участвует в путях передачи сигналов, предшествующих многим клеточным процессам, включая различные метаболические, вирулентные и гомеостатические пути.
Механизм
Механизм реакций, катализируемых гистидинкиназой, полностью не выяснен, но имеющиеся данные свидетельствуют о том, что каталитический домен одной димерной единицы может вращаться таким образом, что АТФ-связывающий карман этой единицы может вступать в контакт с определенным остатком гистидина. на противоположном звене, и нуклеофильное добавление приводит к фосфорилированному гистидину.
Структура и функции
HK состоит из нескольких доменов, начинающихся с короткого N-концевого участка цитоплазмы, соединенного с внеклеточным сенсорным доменом через трансмембранную α-спираль . Вторая трансмембранная α-спираль соединяет внеклеточный домен с С-концевым цитоплазматическим каталитическим доменом. HKs, как известно, играют роль во многих различных путях передачи сигналов, поэтому неудивительно, что внеклеточный сенсорный домен не очень хорошо консервативен в семействе HK. Напротив, цитоплазматический домен имеет тенденцию иметь высокую гомологию последовательностей и содержит несколько хорошо известных мотивов . Эти мотивы включают блоки H, N, G1, F и G2. H-бокс автофосфорилирования содержится в N-концевом домене димеризации и гистидинфосфотрансфера (DHp). В HK853-CD, кристаллизованном из Thermotoga maritima , этот домен представляет собой спиральную шпильку и образован остатками 232–317. Сайт фосфорилирования гистидина расположен в His-260. Боксы N, G1, F и G2 содержатся в С-концевом каталитическом и АТФ-связывающем (СА) домене. Этот домен образован остатками 323-489 и образует структуру, известную как α / β-сэндвич-складка. Эта конкретная складка имеет один слой, состоящий из 5-нитевого β-листа, а другой слой состоит из трех α-спиралей.
Димерная единица удерживается вместе с помощью пучка из четырех спиралей, образованного, когда С-концевые сегменты спиралей α1 на каждой субъединице взаимодействуют антипараллельным образом с обеими спиралями α2. Стабильности димера способствует несколько взаимодействий на границе раздела между DHps каждого мономера. К ним относятся гидрофобные взаимодействия между консервативными гидрофобными остатками, а также двумя водородными связями (Thr-252 ... Glu-316 'и Arg-263 ... Asn-307') и одним солевым мостиком (Lys-270 ... Glu- 303 '). Дальнейшие взаимодействия опосредуются водородными связями с водой внутри полости внутри спиральной спирали и примыкают к гидрофобным остаткам.
Нуклеотид / АТФ связывающий карман содержится внутри домена CA и структурное сходство этого кармана является высоким между большинством ОК. Полость CheA, также кристаллизованная из T. maritima, сначала образована β-листом P4 в задней части, а стороны полости образованы 4 мотивами, упомянутыми ранее, блоками N, G1, F и G2. Большинство остатков β-листа являются гидрофобными, за исключением Asp449. Этот остаток инвариантен и образует водородную связь вместе с молекулой воды с аминогруппой аденина . Три другие молекулы воды образуют прямые водородные связи с основанием аденина. Ион Mg 2+ образует мостик между всеми тремя фосфатами и инвариантным остатком Asn. Наконец, еще две молекулы воды завершают октаэдрическую координацию с Mg 2+ и связаны с Arg-408 и His-405. Когда γ-фосфат АТФ дестабилизируется, Mg 2+ больше не наблюдается из-за его неспособности к октаэдрической координации. Марина и др. утверждают, что аналогичная координация Mg 2+ происходит в HK853, но не наблюдается из-за использования аналога АТФ AMPPNP в кристаллической структуре. В процессе кристаллизации аналог гидролизовался до продукта, аналогичного АДФ.
Последняя сторона кармана для связывания АТФ удобно названа «крышкой АТФ». Стабильность этой структуры обеспечивается присутствием γ-фосфата и, следовательно, иона Mg 2+ в сайте связывания. Также было доказано, что присутствие нуклеотидного основания играет важную роль в стабилизации крышки в закрытой конформации . Крышка АТФ связана с остальным белком через гидрофобные остатки. Γ-фосфат АТФ в некоторой степени подвергается воздействию, что позволяет дефосфорилировать . Считается, что при связывании АТФ в этом кармане происходит конформационное изменение, позволяющее вращению домена СА вступать в контакт с DHp другого мономера и, таким образом, позволяя консервативному His-260 находиться рядом с γ-фосфатом. Затем Nε His-260 атакует γ-фосфат АТФ путем нуклеофильного присоединения и удаляет АДФ в качестве уходящей группы.
Роль в грибковых инфекциях
Двухкомпонентная система (ТТС), с участием гистидинкиназы и переменной регуляторой ответа белок, может иметь решающее значение для вирулентности некоторых штаммов грибов , таких как Candida Albicans , которые часто ответственности за причинение кандидоза в ослабленном иммунитете лиц. C. albicans с делецией CHK1, двухкомпонентного гена гистидинкиназы, демонстрируют дефекты морфогенеза и резкое снижение способности клетки сопротивляться элиминации нейтрофилами человека . Поскольку у людей отсутствует эта двухкомпонентная система, она может быть хорошей мишенью для антимикробных агентов при лечении кандидоза .
Роль в бактериальных инфекциях
Подобно грибку, двухкомпонентные системы также могут быть обнаружены при некоторых стойких бактериальных инфекциях. Например, сообщалось , что Staphylococcus aureus использует SrrAB TCS, состоящие из сенсорных HK (SrrB), которые будут передавать фосфатную группу на эффекторный регулятор ответа (SrrA), что приводит к модификации активности SrrA, включая регуляцию генов. Эти TCS использовались S. aureus для определения изменений условий окружающей среды и передачи сигнала соответствующей отвечающей системе, например, гены ica индуцируются SrrAB, чтобы опосредовать сборку клеток и образование биопленок для выживания в анаэробных условиях.
использованная литература
дальнейшее чтение
- Ковлуру А (2002). «Идентификация и характеристика новой протеин-гистидинкиназы в островковых бета-клетках: доказательства ее регуляции мастопараном, активатором G-белков и секреции инсулина». Biochem. Pharmacol . 63 (12): 2091–100. DOI : 10.1016 / S0006-2952 (02) 01025-0 . PMID 12110368 .
- Йошими А., Цуда М., Танака С. (2004). «Клонирование и характеристика гена гистидинкиназы Dic1 из Cochliobolus heterostrophus, который придает устойчивость к дикарбоксимиду и осмотическую адаптацию». Мол. Genet. Геномика . 271 (2): 228–36. DOI : 10.1007 / s00438-003-0974-4 . PMID 14752661 . S2CID 26038953 .
- Байер Д., Франк Р. (2000). «Молекулярная характеристика двухкомпонентных систем Helicobacter pylori» . J. Bacteriol . 182 (8): 2068–76. DOI : 10.1128 / JB.182.8.2068-2076.2000 . PMC 111253 . PMID 10735847 .
- Пфлок М., Дитц П., Шар Дж., Байер Д. (2004). «Генетические доказательства того, что гистидинкиназа HP165 является кислотным сенсором Helicobacter pylori» . FEMS Microbiol. Lett . 234 (1): 51–61. DOI : 10.1111 / j.1574-6968.2004.tb09512.x . PMID 15109719 .
- Робертс Д.Л., Беннетт Д.В., Forst SA (1994). «Идентификация сайта фосфорилирования на осмосенсоре EnvZ Escherichia coli» . J. Biol. Chem . 269 (12): 8728–33. DOI : 10.1016 / S0021-9258 (17) 37029-1 . PMID 8132603 .
- Александрин М. Билвес; Лиза А. Алекс; Брайан Р. Крейн; Мелвин И. Саймон (1999). «Структура CheA, гистидинкиназы, передающей сигнал» . Cell . 96 (1): 131–41. DOI : 10.1016 / S0092-8674 (00) 80966-6 . PMID 9989504 . S2CID 16842653 .
- Райан Л. Брунсинг; Чандра Ла Клер; Шэрон Танг; Кристина Чанг; Линн Э. Хэнкок; Марта Перего; Джеймс Хох (2005). «Характеристика гистидинкиназ споруляции Bacillus anthracis» . J. Bacteriol . 187 (20): 6972–81. DOI : 10.1128 / JB.187.20.6972-6981.2005 . PMC 1251614 . PMID 16199567 .
- Амр Эльдакак; Ф. Марион Хьюлетт (2007). «Cys303 в гистидинкиназе PhoR имеет решающее значение для реакции фосфопереноса в двухкомпонентной системе PhoPR в Bacillus subtilis» . J. Bacteriol . 189 (2): 410–21. DOI : 10.1128 / JB.01205-06 . PMC 1797398 . PMID 17085571 .
- Хиршман А., Бухвалова М., ВанБругген Р., Вулф А.Дж., Стюарт Р.К. (ноябрь 2001 г.). «Мутации в активном сайте CheA, протеинкиназы, передающей сигнал, системы хемотаксиса Escherichia coli». Биохимия . 40 (46): 13876–87. DOI : 10.1021 / bi0113622 . PMID 11705377 .




