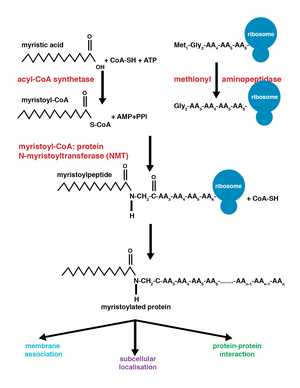
Миристоилирование - Myristoylation

Миристоилирование представляет собой модификацию липидирования, при которой миристоильная группа , полученная из миристиновой кислоты , ковалентно присоединена амидной связью к альфа-аминогруппе N-концевого остатка глицина . Миристиновая кислота - это 14-углеродная насыщенная жирная кислота (14: 0) с систематическим названием н- тетрадекановая кислота. Эта модификация может быть добавлена как ко-трансляционно, так и пост-трансляционно . N-миристоилтрансфераза (NMT) катализирует реакцию присоединения миристиновой кислоты в цитоплазме клеток. Это событие липидирования является наиболее часто встречающимся типом ацилирования жирных кислот и распространено среди многих организмов, включая животных , растения , грибы , простейшие и вирусы . Миристоилирование допускает слабые белок-белковые и белок-липидные взаимодействия и играет важную роль в нацеливании на мембраны, белок-белковых взаимодействиях и широко функционирует в различных путях передачи сигнала.
Открытие
В 1982 году лаборатория Коити Титани идентифицировала «N-концевую блокирующую группу» на каталитической субъединице циклической АМФ-зависимой протеинкиназы у коров как n- тетрадеканоил. Почти одновременно в лаборатории Клода Б. Клее эта же группа, блокирующая N-конец, была далее охарактеризована как миристиновая кислота. Обе лаборатории сделали это открытие, используя схожие методы: бомбардировку быстрыми атомами , масс-спектрометрию и газовую хроматографию .
N-миристоилтрансфераза
Фермент N-миристоилтрансфераза (NMT) или глицилпептид N-тетрадеканоилтрансфераза отвечает за необратимое присоединение миристоильной группы к N-концевым или внутренним остаткам глицина в белках. Эта модификация может происходить ко-трансляционно или пост-трансляционно . У позвоночных эта модификация осуществляется двумя NMT, NMT1 и NMT2 , оба из которых являются членами суперсемейства ацетилтрансфераз GCN5 .
Состав
Кристаллическая структура из NMT показывает два идентичных субъединиц, каждый со своим собственным сайтом связывания миристоильная - СоА. Каждая субъединица состоит из большого седловидного β-листа, окруженного α-спиралями . Симметрия складки псевдодвойственна. Миристоил-КоА связывается с N-концевой частью, в то время как С-концевой конец связывает белок.
Механизм
Присоединение миристоильной группы происходит посредством реакции нуклеофильного присоединения-элиминирования . Во-первых, миристоил- коэнзим A (CoA) располагается в своем связывающем кармане NMT, так что карбонил обращен к двум аминокислотным остаткам, фенилаланину 170 и лейцину 171. Это поляризует карбонил, так что на углероде возникает чистый положительный заряд, что делает его чувствительны к нуклеофильной атаке остатком глицина модифицируемого белка. Когда миристоил-КоА связывается, NMT переориентируется, чтобы позволить связывание пептида. С-конец NMT затем действует как общее основание для депротонирования NH 3 + , активируя аминогруппу для атаки на карбонильную группу миристоил-КоА. Полученный тетраэдрический промежуточный продукт стабилизируется взаимодействием между положительно заряженной оксианионной дыркой и отрицательно заряженным алкоксид- анионом. Затем высвобождается свободный КоА, вызывая конформационное изменение фермента, которое позволяет высвобождать миристоилированный пептид.
Совместное трансляционное и посттрансляционное добавление
Ко-трансляционные и посттрансляционные ковалентные модификации позволяют белкам развивать более высокий уровень сложности клеточной функции, дополнительно добавляя разнообразия протеому . Добавление миристоил-КоА к белку может происходить во время трансляции белка или после нее. Во время ко-трансляционного добавления миристоильной группы N-концевой глицин модифицируется после расщепления N-концевого остатка метионина во вновь формирующемся растущем полипептиде . Посттрансляционное миристоилирование обычно происходит после расщепления каспазы , что приводит к обнажению внутреннего остатка глицина, который затем становится доступным для добавления миристиновой кислоты.
Функции
Миристоилированные белки
| Протеин | Физиологическая роль | Функция миристоилирования |
|---|---|---|
| Актин | Структурный белок цитоскелета | Посттрансляционное миристоилирование при апоптозе |
| Делать ставку | Белок, способствующий апоптозу | Посттрансляционное миристоилирование после расщепления каспазой направляет белок на митохондриальную мембрану |
| ОТМЕТКИ | сшивание актина при фосфорилировании протеинкиназой C | Совместное трансляционное миристоилирование способствует ассоциации с плазматической мембраной |
| G-белок | Сигнализация GTPase | Совместное трансляционное миристоилирование способствует ассоциации с плазматической мембраной |
| Гельсолин | Актиновый белок, расщепляющий нити | Посттрансляционное миристоилирование усиливает антиапоптотические свойства |
| PAK2 | Рост клеток серин / треонинкиназы , подвижность, стимулятор выживания | Посттрансляционное миристоилирование усиливает апоптотические свойства и индуцирует локализацию плазматической мембраны |
| Арф | везикулярный трафик и регуляция ремоделирования актина | Миристоилирование N-конца способствует мембранной ассоциации |
| Гиппокальцин | Нейрональный датчик кальция | Содержит переключатель Ca 2+ / миристоил |
Молекулярный переключатель миристоилирования
Миристоилирование не только разнообразит функцию белка, но и добавляет к нему уровни регуляции. Одна из наиболее распространенных функций миристоильной группы - это мембранная ассоциация и клеточная локализация модифицированного белка. Хотя миристоильная группа добавляется на конец белка, в некоторых случаях она изолируется в гидрофобных областях белка, а не подвергается воздействию растворителя. Регулируя ориентацию миристоильной группы, эти процессы могут быть сильно скоординированы и строго контролироваться. Таким образом, миристоилирование является формой « молекулярного переключателя ».
Как гидрофобные миристоильные группы, так и «основные участки» (высоко положительные области на белке) характеризуют миристоил-электростатические переключатели. Базовый пластырь обеспечивает благоприятные электростатические взаимодействия между отрицательно заряженными фосфолипидными головками мембраны и положительной поверхностью связывающего белка. Это обеспечивает более тесную ассоциацию и направленную локализацию белков.
Миристоил-конформационные переключатели могут иметь несколько форм. Связывание лиганда с миристоилированным белком с изолированной его миристоильной группой может вызывать конформационные изменения в белке, приводящие к обнажению миристоильной группы. Аналогичным образом , некоторые myristoylated белки активируются не назначенным лиганда, но путем обмена ВВП для ГТФ с помощью факторов обмена гуанин нуклеотидов в клетке. Как только GTP связывается с миристоилированным белком, он активируется, обнажая миристоильную группу. Эти конформационные переключатели могут использоваться в качестве сигнала для клеточной локализации, межбелковых и межбелковых взаимодействий .
Двойные модификации миристоилированных белков
Дальнейшие модификации N-миристоилированных белков могут добавить еще один уровень регуляции миристоилированного белка. Двойное ацилирование может способствовать более строго регулируемой локализации белков, в частности, направляя белки на липидные рафты на мембранах или позволяя диссоциацию миристоилированных белков от мембран.
Миристоилирование и пальмитоилирование обычно являются сопряженными модификациями. Само по себе миристоилирование может способствовать временным мембранным взаимодействиям, которые позволяют белкам закрепляться на мембранах, но легко диссоциируют. Дальнейшее пальмитоилирование обеспечивает более прочное закрепление и более медленную диссоциацию от мембран, когда этого требует клетка. Эта специфическая двойная модификация важна для путей рецепторов, связанных с G-белком, и называется переключателем двойного жирного ацилирования.
За миристоилированием часто следует фосфорилирование близлежащих остатков. Дополнительное фосфорилирование того же белка может снизить электростатическое сродство миристоилированного белка к мембране, вызывая транслокацию этого белка в цитоплазму после диссоциации от мембраны.
Передача сигнала
Миристоилирование играет жизненно важную роль в нацеливании на мембраны и передаче сигналов в ответах растений на стресс окружающей среды. Кроме того, при передаче сигнала через G-белок пальмитоилирование α-субъединицы, пренилирование γ-субъединицы и миристоилирование участвуют в привязке G-белка к внутренней поверхности плазматической мембраны, так что G-белок может взаимодействовать со своим рецептором.
Апоптоз
Миристоилирование является неотъемлемой частью апоптоза или запрограммированной гибели клеток. Апоптоз необходим для гомеостаза клеток и возникает, когда клетки находятся в состоянии стресса, такого как гипоксия или повреждение ДНК . Апоптоз может происходить путем активации митохондрий или рецепторов. При апоптозе, опосредованном рецепторами, апоптотические пути запускаются, когда клетка связывает рецептор смерти. В одном из таких случаев связывание рецептора смерти инициирует образование сигнального комплекса , вызывающего смерть , комплекса, состоящего из множества белков, включая несколько каспаз, включая каспазу 3 . Каспаза 3 расщепляет ряд белков, которые впоследствии миристоилируются с помощью NMT. Проапоптотические BH3 взаимодействующий смерть домена агонист (Bid) является одним из таких белков , которые когда - то myristoylated, транслоцируется в митохондрии , где он побуждает высвобождение цитохрома с , ведущей к гибели клеток. Актин , гельсолин и p21-активированная киназа 2 PAK2 - это три других белка, которые миристоилируются после расщепления каспазой 3 , что приводит либо к усилению , либо к понижению регуляции апоптоза.
Влияние на здоровье человека
Рак
c-Src - это ген, который кодирует протоонкоген тирозин-протеинкиназу Src, белок, важный для нормального митотического цикла . Он фосфорилируется и дефосфорилируется, чтобы включать и выключать передачу сигналов. Протоонкоген тирозин-протеинкиназа Src должен быть локализован на плазматической мембране для фосфорилирования других нижестоящих мишеней; миристоилирование отвечает за этособытие нацеливания на мембрану . Повышенное миристоилирование c-Src может привести к усиленной пролиферации клеток и быть ответственным за трансформацию нормальных клеток в раковые . Активация c-Src может привести к так называемым признакам рака : усилению ангиогенеза , пролиферации и инвазии .
Вирусная инфекционность
ВИЧ-1 - это ретровирус, который полагается на миристоилирование одного из своих структурных белков, чтобы успешно упаковать свой геном, собрать и созреть в новую инфекционную частицу. Белок вирусного матрикса , самый N-концевой домен полипротеина gag, является миристоилированным. Эта модификация миристоилирования нацелена на gag к мембране клетки-хозяина. Используя миристоил-электростатический переключатель, включая базовый участок на матричном белке, gag может собираться на липидных рафтах на плазматической мембране для сборки вируса , почкования и дальнейшего созревания. Чтобы предотвратить вирусную инфекционность, миристоилирование матричного белка может стать хорошей лекарственной мишенью.
Прокариотические и эукариотические инфекции
Некоторые NMT являются терапевтическими мишенями для разработки лекарств против бактериальных инфекций . Было показано, что миристоилирование необходимо для выживания ряда болезнетворных грибов , в том числе C. albicans и C. neoformans . Помимо прокариотических бактерий, в качестве мишеней для лекарств были идентифицированы NMT многих болезнетворных эукариотических организмов . Правильное функционирование NMT у простейших Leishmania major и Leishmania donovani ( лейшманиоз ), Trypanosoma brucei ( африканская сонная болезнь ) и P. falciparum ( малярия ) необходимо для выживания паразитов. Ингибиторы этих организмов в настоящее время исследуются. Пиразола сульфонамидную ингибитор был идентифицирован , который селективно связывается Т. brucei , конкурирующих за пептидного связывания сайта, тем самым ингибируя ферментативную активность и устранение паразита из крови мышей с африканской сонной болезнью .
Смотрите также
использованная литература
- ^ a b Кокс, Дэвид Л. Нельсон, Майкл М. (2005). Принципы биохимии Ленингера (4-е изд.). Нью-Йорк: WH Freeman. ISBN 978-0716743392.
- ^ a b Tamanoi, под редакцией Фуюхико; Сигман, Дэвид С. (2001). Липидирование белков (3-е изд.). Сан-Диего, Калифорния: Academic Press. ISBN 978-0-12-122722-7.CS1 maint: дополнительный текст: список авторов ( ссылка )
- ^ Мохаммадзаде, Фатемех; Хоссейни, Вахид; Мехдизаде, Амир; Дэни, Кристиан; Дараби, Масуд (30.11.2018). «Метод общего анализа ацилирования белков методом газожидкостной хроматографии» . МСБМБ Жизнь . 71 (3): 340–346. DOI : 10.1002 / iub.1975 . ISSN 1521-6543 . PMID 30501005 .
- ^ Кара, UA; Стензель, диджей; Ингрэм, LT; Бушелл, гр .; Lopez, JA; Кидсон, К. (апрель 1988 г.). «Ингибирующее моноклональное антитело против (миристилированного) низкомолекулярного антигена из Plasmodium falciparum, связанного с мембраной паразитофорной вакуоли» . Инфекция и иммунитет . 56 (4): 903–9. DOI : 10.1128 / IAI.56.4.903-909.1988 . PMC 259388 . PMID 3278984 .
- ^ a b c d e f g h Фарази, TA (29 августа 2001 г.). «Биология и энзимология N-миристоилирования белков» . Журнал биологической химии . 276 (43): 39501–39504. DOI : 10.1074 / jbc.R100042200 . PMID 11527981 .
- ^ a b Carr, SA; Биманн, К; Сёдзи, S; Пармели, округ Колумбия; Титани, К. (октябрь 1982 г.). «n-Тетрадеканоил представляет собой NH2-концевую блокирующую группу каталитической субъединицы циклической АМФ-зависимой протеинкиназы из сердечной мышцы крупного рогатого скота» . Труды Национальной академии наук Соединенных Штатов Америки . 79 (20): 6128–31. Bibcode : 1982PNAS ... 79.6128C . DOI : 10.1073 / pnas.79.20.6128 . PMC 347072 . PMID 6959104 .
- ^ а б Эйткен, А; Коэн, П; Сантикарн, S; Уильямс, DH; Calder, AG; Смит, А; Клее, CB (27 декабря 1982 г.). «Идентификация NH2-концевой блокирующей группы кальциневрина B как миристиновая кислота». Письма FEBS . 150 (2): 314–8. DOI : 10.1016 / 0014-5793 (82) 80759-х . PMID 7160476 . S2CID 40889752 .
- ^ a b c d e f g h i j Мартин, Дейл Д. О.; Бошам, Эрван; Бертьям, Люк Г. (январь 2011 г.). «Посттрансляционное миристоилирование: жир имеет значение в жизни и смерти клеток». Биохимия . 93 (1): 18–31. DOI : 10.1016 / j.biochi.2010.10.018 . PMID 21056615 .
- ^ а б Бхатнагар, РС; Fütterer, K; Waksman, G; Гордон, JI (23 ноября 1999 г.). «Структура миристоил-КоА: протеин N-миристоилтрансфераза». Biochimica et Biophysica Acta (BBA) - молекулярная и клеточная биология липидов . 1441 (2–3): 162–72. DOI : 10.1016 / s1388-1981 (99) 00155-9 . PMID 10570244 .
- ^ Снайдер, Джаред. «Обзор посттрансляционных модификаций (PTM)» . Thermo Scientific.
- ^ Чен, Кэтрин А .; Мэннинг, Дэвид Р. (2001). «Регулирование G белков ковалентной модификацией» . Онкоген . 20 (13): 1643–1652. DOI : 10.1038 / sj.onc.1204185 . PMID 11313912 .
- ^ a b c Маклафлин, Стюарт; Адерем, Алан (июль 1995 г.). «Миристоил-электростатический переключатель: модулятор обратимых межмембранных взаимодействий». Направления биохимических наук . 20 (7): 272–276. DOI : 10.1016 / S0968-0004 (00) 89042-8 . PMID 7667880 .
- ^ а б Райт, Меган Х .; Heal, William P .; Манн, Дэвид Дж .; Тейт, Эдвард В. (7 ноября 2009 г.). «Миристоилирование белков в здоровье и болезни» . Журнал химической биологии . 3 (1): 19–35. DOI : 10.1007 / s12154-009-0032-8 . PMC 2816741 . PMID 19898886 .
- ^ Левенталь, Илья; Гжибек, Михал; Саймонс, Кай (3 августа 2010 г.). «Смазывая их путь: модификации липидов определяют ассоциацию белков с мембранными рафтами». Биохимия . 49 (30): 6305–6316. DOI : 10.1021 / bi100882y . PMID 20583817 .
- ^ ХАЯСИ, Нобухиро; ТИТАНИ, Коити (2010). «N-миристоилированные белки, ключевые компоненты в системах передачи внутриклеточного сигнала, обеспечивающие быстрые и гибкие клеточные ответы» . Труды Японской академии, серии B . 86 (5): 494–508. Bibcode : 2010PJAB ... 86..494H . DOI : 10,2183 / pjab.86.494 . PMC 3108300 . PMID 20467215 .
- ^ Wall, Mark A .; Коулман, Дэвид Э .; Ли, Итан; Иньигес-Ллухи, Хорхе А .; Познер, Брюс А .; Гилман, Альфред Дж .; Спранг, Стивен Р. (декабрь 1995 г.). «Структура гетеротримера G-белка Giα1β1γ2» . Cell . 83 (6): 1047–1058. DOI : 10.1016 / 0092-8674 (95) 90220-1 . PMID 8521505 .
- ^ а б Сёдзи, S; Кубота, Y (февраль 1989 г.). «[Функция белкового миристоилирования в клеточной регуляции и вирусной пролиферации]» . Yakugaku Zasshi . 109 (2): 71–85. DOI : 10,1248 / yakushi1947.109.2_71 . PMID 2545855 .
- ^ Ханахан, Дуглас; Вайнберг, Роберт А. (март 2011 г.). «Признаки рака: следующее поколение» . Cell . 144 (5): 646–674. DOI : 10.1016 / j.cell.2011.02.013 . PMID 21376230 .
- ^ Hearps, AC; Янс, Д.А. (март 2007 г.). «Регулирование функций матричного белка ВИЧ-1». Исследования СПИДа и ретровирусы человека . 23 (3): 341–6. DOI : 10,1089 / aid.2006.0108 . PMID 17411366 .