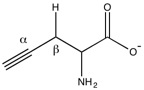
Цистатионин гамма-лиаза - Cystathionine gamma-lyase
| цистатионин гамма-лиаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
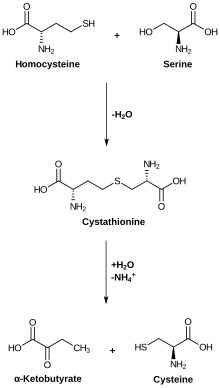 Метаболизм цистеина. Цистатионаза катализирует низшую реакцию.
| |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 4.4.1.1 | ||||||||
| Количество CAS | 9012-96-8 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
| цистатионаза (цистатионин гамма-лиаза) | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Идентификаторы | |||||||
| Символ | CTH | ||||||
| Ген NCBI | 1491 | ||||||
| HGNC | 2501 | ||||||
| OMIM | 607657 | ||||||
| RefSeq | NM_001902 | ||||||
| UniProt | P32929 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 4.4.1.1 | ||||||
| Locus | Chr. 1 п. 31.1 | ||||||
| |||||||
Цистатионин-гамма-лиаза ( CTH или CSE ; также цистатионаза ) - это фермент, расщепляющий цистатионин на цистеин , α-кетобутират и аммиак . Пиридоксальфосфат - простетическая группа этого фермента.
Цистатионин гамма-лиаза также катализирует следующие реакции элиминации:
- L- гомосерин с образованием H 2 O, NH 3 и 2-оксобутаноата
- L- цистин , продуцирующий тиоцистеин, пируват и NH 3
- L- цистеин, продуцирующий пируват, NH 3 и H 2 S
У некоторых бактерий и млекопитающих , включая человека, этот фермент участвует в образовании сероводорода . Сероводород - один из немногих газов, который, как недавно было обнаружено, играет роль в передаче сигналов клетками в организме.
Ферментный механизм
Цистатионаза использует пиридоксальфосфат для облегчения расщепления связи сера-гамма-углерод цистатионина, что приводит к высвобождению цистеина. После этого внешний кетимин гидролизуется, вызывая высвобождение α-кетобутирата. Лизин остатки реформы внутренного Альдимина путем сбрасывая аммиак уходящего группы.
Аминогруппа цистатионина депротонирована и подвергается нуклеофильной атаке внутреннего альдимина. Дополнительное депротонирование общим основанием приводит к образованию внешнего альдимина и удалению остатка лизина. Затем основной остаток лизина способен депротонировать альфа-углерод, перемещая электронную плотность в азот пиридинового кольца. Пиридоксальфосфат необходим для стабилизации этого карбанионного интермедиата; в противном случае pKa протона будет слишком высоким. Затем бета-углерод депротонируется, создавая альфа-бета-ненасыщенность и выталкивая неподеленную пару на альдиминовый азот. Чтобы преобразовать альдимин, эта неподеленная пара отталкивается, разрывая связь сера-гамма-углерод, что приводит к высвобождению цистеина.
Пиридоксаминовое производное винилглиоксилата остается после гамма- элиминирования . Неподеленная пара из пиридинового азота подталкивает электронную плотность к гамма-углероду, который протонируется лизином. Затем лизин атакует внешний альдимин, подталкивая электронную плотность к бета-углероду, который протонируется общей кислотой. Затем имин гидролизуют с высвобождением α-кетобутирата. Депротонирование остатка лизина вызывает удаление аммиака, завершая каталитический цикл .
Цистатионин-гамма-лиаза также проявляет гамма-синтазную активность в зависимости от присутствующих концентраций реагентов. Механизмы остаются такими же, пока они не расходятся после образования производного винилглиоксилата. В механизме гамма-синтазы гамма-углерод атакуется нуклеофилом серы, что приводит к образованию новой связи сера-гамма-углерод.
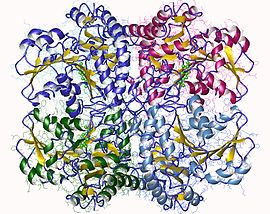
Структура фермента
Цистатионин-гамма-лиаза является членом семейства PLP-зависимых ферментов метаболизма Cys / Met. Другие члены включают цистатионин-гамма-синтазу, цистатионин-бета-лиазу и метионин-гамма-лиазу. Он также является членом более широкого семейства аспартатаминотрансфераз . Как и многие другие PLP-зависимые ферменты, цистатионин-гамма-лиаза представляет собой тетрамер с симметрией D2 .
Пиридоксальфосфат связывается в активном центре с помощью Lys 212 .
Актуальность болезни
Цистеин является субстратом, ограничивающим скорость синтеза глутатиона в глазу. Глутатион - антиоксидант, который защищает кристаллины глаза от активных форм кислорода; денатурированные кристаллины могут привести к катаракте . Цистатионаза также является мишенью для активных форм кислорода. Таким образом, по мере окисления цистатионазы ее активность снижается, вызывая уменьшение цистеина и, в свою очередь, глутатиона в глазу, что приводит к снижению доступности антиоксидантов, вызывая дальнейшее снижение активности цистатионазы. Также было показано, что недостаточность цистатионазной активности способствует истощению запасов глутатиона у пациентов с раком и СПИДом .
Мутации и дефицит цистатионазы связаны с цистатионинурией . Мутации T67I и Q240E ослабляют сродство фермента к пиридоксальфосфату, кофактору, жизненно важному для ферментативной функции. Низкие уровни H 2 S также были связаны с гипертензией у мышей.
Чрезмерные уровни H 2 S, из - за повышенной активности cystathionase, связаны с эндотоксемии , острый панкреатит , геморрагический шок , и сахарный диабет .
Propargylglycine и β-cyanoalanine два необратимые ингибиторы из cystathionase , используемых для лечения повышенной Н 2 уровня S. Механически аминогруппа пропаргилглицина атакует альдимин с образованием внешнего альдимина. Затем β-положение алкина депротонируется с образованием аллена , который затем подвергается атаке фенолом Tyr 114 . Внутренний альдимин может регенерироваться, но вновь созданный виниловый эфир стерически препятствует активному центру , блокируя цистеин от атаки пиридоксальфосфата.
Регулирование
H 2 S снижает транскрипцию цистатионазы при концентрациях от 10 до 80 мкМ. Однако транскрипция увеличивается при концентрациях около 120 мкМ и полностью подавляется при концентрациях, превышающих 160 мкМ.
Смотрите также
Рекомендации
внешняя ссылка
- Цистатионин + гамма-лиаза в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)