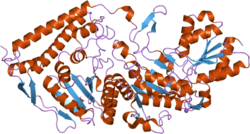
Пируватдегидрогеназа (липоамид) бета - Pyruvate dehydrogenase (lipoamide) beta
Пируватдегидрогеназный (липоамид) бета , также известную как пируватдегидрогеназный Е1 компонента субъединица бета, митохондриальная или PDHE1-Б представляет собой фермент , который у человека кодируется PDHB ген . Комплекс пируватдегидрогеназы (PDH) представляет собой кодируемый ядром митохондриальный мультиферментный комплекс, который катализирует общее превращение пирувата в ацетил-CoA и CO 2 и обеспечивает первичное звено между гликолизом и циклом трикарбоновой кислоты ( TCA ). Комплекс PDH состоит из нескольких копий трех ферментных компонентов: пируватдегидрогеназы (E1), дигидролипоамидацетилтрансферазы (E2) и липоамиддегидрогеназы (E3). Фермент E1 представляет собой гетеротетрамер из двух альфа- и двух бета-субъединиц. Этот ген кодирует бета-субъединицу E1. Мутации в этом гене связаны с дефицитом пируватдегидрогеназы E1-бета.
Состав
Гены PDH, которые составляют субъединицу E1, имеют длину 1,36 тыс. Пар оснований (альфа) и 1,69 т.п.н. (бета). Ген PDHB имеет всего 10 экзонов и 9 интронов. Все сплайсинговые соединения интрон-экзон подчиняются стандартному правилу GT / AG. В интронах 2 и 8 было обнаружено семейство Alu. Ген 5'-фланкирующей области содержит консенсусную промоторную последовательность «СААТ», но не последовательность «ТАТА». Сайт начала транскрипции представляет собой остаток аденина, расположенный на 132 п.о. выше кодона инициации в экзоне 1. Вид мРНК, полученный в результате транскрипции PDHB, был экспериментально определен с помощью Нозерн-блоттинга , как длина 1,6 т.п.н., хотя другой фрагмент - 5,5 т.п. долго также был идентифицирован.
Ген PDHB кодирует белок-предшественник, который имеет 359 аминокислотных остатков, и конечный зрелый белок, который состоит из 329 аминокислот и является частью мультиферментного комплекса пируватдегидрогеназы . Два зрелых белка PDHB объединяются с двумя белками PDHA с образованием гетеротетрамерной субъединицы E1. Кристаллические структуры позволили создать модель, в которой фермент подвергается 2-A челночному движению своих гетеродимеров для осуществления катализа. В частности, каталитический остаток был идентифицирован на субъединице PDHB, 89-м остатке, который представляет собой глутамат. При образовании всего комплекса PDH 289-й бета-остаток аспарагиновой кислоты взаимодействует с 276-м остатком комплекса E2, лизином. Весь комплекс человека имеет размер 9,5 МДа и был описан как 60-мерный, что означает, что более 60 компонентов собраны, чтобы образовать весь комплекс. Эти субъединицы консервативны у многих видов, так как функция этого комплекса важна для генерации АТФ для всех эукариот . Каждый компонент отвечает за катализ на одном этапе этого пути; этот комплекс существует с целью передачи промежуточных продуктов каждой реакции следующему ферменту, что значительно увеличивает скорость реакции.
Функция
Комплекс пируватдегидрогеназы отвечает за окислительное декарбоксилирование пирувата , конечным продуктом которого является ацетил-КоА . Всего комплекс катализирует пять реакций, из которых общая реакция:
Пируват + CoA + NAD + → ацетил-CoA + CO 2
Есть три различных коферментов , необходимых в течение 5 шагов , что этот комплекс осуществляет: тиамин пирофосфат (ТЭС), липоамид и коэнзима А . Этот этап - только один из центральных метаболических путей, осуществляемых эукариотами, при котором глюкоза окисляется с образованием углекислого газа, воды и АТФ . Комплекс E1 специально использует кофактор TPP для расщепления связи Calpha-C (= O) пирувата, а затем переносит ацетильную группу на кофермент TPP, что приводит к промежуточному соединению, гидроксилэтил-Tpp * E1, и производству CO 2 . Тиазолиевое кольцо на TPP идеально подходит для присоединения к карбонильным группам и действует как приемник электронов или группа, которая может вытягивать электроны из реакции и стабилизировать электронодефицитный промежуточный продукт. Кроме того, PDHB взаимодействует с пролилгидроксилазой PHD3, чтобы регулировать клеточную активность PDH.
Клиническое значение
Известно, что мутации в гене PDHB вызывают одну из форм недостаточности пируватдегидрогеназы . Дефицит пируватдегидрогеназы характеризуется накоплением в организме химического вещества, называемого молочной кислотой, и множеством неврологических проблем. Признаки и симптомы этого состояния обычно сначала появляются вскоре после рождения, и они могут сильно различаться у разных людей. Наиболее частым признаком является потенциально опасное для жизни накопление молочной кислоты (лактоацидоз), которое может вызывать тошноту, рвоту, серьезные проблемы с дыханием и аномальное сердцебиение. Люди с дефицитом пируватдегидрогеназы обычно также имеют неврологические проблемы. У большинства задерживается развитие умственных способностей и моторики, таких как сидение и ходьба. Другие неврологические проблемы могут включать умственную отсталость, судороги, слабый мышечный тонус ( гипотония ), плохую координацию и трудности при ходьбе. У некоторых пораженных людей есть аномальные структуры мозга, такие как недоразвитие ткани, соединяющей левую и правую половинки мозга ( мозолистое тело ), истощение (атрофия) внешней части мозга, известной как кора головного мозга, или участки поврежденного ткань (поражения) на некоторых участках головного мозга . Из-за серьезных последствий для здоровья многие люди с дефицитом пируватдегидрогеназы не доживают до детства, хотя некоторые могут дожить до подросткового или взрослого возраста. Большинство случаев дефицита пируватдегидрогеназного комплекса (PDHc) связано с мутациями в гене PDHA1, который кодирует субъединицу E (1) α, при этом описано несколько случаев мутаций в генах E3, E3BP и E2. Однако есть несколько случаев, когда мутации в гене бета-субъединицы приводили к появлению пациентов с синдромом Ли . Описано множество патологических мутаций, в том числе: R36C, который приводит к конформационным изменениям из-за усиления аминокислотных взаимодействий; C306R, в целом влияющий на взаимодействие двух бета-субъединиц; I142M, влияющий на конформацию вокруг иона калия , тем самым снижая стабильность PDHB; W165S, который также влияет на гидрофобное взаимодействие между бета-субъединицами; и Y132C. Были описаны другие случаи, в которых патологические мутации отсутствуют, но врожденные ошибки метаболизма, особенно связанные с убиквитинизацией и протеасомными механизмами, привели к дефициту PDHB. Это было продемонстрировано восстановлением активности ПДГ в клетках, обработанных MG132, который известен как ингибитор протеасом. Клинические проявления этого дефицита аналогичны таковым при дефиците PDHA1, за исключением того, что атаксия в этих случаях встречается реже и что родство было обнаружено только в семьях с дефицитом PDHB.
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.
использованная литература
дальнейшее чтение
- Ciszak EM, Короткина LG, Dominiak PM, Sidhu S, Patel MS (июнь 2003 г.). «Структурные основы триггерного действия тиаминпирофосфат-зависимых ферментов, выявленных пируватдегидрогеназой человека» . Журнал биологической химии . 278 (23): 21240–6. DOI : 10.1074 / jbc.M300339200 . PMID 12651851 .
- Окадзима К., Короткина Л.Г., Прасад С., Рупар Т., Филлипс Дж. А., Фичичиоглу С., Хертекант Дж., Патель М.С., Керр Д.С. (апрель 2008 г.). «Мутации гена субъединицы E1beta (PDHB) в четырех семьях с дефицитом пируватдегидрогеназы». Молекулярная генетика и метаболизм . 93 (4): 371–80. DOI : 10.1016 / j.ymgme.2007.10.135 . PMID 18164639 .
- Кимура К., Вакамацу А., Сузуки И., Ота Т., Нисикава Т., Ямасита Р., Ямамото Дж., Секин М., Цуритани К., Вакагури Х., Исии С., Сугияма Т., Сайто К., Исоно Ю., Ирие Р., Кушида Н., Йонеяма Т. , Otsuka R, Kanda K, Yokoi T, Kondo H, Wagatsuma M, Murakawa K, Ishida S, Ishibashi T, Takahashi-Fujii A, Tanase T, Nagai K, Kikuchi H, Nakai K, Isogai T, Sugano S (январь 2006 г.) ). «Диверсификация транскрипционной модуляции: широкомасштабная идентификация и характеристика предполагаемых альтернативных промоторов генов человека» . Геномные исследования . 16 (1): 55–65. DOI : 10.1101 / gr.4039406 . PMC 1356129 . PMID 16344560 .
- Wiemann S, Weil B, Wellenreuther R, Gassenhuber J, Glassl S, Ansorge W, Böcher M, Blöcker H, Bauersachs S, Blum H, Lauber J, Düsterhöft A, Beyer A, Köhrer K, Strack N, Mewes HW, Ottenwälder B , Обермайер Б., Тампе Дж., Хойбнер Д., Вамбутт Р., Корн Б., Кляйн М., Поустка А. (март 2001 г.). «К каталогу генов и белков человека: секвенирование и анализ 500 новых полных белков, кодирующих кДНК человека» . Геномные исследования . 11 (3): 422–35. DOI : 10.1101 / гр . GR1547R . PMC 311072 . PMID 11230166 .
- Браун Р.М., руководитель RA, Бубриак II, Леонард Дж. В., Томас Н.Х., Браун Г.К. (июль 2004 г.). «Мутации в гене субъединицы E1beta: новая причина дефицита пируватдегидрогеназы» . Генетика человека . 115 (2): 123–7. DOI : 10.1007 / s00439-004-1124-8 . PMID 15138885 . S2CID 30741075 .
- Sugden MC, Holness MJ (май 2003 г.). «Последние достижения в механизмах, регулирующих окисление глюкозы на уровне пируватдегидрогеназного комплекса с помощью PDK». Американский журнал физиологии. Эндокринология и обмен веществ . 284 (5): E855–62. DOI : 10,1152 / ajpendo.00526.2002 . PMID 12676647 .
- Судзуки Ю., Ёситомо-Накагава К., Маруяма К., Суяма А., Сугано С. (октябрь 1997 г.). «Создание и характеристика полноразмерной библиотеки кДНК, обогащенной по 5'-концу». Джин . 200 (1–2): 149–56. DOI : 10.1016 / S0378-1119 (97) 00411-3 . PMID 9373149 .
- Короткина Л.Г., Пател М.С. (фев 2008). «Связывание пируватдегидрогеназы с ядром пируватдегидрогеназного комплекса человека» . Письма FEBS . 582 (3): 468–72. DOI : 10.1016 / j.febslet.2007.12.041 . PMC 2262399 . PMID 18206651 .
- Фанг Р., Никсон П.Ф., Дагглби Р.Г. (октябрь 1998 г.). «Идентификация каталитического глутамата в компоненте E1 пируватдегидрогеназы человека». Письма FEBS . 437 (3): 273–7. DOI : 10.1016 / S0014-5793 (98) 01249-6 . PMID 9824306 . S2CID 40849431 .
- Хан З, Чжун Л., Шривастава А., Стакпул П. В. (январь 2008 г.). «Дефицит пируватдегидрогеназного комплекса, вызванный убиквитинированием и протеасомной деградацией субъединицы E1» . Журнал биологической химии . 283 (1): 237–43. DOI : 10.1074 / jbc.M704748200 . PMID 17923481 .
- Caruso M, Maitan MA, Bifulco G, Miele C, Vigliotta G, Oriente F, Formisano P, Beguinot F (ноябрь 2001 г.). «Активация и митохондриальная транслокация протеинкиназы Cdelta необходимы для стимуляции инсулином активности комплекса пируватдегидрогеназы в клетках мышц и печени» . Журнал биологической химии . 276 (48): 45088–97. DOI : 10.1074 / jbc.M105451200 . PMID 11577086 .
- Хирнер С., Кроне С., Шустер А., Хоффманн С., Витт С., Эрбер Р., Штихт С., Гаш А., Лабейт С., Лабейт Д. (июнь 2008 г.). «MuRF1-зависимая регуляция системного метаболизма углеводов, выявленная в исследованиях на трансгенных мышах». Журнал молекулярной биологии . 379 (4): 666–77. DOI : 10.1016 / j.jmb.2008.03.049 . PMID 18468620 .
- Мехрле А., Розенфельдер Х., Шупп И., дель Валь С., Арльт Д., Хане Ф., Бектель С., Симпсон Дж., Хофманн О., Хиде В., Глаттинг К. Х., Хубер В., Пепперкок Р., Поустка А., Виманн С. (январь 2006 г.). «База данных LIFEdb в 2006 году» . Исследования нуклеиновых кислот . 34 (выпуск базы данных): D415–8. DOI : 10.1093 / NAR / gkj139 . PMC 1347501 . PMID 16381901 .
- Хиромаса Ю., Фудзисава Т., Асо Ю., Roche TE (февраль 2004 г.). «Организация ядер комплекса пируватдегидрогеназы млекопитающих, образованного E2 и E2 плюс E3-связывающий белок, и их способность связывать компоненты E1 и E3» . Журнал биологической химии . 279 (8): 6921–33. DOI : 10.1074 / jbc.M308172200 . PMID 14638692 .
- Хартли Дж. Л., Темпл Г. Ф., Браш Массачусетс (ноябрь 2000 г.). «Клонирование ДНК с использованием сайт-специфической рекомбинации in vitro» . Геномные исследования . 10 (11): 1788–95. DOI : 10.1101 / gr.143000 . PMC 310948 . PMID 11076863 .
- Боналдо М.Ф., Леннон Г., Соарес МБ (сентябрь 1996 г.). «Нормализация и вычитание: два подхода к облегчению открытия генов» . Геномные исследования . 6 (9): 791–806. DOI : 10.1101 / gr.6.9.791 . PMID 8889548 .
- Маруяма К., Сугано С. (январь 1994 г.). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Джин . 138 (1–2): 171–4. DOI : 10.1016 / 0378-1119 (94) 90802-8 . PMID 8125298 .
- Wiemann S, Arlt D, Huber W., Wellenreuther R, Schleeger S, Mehrle A, Bechtel S, Sauermann M, Korf U, Pepperkok R, Sültmann H, Poustka A (октябрь 2004 г.). «От ORFeome к биологии: конвейер функциональной геномики» . Геномные исследования . 14 (10B): 2136–44. DOI : 10.1101 / gr.2576704 . PMC 528930 . PMID 15489336 .
Эта статья включает текст из Национальной медицинской библиотеки США , который находится в общественном достоянии .