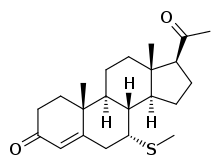
7α-Тиопрогестерон - 7α-Thioprogesterone
 | |
| Клинические данные | |
|---|---|
| Другие имена | 7α-TP4; SC-8365; 7α-Меркаптопрегн-4-ен-3,20-дион |
| Идентификаторы | |
| |
| Химические и физические данные | |
| Формула | C 21 H 28 O 2 S |
| Молярная масса | 344,51 г · моль -1 |
| 3D модель ( JSmol ) | |
| |
| |
7α-Тиопрогестерон ( 7α-TP4 ; кодовое название SC-8365 ; также известный как 7α-меркаптопрегн-4-ен-3,20-дион ) представляет собой синтетический , стероидный и мощный антиминералокортикоид (предполагаемый) и антиандроген, который был разработан GD Searle & Co и был описан в конце 1970-х - начале 1980-х годов, но никогда не был разработан и не внедрен для медицинского использования. Это является производным от прогестерона (прегно-4-ен-3,20-дион) с тио ( серы ) замещениями в положении C7α, и относится к spirolactone группе препаратов , но не хватает Г- лактон кольца .
В качестве антиандрогенов, 7α-ТР4 имеет приблизительно 8,5% от аффинности в дигидротестостерон (ДГТ) для крыс вентральной простаты андрогенного рецептора (AR), который похож на спиронолактон и его активного метаболита 7 &-тиометилспиролактона . Препарат также оценивался на белках-носителях, связанных со стероидными гормонами , и показал очень низкое связывание с глобулином, связывающим половые гормоны (SHBG), но высокое сродство к кортикостероидсвязывающему глобулину (CBG), примерно такое же, как у прогестерона.
Было обнаружено, что 7α-ацетилтио-17α-гидроксипрогестерон , родственное производное прогестерона, а также 17α-гидроксипрогестерона , аналогичным образом обладает сильной антиминералокортикоидной активностью. Спиронолактон является производным этого соединения, в котором ацетильная группа в положении C17β циклизована с гидроксильной группой C17α с образованием γ- лактонного кольца спиро 21- карбоновой кислоты .
использованная литература
