Синдром Гудпасчера - Goodpasture syndrome
| Синдром Гудпасчера | |
|---|---|
| Другие имена | Болезнь Гудпасчера, болезнь антиглубоких базальных антител, болезнь анти-GBM |
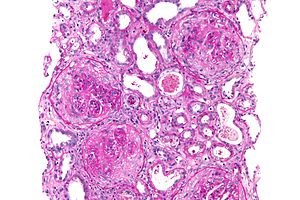 | |
| Микрофотография из серповидного гломерулонефрита , который был показан , чтобы быть antiglomerular фундамента мембранной болезнью, ПАС пятно | |
| Специальность |
Нефрология , пульмонология , иммунология |
Синдром Гудпасчера (GPS) , также известный как болезнь антигломерулярной базальной мембраны , представляет собой редкое аутоиммунное заболевание, при котором антитела атакуют базальную мембрану легких и почек, что приводит к кровотечению из легких, гломерулонефриту и почечной недостаточности . Считается, что он атакует альфа-3-субъединицу коллагена типа IV , который поэтому был назван антигеном Goodpasture. Синдром Гудпасчера может быстро привести к необратимому повреждению легких и почек, что часто приводит к смерти. Его лечат лекарствами, подавляющими иммунную систему, такими как кортикостероиды и циклофосфамид , а также плазмаферезом , при котором антитела удаляются из крови.
Заболевание было впервые описано американским патологом Эрнестом Гудпастуром из Университета Вандербильта в 1919 году и позже было названо в его честь.
Признаки и симптомы
Антитела против базальной мембраны клубочков (GBM) в первую очередь атакуют почки и легкие, хотя общие симптомы, такие как недомогание, потеря веса, усталость, лихорадка и озноб, также распространены, как и боли в суставах. От 60 до 80% людей с этим заболеванием страдают как легкие, так и почки; 20-40% имеют поражение только почек и менее 10% имеют поражение только легких. Легочные симптомы обычно предшествуют почечным симптомам и обычно включают: кашель с кровью , боль в груди (менее чем в 50% случаев в целом), кашель и одышку . Почечные симптомы обычно включают кровь в моче , белок в моче , необъяснимый отек конечностей или лица , высокое количество мочевины в крови и высокое кровяное давление .
Причина
Хотя точная причина неизвестна, генетическая предрасположенность к GPS связана с системой человеческого лейкоцитарного антигена (HLA), в частности, HLA-DR15 . В дополнение к генетической предрасположенности, необходимо первоначальное воздействие окружающей среды на легочную сосудистую сеть, чтобы позволить антителам антигломерулярной базальной мембраны (анти-GBM) достичь альвеолярных капилляров . Примеры такого поражения включают: воздействие органических растворителей (например, хлороформ ) или углеводородов, воздействие табачного дыма, инфекцию (например, грипп A ), вдыхание кокаина, вдыхание металлической пыли, бактериемию , сепсис , среду с высоким содержанием кислорода и антилимфоцитарную терапию. (особенно с моноклональными антителами ). Воздействие химикатов для химической чистки и средства от сорняков марки Paraquat также считается потенциальным оскорблением. В GPS антитела против GBM производятся и циркулируют по кровотоку, повреждая мембраны, выстилающие легкие и почки, а также поражая их капилляры.
Патофизиология
GPS вызывается аномальной выработкой плазматическими клетками антител против GBM. Основной мишенью этих аномальных антител является неколлагеновый домен альфа-3 цепи коллагена 4 типа, который в основном обнаруживается в базальных мембранах клубочковых и альвеолярных капилляров, что объясняет неясные специфические симптомы этого состояния. Эти антитела связывают свои реактивные эпитопы с базальными мембранами и активируют каскад комплемента, что приводит к гибели меченых клеток. Связывание специфического антитела и эпитопа, которое проявляет наивысшее сродство и является патогенным, происходит между антителами GP A и областью эпитопа против GBM, обозначенной E A , которая представляет собой остатки 17-31 субъединицы альфа 3 неколлагенового домена типа IV. коллаген. Также вовлечены Т-клетки , хотя обычно это считается реакцией гиперчувствительности II типа.
Диагностика
Диагностика GPS часто затруднена, так как многочисленные другие заболевания могут вызывать различные проявления состояния, а само состояние встречается редко. Наиболее точным способом постановки диагноза является исследование пораженных тканей с помощью биопсии , особенно почки, поскольку это наиболее изученный орган для получения образца на наличие антител против GBM. Помимо антител против GBM, вовлеченных в заболевание, примерно каждый третий из пораженных также имеет цитоплазматические антинейтрофильные антитела в кровотоке, которые часто опережают антитела против GBM примерно на несколько месяцев или даже лет. Чем позже будет диагностировано заболевание, тем хуже для больного.
Кроме того, если есть существенное подозрение на заболевание, сералогическое тестирование для анализа ELISA обычно выполняется путем поиска области домена альфа3 NC1 коллагена IV, чтобы избежать ложноположительных результатов.
Уход
Основным методом лечения GPS является плазмаферез , процедура, при которой кровь пострадавшего проходит через центрифугу и различные компоненты разделяются в зависимости от веса. Плазма содержит анти-GBM антитела , которые атакуют легкие и почки пострадавшего, и отфильтровывают. Другие части крови ( эритроциты , лейкоциты и тромбоциты ) рециркулируют и повторно вводят внутривенно. Большинство людей, страдающих этим заболеванием, также нуждаются в лечении иммунодепрессантами , особенно циклофосфамидом , преднизоном и ритуксимабом , чтобы предотвратить образование новых антител против GBM и предотвратить дальнейшее повреждение почек и легких. Другие, менее токсичные иммунодепрессанты, такие как азатиоприн, могут использоваться для поддержания ремиссии.
Прогноз
При лечении пятилетняя выживаемость составляет> 80%, и менее 30% больных нуждаются в длительном диализе. Исследование, проведенное в Австралии и Новой Зеландии, показало, что у пациентов, которым требуется заместительная почечная терапия (включая диализ), среднее время выживания составляет 5,93 года. Без лечения практически каждый пострадавший умрет либо от тяжелой почечной недостаточности, либо от кровоизлияния в легкие.
Эпидемиология
GPS встречается редко, поражая около 0,5–1,8 на миллион человек в год в Европе и Азии. Это также необычно среди аутоиммунных заболеваний , поскольку чаще встречается у мужчин, чем у женщин, а также реже встречается у чернокожих, чем у белых, но чаще встречается у маори в Новой Зеландии. Пиковый возраст начала заболевания - 20–30 и 60–70 лет.
Смотрите также
использованная литература
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |