Гемопексин - Hemopexin
Гемопексина (или хамопексин ; HPX; Нх), также известная как бета-1b-гликопротеин, является гликопротеином , что в организме человека кодируются HPX геном и принадлежит гемопексину семейству белков. Гемопексин - это белок плазмы с самым высоким сродством связывания с гемом.
Сам гемоглобин , циркулирующий отдельно в плазме крови (называемый свободным гемоглобином , в отличие от гемоглобина, живущего в эритроците и циркулирующего с ним), вскоре будет окислен до метгемоглобина, который затем диссоциирует на свободный гем вместе с цепью глобина . Затем свободный гем будет окислен до свободного мет-гема, и рано или поздно гемопексин свяжет свободный мет-гем вместе, образуя комплекс мет-гема и гемопексина, продолжая свой путь в кровообращении до достижения рецептора, такого как как CD91 , на гепатоцитах или макрофагах в селезенке, печени и костном мозге.
Поступление и последующее связывание гемопексина со свободным гемом не только предотвращает прооксидантные и провоспалительные эффекты гема, но также способствует детоксикации свободного гема.
Важно различать гемопексин и гаптоглобин , последний всегда связывается со свободным гемоглобином . (См. Гаптоглобин § Дифференциация с гемопексином )
Клонирование, выражение и открытие
Takahashi et al. (1985) определили, что Hx плазмы человека состоит из одной полипептидной цепи из 439 аминокислотных остатков с шестью внутрицепочечными дисульфидными мостиками и имеет молекулярную массу приблизительно 63 кДа. Амино-концевой остаток треонина заблокирован O-связанный галактозамин олигосахарида , и белок имеет пять глюкозамина N-олигосахариды связаны с последовательностью акцепторной Asn-X-Ser / Thr. 18 остатков триптофана расположены в четыре кластера, а 12 триптофанов консервативны в гомологичных положениях. Компьютерный анализ внутренней гомологии в аминокислотной последовательности предположил дупликацию предкового гена, что указывает на то, что Hx состоит из двух одинаковых половин.
Альтруда и др. (1988) продемонстрировали, что ген HPX занимает примерно 12 т.п.н. и прерывается 9 экзонами. Демонстрация показывает прямое соответствие между экзонами и 10 повторяющимися единицами в белке. Интроны не были размещены случайным образом; они попали в центр области гомологии аминокислотной последовательности в поразительно сходных местах в 6 из 10 единиц и в симметричном положении в каждой половине кодирующей последовательности. На основании этих наблюдений Altruda et al. (1988) пришли к выводу, что ген эволюционировал через интрон-опосредованные дупликации первичной последовательности до 5-экзонного кластера.
Картирование гена гемопексина
Cai и Law (1986) подготовили клон кДНК для Hx путем саузерн-блоттинга гибридов человека / хомяка, содержащих различные комбинации хромосом человека, приписали ген HPX хромосоме 11 человека. Law et al. (1988) с помощью гибридизации in situ приписали ген HPX к 11p15.5-p15.4, в том же месте, что и комплекс генов бета-глобина .
Дифференциальный паттерн транскрипции гена гемопексина
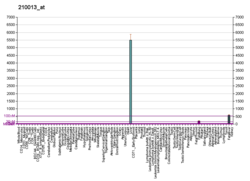
В 1986 году экспрессия гена HPX человека в различных тканях и клеточных линиях человека была проведена с использованием специфического зонда кДНК. На основании полученных результатов был сделан вывод, что этот ген был экспрессирован в печени и был ниже уровня обнаружения в других исследованных тканях или клеточных линиях. При картировании S1 сайт инициации транскрипции в клетках печени был расположен на 28 пар оснований выше кодона инициации AUG гена гемопексина.
Функция
Hx связывает гем с самым высоким сродством из всех известных белков . Его основная функция - удаление гема, высвободившегося или потерянного в результате обмена гемовых белков, таких как гемоглобин, и, таким образом, защита организма от окислительного повреждения, которое может вызвать свободный гем. Кроме того, Hx высвобождает связанный лиганд для интернализации при взаимодействии с CD91 . Hx сохраняет железо в организме . Hx-зависимое поглощение внеклеточного гема может привести к деактивации репрессии Bach1, что приводит к транскрипционной активации гена антиоксидантной гемоксигеназы-1. Гемоглобин, гаптоглобин (Hp) и Hx связаны с липопротеинами высокой плотности (HDL) и влияют на воспалительные свойства HDL. Hx может подавлять рецептор ангиотензина II типа 1 (AT1-R) in vitro .
Клиническое значение
Преобладающим источником циркулирующего Hx является печень с концентрацией в плазме 1-2 мг / мл. Уровень Hx в сыворотке отражает количество гема в крови. Таким образом, низкий уровень Hx указывает на то, что произошла значительная деградация гемсодержащих соединений. Низкий уровень Hx является одним из диагностических признаков внутрисосудистой гемолитической анемии . Hx причастен к сердечно-сосудистым заболеваниям , септическому шоку , церебральному ишемическому повреждению и экспериментальному аутоиммунному энцефаломиелиту . Уровень циркулирующего Hx связан с прогнозом у пациентов с септическим шоком.
HPX производится в головном мозге. Делеция гена HPX может усугубить повреждение головного мозга с последующим внутримозговым кровоизлиянием, вызванным бессистемным гемоглобином . Высокий уровень Hx в спинномозговой жидкости связан с плохим исходом после субарахноидального кровоизлияния .
Отношение к гаптоглобину
В прошлом были сообщения, показывающие, что у пациентов с серповидноклеточной анемией , сфероцитозом , аутоиммунной гемолитической анемией , эритропоэтической протопорфирией и дефицитом пируваткиназы снижение концентрации Hx происходит в ситуациях, когда концентрации гаптоглобина (Hp) низки или истощены в результате тяжелый или длительный гемолиз. И Hp, и Hx являются белками острой фазы, синтез которых индуцируется во время инфекции и после воспалительных состояний, чтобы минимизировать повреждение тканей и облегчить восстановление тканей. Hp и Hx предотвращают токсичность гема, связываясь с гемом до прибытия моноцитов или макрофагов и последующего клиренса, что может объяснить их влияние на исход при некоторых заболеваниях и лежит в основе обоснования экзогенных Hp и Hx в качестве терапевтических белков при гемолитических или геморрагических заболеваниях. условия. Гемопексин является основным транспортным средством для переноса гема в плазме.
использованная литература
дальнейшее чтение
- Piccard H, Van den Steen PE, Opdenakker G (апрель 2007 г.). «Домены гемопексина как многофункциональные лигандирующие модули в матриксных металлопротеиназах и других белках» . Журнал биологии лейкоцитов . 81 (4): 870–92. DOI : 10,1189 / jlb.1006629 . PMID 17185359 . S2CID 16210789 .
- Морган В. Т., Мюллер-Эберхард Ю., Ламола А. А. (январь 1978 г.). «Взаимодействие кроличьего гемопексина с билирубином». Biochimica et Biophysica Acta (BBA) - Структура белка . 532 (1): 57–64. DOI : 10.1016 / 0005-2795 (78) 90447-6 . PMID 620056 .
- Лю Х.М., Атак-младший, Рапопорт С.И. (1989). «Иммуногистохимическая локализация внутриклеточных белков плазмы в центральной нервной системе человека». Acta Neuropathologica . 78 (1): 16–21. DOI : 10.1007 / BF00687397 . PMID 2735186 . S2CID 24415663 .
- Смит А., Татум FM, Мустер П., Берч М.К., Морган В.Т. (апрель 1988 г.). «Важность лиганд-индуцированных конформационных изменений гемопексина для рецептор-опосредованного транспорта гема» . Журнал биологической химии . 263 (11): 5224–9. DOI : 10.1016 / S0021-9258 (18) 60703-3 . PMID 2833500 .
- Альтруда Ф, Поли В, Рестаньо Дж, Силенго Л (1988). «Структура гена гемопексина человека и доказательства интрон-опосредованной эволюции». Журнал молекулярной эволюции . 27 (2): 102–8. Bibcode : 1988JMolE..27..102A . DOI : 10.1007 / BF02138368 . PMID 2842511 . S2CID 11271490 .
- Альтруда Ф., Поли В., Рестаньо Дж., Аргос П., Кортезе Р., Силенго Л. (июнь 1985 г.). «Первичная структура гемопексина человека, выведенная из последовательности кДНК: свидетельство внутренней повторяющейся гомологии» . Исследования нуклеиновых кислот . 13 (11): 3841–59. DOI : 10.1093 / NAR / 13.11.3841 . PMC 341281 . PMID 2989777 .
- Taketani S, Kohno H, Naitoh Y, Tokunaga R (июнь 1987 г.). «Выделение рецептора гемопексина из плаценты человека» . Журнал биологической химии . 262 (18): 8668–71. DOI : 10.1016 / S0021-9258 (18) 47465-0 . PMID 3036819 .
- Law ML, Cai GY, Hartz JA, Jones C., Kao FT (июль 1988 г.). «Ген гемопексина отображается в том же месте, что и кластер генов бета-глобина на хромосоме 11 человека». Геномика . 3 (1): 48–52. DOI : 10.1016 / 0888-7543 (88) 90158-9 . PMID 3220477 .
- Морган В. Т., Алам Дж., Дьячук В., Мустер П., Татум Ф. М., Смит А. (июнь 1988 г.). «Взаимодействие гемопексина с Sn-протопорфирин IX, ингибитором гемоксигеназы. Роль гемопексина в захвате печенью Sn-протопорфирина IX и индукции мРНК гемоксигеназы» . Журнал биологической химии . 263 (17): 8226–31. DOI : 10.1016 / S0021-9258 (18) 68467-4 . PMID 3372522 .
- Такахаши Н., Такахаши Ю., Патнэм Ф.В. (январь 1985 г.). «Полная аминокислотная последовательность человеческого гемопексина, гем-связывающего белка сыворотки» . Труды Национальной академии наук Соединенных Штатов Америки . 82 (1): 73–7. Полномочный код : 1985PNAS ... 82 ... 73T . DOI : 10.1073 / pnas.82.1.73 . PMC 396973 . PMID 3855550 .
- Такахаши Н., Такахаши Ю., Патнэм Ф.В. (апрель 1984 г.). «Структура человеческого гемопексина: O-гликозильные и N-гликозильные сайты и необычная кластеризация остатков триптофана» . Труды Национальной академии наук Соединенных Штатов Америки . 81 (7): 2021–5. Bibcode : 1984PNAS ... 81.2021T . DOI : 10.1073 / pnas.81.7.2021 . PMC 345428 . PMID 6371807 .
- Франтикова В., Борвак Дж., Клух И., Моравек Л. (декабрь 1984 г.). «Аминокислотная последовательность N-концевой области гемопексина человека». Письма FEBS . 178 (2): 213–6. DOI : 10.1016 / 0014-5793 (84) 80603-1 . PMID 6510521 . S2CID 45009902 .
- Смит А., Алам Дж., Эскриба П.В., Морган В.Т. (апрель 1993 г.). «Регулирование экспрессии генов гемоксигеназы и металлотионеина аналогами гема, кобальтом и протопорфирином олова» . Журнал биологической химии . 268 (10): 7365–71. DOI : 10.1016 / S0021-9258 (18) 53184-7 . PMID 8463269 .
- Моррис CM, Candy JM, Эдвардсон JA, Bloxham CA, Smith A (январь 1993 г.). «Доказательства локализации иммунореактивности гемопексина в нейронах головного мозга человека». Письма неврологии . 149 (2): 141–4. DOI : 10.1016 / 0304-3940 (93) 90756-B . PMID 8474687 . S2CID 24743139 .
- Hrkal Z, Kuzelová K, Muller-Eberhard U, Stern R (март 1996). «Гиалуронансвязывающие свойства сывороточного гемопексина человека». Письма FEBS . 383 (1–2): 72–4. DOI : 10.1016 / 0014-5793 (96) 00225-6 . PMID 8612795 . S2CID 21283343 .
- Hunt RC, Hunt DM, Gaur N, Smith A (июль 1996 г.). «Гемопексин в сетчатке человека: защита сетчатки от гемопосредованной токсичности». Журнал клеточной физиологии . 168 (1): 71–80. DOI : 10.1002 / (SICI) 1097-4652 (199607) 168: 1 <71 :: AID-JCP9> 3.0.CO; 2-5 . PMID 8647924 .
- Миллер Ю.И., Смит А., Морган В.Т., Шаклай Н. (октябрь 1996 г.). «Роль гемопексина в защите липопротеинов низкой плотности от окисления, вызванного гемоглобином». Биохимия . 35 (40): 13112–7. DOI : 10.1021 / bi960737u . PMID 8855948 .
- Гринберг Л.Н., О'Брайен П.Дж., Хркал З. (июль 1999 г.). «Влияние гем-связывающих белков на пероксидантную и каталатическую активность гемина». Свободная радикальная биология и медицина . 27 (1–2): 214–9. DOI : 10.1016 / S0891-5849 (99) 00082-9 . PMID 10443938 .
- Накадзима С., Морияма Т., Хаяси Х., Саката И., Накаэ Ю., Такемура Т. (февраль 2000 г.). «Гемопексин как белок-носитель опухолевого Ga-металлопорфирина-ATN-2». Письма о раке . 149 (1-2): 221-6. DOI : 10.1016 / S0304-3835 (99) 00367-5 . PMID 10737728 .
- Шипулина Н., Смит А., Морган В. Т. (апрель 2000 г.). «Связывание гема гемопексином: доказательства нескольких способов связывания и функциональных последствий». Журнал химии белков . 19 (3): 239–48. DOI : 10,1023 / A: 1007016105813 . PMID 10981817 . S2CID 45510572 .
внешние ссылки
- Гемопексин в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)