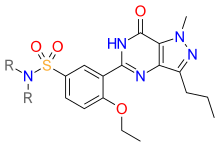
Открытие и разработка ингибиторов фосфодиэстеразы 5 - Discovery and development of phosphodiesterase 5 inhibitors
Фосфодиэстеразы (СРПО) представляют собой надсемейство из ферментов . Это суперсемейство далее подразделяется на 11 семейств, PDE1 - PDE11, на основе регуляторных свойств, аминокислотных последовательностей, специфичности субстрата, фармакологических свойств и распределения в тканях. Их функция заключается в разрушении внутриклеточных вторичных мессенджеров, таких как циклический аденинмонофосфат ( цАМФ ) и циклический гуанозинмонофосфат ( цГМФ ), что приводит к нескольким биологическим процессам, таким как влияние на уровень внутриклеточного кальция через путь Ca 2+ .
Фосфодиэстераза 5 ( PDE5 ) широко экспрессируется в нескольких тканях тела, например в головном мозге, легких, почках, мочевом пузыре, гладких мышцах и тромбоцитах. Можно предотвратить гидролиз цГМФ путем ингибирования ФДЭ5 и, следовательно, лечить заболевания, связанные с низким уровнем цГМФ, из-за этого ФДЭ5 является идеальной мишенью для разработки ингибиторов. Терапевтические эффекты ингибирования PDE5 были продемонстрированы при нескольких сердечно-сосудистых заболеваниях, хроническом заболевании почек и сахарном диабете .
Основными ингибиторами ФДЭ5 (подгруппа ингибиторов фосфодиэстеразы ) являются силденафил , тадалафил , варденафил и аванафил , и, хотя все они имеют один и тот же механизм действия, каждый из них обладает уникальными фармакокинетическими и фармакодинамическими свойствами, которые определяют их пригодность в различных условиях и профиль их побочных эффектов. .
Общий
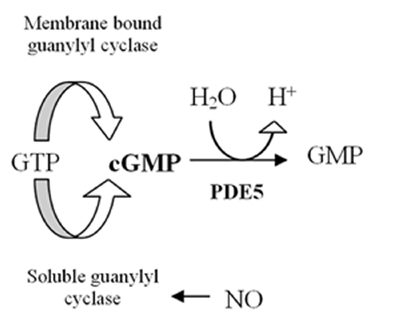
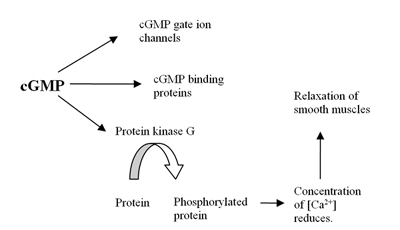
Геном человека содержит , по меньшей мере 21 генов , участвующих в определении внутриклеточные уровни цАМФ и цГМФ по выражению фосфодиэстеразы белков или ООП. Эти PDE сгруппированы по крайней мере в 11 функциональных подсемейств, названных PDE1-PDE11. ФДЭ представляют собой ферменты, которые гидролизуют циклический аденозин-3,5-монофосфат (цАМФ) и циклический гуанозин-3,5-монофосфат (цГМФ), которые являются внутриклеточными вторичными посредниками , в АМФ и GMP. Эти вторичные посланники контролируют многие физиологические процессы. ЦАМФ образуется из АТФ с помощью фермента аденилатциклазы и цГМФ формируется из ГТФ ферментом гуанилатциклазы , которые являются либо мембраны связаны или растворимыми в цитозоле . Когда растворимые функции его в качестве рецептора для оксида азота (NO) (смотри рисунок 1). Формирование цГМФ инициирует несколько реакций в организме , включая влияние на цГМФ ионных каналов , цГМФ связывающих белков и протеинкиназы G (PKG). Воздействие на PKG снижает уровень кальция, что приводит к расслаблению гладких мышц (см. Рисунок 2). Фермент PDE5 специфичен для цГМФ, что означает, что он гидролизует только цГМФ, но не цАМФ. Селективность опосредуется сложной сетью водородных связей, которая благоприятна для цГМФ, но неблагоприятна для цАМФ в ФДЭ5. За счет ингибирования фермента PDE5 концентрация цГМФ будет повышена и, следовательно, может увеличить расслабление гладких мышц. PDE5 имеет только один подтип, PDE5A, из которых у человека есть 4 изоформы, называемые PDE5A1-4. Разница в изоформах PDE5A1-3 заключается только в 5´ конце мРНК и соответствующем N-конце белка.
Распределение ФДЭ5 в организме
У людей распределение изоформ PDE5A1 и PDE5A2 одинаково и может быть обнаружено в головном мозге , легочной ткани, сердце , печени , почках , мочевом пузыре , простате , уретре , половом члене , матке и скелетных мышцах . PDE5A2 встречается чаще, чем PDE5A1. PDE5A3 не так широко распространен, как две другие изоформы, и обнаруживается только в гладкомышечных тканях, он обнаруживается в сердце , мочевом пузыре , простате , уретре , половом члене и матке. Точное распределение изоформы PDE5A4 не было обнаружено в литературе. ФДЭ5 фермент в организме человека также сообщались в тромбоцитах , желудочно - кишечные эпителиальные клетки, клетка Пуркиньи из мозжечка , пещеристые тела , поджелудочная железа , плаценты и толстая кишка, клитор пещеристые тел , а также вагинальный гладких мышц и эпителий.
Структура PDE и SAR
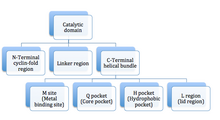
Ферменты PDE состоят из 3 функциональных доменов: N-концевого циклинового складчатого домена, линкерного спирального домена и C-концевого спирального домена пучка (см. Рисунок 3). Активный сайт представляет собой глубокий карман на стыке трех субдоменов и выстлан высококонсервативными остатками между изотипами PDE. Глубина кармана составляет примерно 15 Å, а размер отверстия - примерно 20 на 10 Å. Объем активного центра составляет от 875 до 927 Å 3 . Активный сайт ФДЭ5 был описан как подразделяется на 3 основных регионов на основе его кристаллической структуры в комплексе с силденафилом :
- Участок M: содержит ионы цинка и магния . Роль ионов заключается в стабилизации структуры и активации гидроксида, чтобы опосредовать реакцию. Современные ингибиторы PDE5 не взаимодействуют с ионами металлов, в отличие от цГМФ . Прямые или косвенные взаимодействия могут улучшить эффективность будущих ингибиторов.
- Q-карман: считается, что гуанидиновая группа цГМФ связывается в этой области, поскольку Q-карман вмещает пиразолопиримидиноновую группу (см. Фиг.4) силденафила . Пиразолопиримидинон силденафила имитирует гуанин в цГМФ и имеет те же донорные и акцепторные свойства водородной связи, образуя бидендратную водородную связь с Q817. Card et al. Опишите Q-карман как разделенный на 3 части:
- Седло, образованное консервативным глутамином (Q817 в PDE5A, Q443 в PDE4B и Q369 в PDE4D) и P-зажимом (гидрофобный зажим на узкой стороне кармана активных центров, образованный инвариантным пурин-селективным глутамином и парой консервативных остатки).
- 2 узких гидрофобных кармана, Q1 и Q2, состоящие в основном из гидрофобных остатков по бокам седла.
- Область L: метилпиперазиновая группа (см. Фигуру 4) силденафила окружена остатками Tyr 664, Met 816, Ala 823 и Gly 819, а остатки 662-664 образуют крышку над карманом, сужая вход в активный центр PDE5. .
Jeon et al. также описывают четвертый карман, называемый H-карманом, который является гидрофобным и вмещает этоксифенильную группу силденафила . 3 ингибитора PDE5, уже имеющихся на рынке, силденафил , тадалафил и варденафил , занимают часть активного центра, в основном вокруг Q-кармана, а иногда и M pocket, и все 3 взаимодействуют с активным сайтом тремя важными способами:
- взаимодействие между ионами металлов через воду
- водородная связь с седлом Q-кармана
- гидрофобное взаимодействие с гидрофобными остатками, выстилающими полость активного центра.
Также было описано, что гидрофобное взаимодействие с карманами Q1 и Q2 важно для эффективности ингибитора, и различия между изотипами PDE в кармане Q2 можно использовать для селективности между изотипами.

Роль в болезнях
Эректильная дисфункция
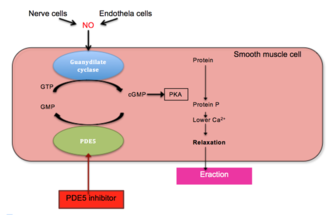
Лекарства, подавляющие ФДЭ5, силденафил , тадалафил и варденафил , используются для лечения эректильной дисфункции . Эти ингибиторы увеличивают цГМФ, расслабление гладких мышц и, следовательно, вызывают эрекцию полового члена во время сексуальной стимуляции.
Легочная артериальная гипертензия
Повышенная регуляция экспрессии гена PDE5 наблюдалась на животных моделях легочной гипертензии и, как полагают, способствует сужению сосудов в легких. Несколько рандомизированных контролируемых исследований по изучению использования ингибиторов ФДЭ5 при легочной артериальной гипертензии, подтипе легочной гипертензии, продемонстрировали их сильные эффекты в снижении легочной гипертензии и ремоделирования сосудов, а также в улучшении симптомов и смертности у пациентов с этим заболеванием. Было показано, что длительное лечение ингибитором PDE5 усиливает путь натрийуретический пептид-цГМФ, подавляет сигнальный путь Ca 2+ и изменяет тонус сосудов в легочных артериях на моделях крыс.
Доброкачественная гиперплазия предстательной железы
С 2011 г. препарат длительного действия тадалафил лицензирован для лечения симптомов со стороны мочевыводящих путей, вызванных доброкачественной гиперплазией предстательной железы.
Показания к применению ингибиторов ФДЭ5 в будущем
Сердечно-сосудистые заболевания
Ингибиторы PDE5 имеют широкий спектр эффектов на сердечно-сосудистую систему, помимо их острого гемодинамического влияния. Например, было показано, что ингибиторы PDE5 улучшают несколько параметров функции эндотелия. Все чаще оценивается их использование для лечения системной гипертензии (включая резистентную к лечению гипертонию), кардиопротекции , сердечной недостаточности и заболеваний периферических артерий .
Сердечная недостаточность
Ингибиторы PDE5 показали себя многообещающими при лечении сердечной недостаточности со сниженной фракцией выброса за счет нескольких положительных эффектов на сосудистую сеть легких , ремоделирование сердца и диастолическую функцию . Исследование показало, что эффективное лечение легочной артериальной гипертензии силденафилом улучшает функциональные возможности и снижает массу правого желудочка у пациентов. Эффекты ремоделирования правого желудочка были значительно сильнее по сравнению с неселективным антагонистом эндотелиальных рецепторов бозентаном . Однако ингибиторы ФДЭ5 могут быть вредными для пациентов с сердечной недостаточностью с сохраненной фракцией выброса из-за потенциальных отрицательных инотропных эффектов.
Хроническое заболевание почек
Экспериментальные исследования на животных показали, что ингибиторы ФДЭ5 могут обратить вспять повреждение почек независимо от их воздействия на артериальное давление через внутрипочечные механизмы. У людей ингибиторы PDE5 также снижают протеинурию , маркер повреждения почек. Однако успешное внедрение ингибиторов SGLT2 и антагонистов рецепторов эндотелина в область почечной терапии делает маловероятной разработку ингибиторов PDE5 для этой цели.
Сахарный диабет
Было показано, что ингибиторы ФДЭ5 обладают различными макрососудистыми , микрососудистыми и метаболическими преимуществами при сахарном диабете , и в большом исследовании мужчин с сахарным диабетом 2 типа было обнаружено, что агенты значительно снижают риск смерти пациентов от любой причины. Неясно, в какой степени это наблюдение отражает защитные эффекты ингибиторов ФДЭ5 против сердечно-сосудистых и почечных заболеваний.
Феномен Рейно
Было показано, что силденафил не менее эффективен, чем блокаторы кальциевых каналов, в лечении тяжелого феномена Рейно (RP), связанного с системным склерозом и язвой пальцев. При приеме силденафила в течение 4 недель у субъектов снизилась средняя частота и продолжительность приступов Рейно и значительно снизился средний балл состояния Рейно. Скорость капиллярного кровотока также увеличилась у каждого отдельного пациента, а средняя скорость капиллярного кровотока у всех пациентов значительно увеличилась. Эти результаты пришли без значительного снижения системного артериального давления . Однако терапевтические эффекты ингибиторов ФДЭ5 при первичной (идиопатической) РП менее четко определены.
Инсульт
Было показано, что силденафил значительно улучшает нервно-сосудистую связь, не влияя на общий церебральный кровоток, за счет повышения уровня цГМФ в головном мозге, вызывая нейрогенез и уменьшая неврологический дефицит у крыс через 2 или 24 часа после инсульта. Эти экспериментальные данные предполагают, что ингибиторы ФДЭ5 могут играть роль в ускорении восстановления после инсульта . Однако исследования на людях остаются безрезультатными.
Преждевременная эякуляция
Согласно недавним исследованиям, добавление ингибиторов ФДЭ5 к препаратам СИОЗС (например, пароксетину) для лечения преждевременной эякуляции может привести к лучшему контролю эякуляции. Возможный механизм основан на системе трансдукции оксида азота (NO) / цГМФ как центрального и периферического медиатора ингибирующей неадренергической, нехолинергической нитрергической нейротрансмиссии в мочеполовой системе.
Расстройство женского сексуального возбуждения
PDE5 экспрессируется в кавернозном теле клитора, а также в гладких мышцах и эпителии влагалища. Следовательно, возможно, что ингибиторы ФДЭ5 могут влиять на расстройство женского сексуального возбуждения, но необходимы дальнейшие исследования. Было показано, что повышенные уровни цГМФ возникают в культивируемых человеком клетках гладких мышц влагалища, обработанных ингибитором ФДЭ5, что предполагает участие оси NO / цГМФ в женской сексуальной реакции.
Расстройство сексуального истощения
Сходство многих ингибиторов PDE5 со структурой многих аналогов кофеина , которые также являются антагонистами аденозина, предполагает, что в будущем, возможно, появится возможность разработать ингибитор PDE5, который, как и кофеин, также является антагонистом аденозина.
Открытие
ФДЭ5 - это фермент, который впервые был очищен в 1980 году из легкого крысы. PDE5 превращает внутриклеточный цГМФ в нуклеотидный GMP. Многие ткани содержат PDE5, такие как легкие, почки, мозг, тромбоциты, печень, простата, уретра, мочевой пузырь и гладкие мышцы. Из-за локализации PDE5 в гладкой мышечной ткани были разработаны ингибиторы для лечения эректильной дисфункции наряду с легочной гипертензией .
Силденафил был впервые представлен для клинических испытаний в 1989 году. Он явился результатом обширных исследований химических агентов, нацеленных на ФДЭ5, которые могут быть эффективными при лечении ишемической болезни сердца . Силденафил не оказался эффективным при ишемической болезни сердца, но был обнаружен интересный побочный эффект - эрекция полового члена . Этот побочный эффект вскоре стал основной областью исследования. Ингибитор очень селективен по отношению к семейству PDE5.
Силденафил - это прототип ингибиторов ФДЭ5, который компания Pfizer выпустила под названием Виагра . Он был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в 1998 году как первое пероральное лекарство от эректильной дисфункции. Позже, в 2005 году, он был одобрен для лечения легочной артериальной гипертензии. Варденафил и тадалафил были открыты в 1990 году. Эти препараты появились в результате исследовательских программ, направленных на поиск ингибиторов ФДЭ5 для лечения сердечно-сосудистых заболеваний и эректильной дисфункции. Два ингибитора PDE5 вскоре стали лечить эти состояния.
Тадалафил является наиболее универсальным ингибитором и имеет самый длительный период полувыведения - 17,5 часов. Это позволяет увеличить терапевтическое окно и поэтому часто оказывается более удобным лекарством, чем другие препараты с более коротким терапевтическим периодом. Тадалафил более биодоступен (80%), чем силденафил (40%) и варденафил (15%), но он имеет медленную абсорбцию, или около 2 часов по сравнению с 50 минутами силденфила. Варденафил наиболее известен своей эффективностью.
Из-за серьезных побочных эффектов и неудовлетворенности пациентов текущим выбором терапии другие ингибиторы недавно были одобрены для клинического использования. Эти ингибиторы - уденфил, аванафил, лоденафил и мироденафил.
Разработка
Биологическая активность
Эрекция полового члена
Эрекция полового члена - это гемодинамическое событие в гладких мышцах пещеристого тела. PDE5 является основным ферментом гидролиза цГМФ, обнаруженным в кавернозном теле полового члена. Эрекция вызывается высвобождением нейромедиатора оксида азота (NO) из неадренергических и нехолинергических нейронов из нервных окончаний полового члена, а также из эндотелиальных клеток . NO активирует растворимую гуанилилциклазу в гладкомышечных клетках полового члена, что приводит к увеличению производства 3'-5'-циклического гуанозинмонофосфата из гуанозин-5'-трифосфата (GTP). Циклический GMP связывается с цГМФ-зависимой протеинкиназой (PKG1), которая фосфорилирует несколько белков, что приводит к снижению внутриклеточного кальция. Более низкий уровень внутриклеточного кальция приводит к расслаблению гладких мышц и, в конечном итоге, к эрекции полового члена. Этот путь показан на рисунке 1 .
Эректильная дисфункция
ФДЭ5 разрушает цГМФ и, следовательно, подавляет эрекцию. Как показано на рисунке 1 , ингибирование PDE5 снижает деградацию цГМФ и приводит к эрекции полового члена. Благодаря этому действию ингибиторы PDE5 были разработаны для лечения эректильной дисфункции полового члена.
Фермент фосфодиэстераза 5
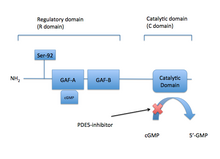
Фермент PDE5 имеет молекулярную массу 200 кДа и его активное состояние представляет собой гомодимер . PDE5 состоит из мономеров, каждый из которых содержит два основных функциональных домена: регуляторный домен (R-домен), расположенный в N-концевой части белка, и каталитический домен (C-домен), расположенный в более C-концевой части белка. .
Домен R содержит специфический аллостерический сайт связывания цГМФ, который контролирует функцию ферментов. Этот сайт специфического связывания состоит из субдомена GAF (цГМФ-специфическая цГМФ-стимулированная ФДЭ, аденилатциклаза и FhlA), который расположен в N-концевом участке специфических белков. Аллостерический сайт связывания GAF состоит из GAFa и GAFb, где GAFa имеет более высокое сродство связывания. Важность и функциональная роль двух гомологичных сайтов связывания неизвестны.
Конформационное изменение происходит, когда цГМФ связывается с аллостерическим сайтом, который экспонирует серин и позволяет фосфорилирование. Результаты фосфорилирования серина приводят к усилению гидролиза цГМФ в каталитическом домене. Сродство каталитического домена к цГМФ увеличивается и дополнительно увеличивает активность каталитического домена PDE5. Через домен C внутриклеточный цГМФ быстро разрушается PDE5, что минимизирует активность цГМФ на его субстрате PKG1 за счет отщепления циклической фосфатной части цГМФ до GMP. GMP - неактивная молекула, не имеющая активности вторичного мессенджера.
Фосфорилирование одиночного серина с помощью PKG1 и аллостерического сайта связывания cGMP активирует каталитическую активность PDE5, и в результате происходит регуляция передачи сигналов cGMP / NO / PKG1 по отрицательной обратной связи . Таким образом, цГМФ взаимодействует как с аллостерическим, так и с каталитическим доменом фермента ФДЭ5, а ингибиторы ФДЭ5 конкурируют с цГМФ за связывание в каталитическом домене, что приводит к более высоким уровням цГМФ. Домены PDE5 показаны на рисунке 2 .
Ингибиторы PDE5
Ингибиторы ФДЭ5 силденафил, варденафил и тадалафил являются конкурентными и обратимыми ингибиторами гидролиза цГМФ каталитической стороной ФДЭ5. Структуры варденафила и силденафила схожи, они оба содержат аналогичное структурированное пуриновое кольцо цГМФ, что способствует их свойствам действовать как конкурентный ингибитор ФДЭ5. Различие молекулярных структур является причиной взаимодействия с каталитическим сайтом PDE5 и улучшает сродство этих соединений по сравнению с селективностью цГМФ.
Фармакофор
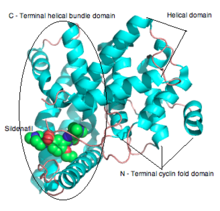
Фармакофорная модель PDE5 обычно состоит из одного акцептора водородной связи, одной гидрофобной алифатической углеродной цепи и двух ароматических колец. Небольшой гидрофобный карман и H-петля фермента PDE5 важны для сродства связывания ингибиторов PDE5. Во многих случаях при связывании ингибитора наблюдаются позиционные и конформационные изменения.
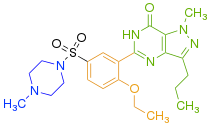
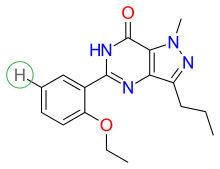
Активный сайт PDE5 расположен в домене спирального пучка в центре домена C (каталитический домен). Карман субстрата состоит из четырех субсайтов: M-сайт (участок связывания металла), Q-карман (сердцевинный карман), H-карман (гидрофобный карман) и L-область (область крышки), как показано на рисунке 3 . Карман Q вмещает пиразолопиримидиноновую группу силденафила. Это предполагает, что другие химические вещества, подобные гуанидиновым группам цГМФ, также могут связываться в этой области. Аминокислотные остатки Gln817, Phe820, Val782 и Tyr612 расположены в Q-кармане, они высококонсервативны во всех PDE. Амидный фрагмент пиразолопиримидиноновой группы образует бидентатную водородную связь с ɣ-амидной группой Gln817. Трехмерная структура силденафила представлена на рисунке 4 .
Побочные эффекты
Ингибиторы PDE5 обычно хорошо переносятся с побочными эффектами, включая преходящие головные боли, приливы, диспепсию, заложенность и головокружение. Также были сообщения о временных нарушениях зрения при приеме силденафила и, в меньшей степени, варденафила, а также о болях в спине и мышцах при приеме тадалафила. Эти побочные эффекты могут быть отнесены к непредвиденным эффектам ингибиторов PDE5 против других изоферментов PDE, таких как PDE1, PDE6 и PDE11. Предполагается, что улучшенная селективность ингибиторов ФДЭ5 может привести к меньшему количеству побочных эффектов. Например, варденафил и тадалафил продемонстрировали снижение побочных эффектов, вероятно, из-за улучшенной селективности в отношении ФДЭ5. Однако в настоящее время высокоселективные ингибиторы PDE5 не разрабатываются.
Пациенты, принимающие нитраты , альфа-блокаторы или стимуляторы рГЦ в течение 24 часов после введения ингибитора ФДЭ5 (или 48 часов для тадалафила), могут испытывать симптоматическую гипотензию , поэтому одновременное применение противопоказано. Ингибиторы ФДЭ5 также противопоказаны пациентам с наследственными заболеваниями глаз, такими как пигментный ретинит, из-за небольшого повышенного риска неартеритической ишемической оптической нейропатии у пациентов, принимающих лекарство.
Нарушение слуха является одним из факторов риска для тех, кто принимает ингибиторы ФДЭ5, и оно зарегистрировано для всех доступных на рынке лекарств. Эта проблема может быть связана с высоким уровнем воздействия цГМФ на волосковые клетки улитки. Сообщалось, что ингибиторы ФДЭ5 (силденафил и варденафил) вызывают временные нарушения зрения, вероятно, из-за ингибирования ФДЭ6.
Несколько отчетов касаются подходов к улучшению ингибиторов PDE5, когда химические группы были заменены для повышения эффективности и селективности, что потенциально должно привести к лекарствам с меньшим количеством побочных эффектов.
Взаимосвязь между структурой и деятельностью (SAR)
Силденафил, первый ингибитор ФДЭ5, был открыт в рамках программы рациональной разработки лекарств. Соединение было сильнодействующим и селективным по сравнению с PDE5, но не имело предпочтительных фармакологических свойств.
Взаимосвязь между структурой и активностью (SAR) показана на рисунках 5 , 6 и 7 . На рисунке 5 показаны три основные группы силденафила: R1, R2 и R3. R1 представляет собой пиразолопиримидиноновое кольцо, R2 представляет собой этоксифенильное кольцо и R3 представляет собой метилпиперазиновое кольцо. Группа R1 отвечает за связывание препарата с его активным сайтом связывания PDE5.
Растворимость - одно из повышенных фармакологических свойств. Группа была заменена на атом водорода, как показано на рисунке 6 . Сульфонамидную группу , была выбрана более низкой липофильности и увеличение растворимости , как показано на рисунке 7 .
Растворимость была дополнительно увеличена путем размещения метильной группы в положениях R, как показано на рисунке 7 . Другие ингибиторы фосфодиэстеразы-5 были разработаны на основе структуры, представленной на рисунке 7 .
Другое исследование
Хотя основное применение ингибиторов ФДЭ5 было при эректильной дисфункции, большой интерес вызывают ингибиторы ФДЭ5 как новые многообещающие терапевтические агенты для лечения других заболеваний, таких как болезнь Альцгеймера . Повышение уровня цГМФ за счет ингибирования ФДЭ5 обеспечивает способ улучшения памяти и обучения. PDE5 также считается потенциальным терапевтическим средством от паразитарных заболеваний, таких как африканская сонная болезнь . В структуру силденафила были внесены стратегические изменения, чтобы молекула могла проецироваться в специфический карман для паразитов (p-карман). Аналогичный подход был использован для создания терапевтических агентов Plasmodium falciparum .
Ингибиторы ФДЭ5 в клинических испытаниях
| Препарат, средство, медикамент | Статус клинического исследования (2005 г.) | Индикация | Режиссер |
|---|---|---|---|
| UK357903 | Фаза II | Эректильная дисфункция (ингибитор ФДЭ5 второго поколения) | Pfizer |
| Аванафил | Фаза II | Эректильная дисфункция и расстройство сексуального возбуждения у женщин | Танабэ |
| Уденафил (DA-8159) | Фаза II | Эндотелиальная дисфункция, эректильная дисфункция и эректильная дисфункция, связанные с ожирением , диабетом и приемом СИОЗС | Dong-A Pharmaceutical |